RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 28/03/2013
TEMOZOLOMIDE MYLAN 5 mg, gélule
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Témozolomide ..................................................................................................................................... 5 mg
Excipients:
Chaque gélule contient 87 mg de lactose anhydre.
Pour la liste complète des excipients, voir rubrique 6.1.
Gélule.
Les gélules ont un corps et une coiffe opaques blancs, elles sont marquées de deux rayures vertes sur la coiffe et un « T 5 mg » vert sur le corps.
4.1. Indications thérapeutiques
Témozolomide Mylan gélules est indiqué pour le traitement:
· des patients adultes atteints d'un glioblastome multiforme nouvellement diagnostiqué en association avec la radiothérapie (RT) puis en traitement en monothérapie,
· des enfants à partir de 3 ans, des adolescents et des patients adultes atteints d'un gliome malin, tel que glioblastome multiforme ou astrocytome anaplasique, présentant une récidive ou une progression après un traitement standard.
4.2. Posologie et mode d'administration
Témozolomide Mylan gélules doit uniquement être prescrit par des médecins qui ont l'expérience du traitement oncologique des tumeurs cérébrales.
Un traitement antiémétique peut être administré (voir rubrique 4.4).
Posologie
Patients adultes avec un glioblastome multiforme nouvellement diagnostiqué
Témozolomide Mylan gélules est administré en association avec la radiothérapie focale (phase concomitante) suivi de témozolomide (TMZ) en monothérapie jusqu'à 6 cycles (phase de monothérapie).
Phase concomitante
TMZ est administré par voie orale à une dose de 75 mg/m2 quotidiennement pendant 42 jours en association à la radiothérapie focale (60 Gy administrés en 30 fractions). Aucune réduction de dose n'est recommandée, mais le report ou l'interruption de l'administration de TMZ doit être décidé de manière hebdomadaire selon des critères de toxicité hématologique et non hématologique.
L'administration de TMZ peut être prolongée au-delà de la période concomitante de 42 jours (jusqu'à 49 jours) si toutes les conditions suivantes sont satisfaites:
· taux de neutrophiles (PNN) en valeur absolue ≥ 1,5 x 109/l,
· taux de plaquettes ≥ 100 x 109/l,
· toxicité non hématologique selon la classification « Common Toxicity Criteria » (CTC) ≤ Grade 1 (excepté pour l'alopécie, les nausées et les vomissements).
Pendant le traitement une Numération Formule Sanguine complète doit être effectuée chaque semaine. L'administration de TMZ doit être interrompue temporairement ou arrêtée définitivement pendant la phase concomitante selon les critères de toxicité hématologique et non hématologique tels que décrits dans le Tableau 1.
Tableau 1. Interruption temporaire ou arrêt définitif du traitement par TMZ pendant la phase concomitante par radiothérapie et TMZ
|
Toxicité |
Interruption temporairea du TMZ |
Arrêt definitif du TMZ |
|
|
Taux de neutrophiles en valeur absolue |
≥ 0,5 et < 1,5 x 109/l |
< 0,5 x 109/l |
|
|
Taux de plaquettes |
≥ 10 et < 100 x 109/l |
< 10 x 109/l |
|
|
Toxicité non hématologique CTC |
Grade 2 CTC |
Grade 3 ou 4 CTC |
aLe traitement concomitant avec TMZ peut être repris lorsque toutes les conditions suivantes sont rencontrées: taux de neutrophiles en valeur absolue ≥ 1,5 x 109/l; taux de plaquettes ≥ 100 x 109/l; toxicité non hématologique CTC ≤ Grade 1 (excepté pour l'alopécie, les nausées, les vomissements).
Phase de monothérapie
Quatre semaines après avoir terminé la phase concomitante de traitement par TMZ + RT, TMZ est administré jusqu'à 6 cycles de traitement en monothérapie. La dose pendant le cycle 1 (monothérapie) est de 150 mg/m2 une fois par jour pendant 5 jours suivis de 23 jours sans traitement. Au début du cycle 2, la dose est augmentée à 200 mg/m2 si la toxicité non hématologique CTC pour le cycle 1 est de Grade ≤ 2 (excepté pour l'alopécie, les nausées et les vomissements), le taux de neutrophiles (PNN) en valeur absolue est ≥ 1,5 x 109/l, et le taux de plaquettes est ≥ 100 x 109/l. Si la dose n'est pas augmentée au cycle 2, l'augmentation ne doit pas être effectuée aux cycles suivants. Une fois augmentée, la dose demeure à 200 mg/m2 par jour pour les 5 premiers jours de chaque cycle suivant à moins qu'une toxicité apparaisse. Les diminutions de dose et les arrêts pendant la phase de monothérapie doivent être effectuées selon les tableaux 2 et 3.
Pendant le traitement, une Numération Formule Sanguine complète doit être effectuée au Jour 22 (21 jours après la première dose de TMZ). La dose doit être réduite ou l'administration interrompue selon le Tableau 3.
Tableau 2. Différents niveaux de dose de TMZ pour le traitement en monothérapie
|
Niveau de dose |
Dose de TMZ (mg/m2/jour) |
Remarques |
|
|
-1 |
100 |
Diminution pour toxicité antérieure |
|
|
0 |
150 |
Dose pendant le cycle 1 |
|
|
1 |
200 |
Dose pendant les cycles 2 à 6 en l'absence de toxicité |
Tableau 3. Diminution de dose de TMZ ou arrêt pendant le traitement en monothérapie
|
Toxicité |
Diminution de TMZ d'un niveau de dosea |
Arrêt de TMZ |
|
|
Taux de neutrophiles en valeur absolue |
< 1,0 x 109 /l |
Voir annotationb |
|
|
Taux de plaquettes |
< 50 x 109/l |
Voir annotationb |
|
|
Toxicité non hématologique CTC |
Grade 3 CTC |
Grade 4b CTC |
ales niveaux de dose de TMZ sont listés dans le Tableau 2.
· ble TMZ doit être arrêté si:le niveau de posologie -1 (100 mg/m2) provoque toujours une toxicité inacceptable
· la même toxicité non hématologique Grade 3 (excepté pour l'alopécie, les nausées, les vomissements) se reproduit après réduction de posologie.
·
Patients adultes et enfants âgés de 3 ans ou plus atteints de gliome malin en progression ou récidiv:
Un cycle de traitement comprend 28 jours. Chez les patients n'ayant pas reçu de chimiothérapie au préalable, TMZ est administré par voie orale à la dose de 200 mg/m2 une fois par jour pendant les 5 premiers jours du cycle puis le traitement devra être arrêté pendant les 23 jours suivants (total de 28 jours). Chez les patients ayant reçu une chimiothérapie préalable, la dose initiale est de 150 mg/m2 une fois par jour, puis est augmentée lors du second cycle à 200 mg/m2 une fois par jour, pendant 5 jours s'il n'y a pas de toxicité hématologique (voir rubrique 4.4).
Populations spéciales
Enfants
Chez les enfants âgés de 3 ans ou plus, TMZ est uniquement utilisé dans le traitement du gliome malin en progression ou récidive. Il n'y a pas d'expérience clinique de l'utilisation de TMZ chez l'enfant de moins de 3 ans. L'expérience chez les enfants plus âgés est très limitée (voir rubriques 4.4 et 5.1).
Patients atteints d'insuffisance hépatique ou rénale
Les paramètres pharmacocinétiques du TMZ étaient comparables chez les patients ayant une fonction hépatique normale et chez ceux atteints d'insuffisance hépatique faible ou modérée. Aucune donnée n'est disponible concernant l'administration de TMZ chez les patients atteints d'insuffisance hépatique sévère (stade C de la classification de Child) ou d'insuffisance rénale. Sur la base des propriétés pharmacocinétiques du TMZ, il est peu probable qu'une réduction de dose soit nécessaire chez les patients atteints d'insuffisance hépatique sévère ou de n'importe quel degré d'insuffisance rénale. Cependant, des précautions doivent être prises lorsque TMZ est administré chez ces patients.
Patients âgés
Sur la base d'une analyse pharmacocinétique de population chez des patients âgés de 19 à 78 ans, la clairance du TMZ n'est pas affectée par l'âge. Cependant, les patients âgés (> 70 ans) semblent avoir un risque augmenté de neutropénie et trombocytopénie (voir rubrique 4.4).
Mode d'administration
Témozolomide Mylan gélules doit être administré à jeun.
Les gélules doivent être avalées entières avec un verre d'eau et ne doivent pas être ouvertes ni mâchées.
Si des vomissements surviennent après l'administration de la dose, ne pas administrer une deuxième dose le même jour.
· Hypersensibilité à la substance active ou à l'un des excipients.
· Hypersensibilité à la dacarbazine (DTIC).
· Myélosuppression sévère (voir rubrique 4.4).
4.4. Mises en garde spéciales et précautions d'emploi
Pneumonie à Pneumocystis carinii
Dans un essai pilote les patients ayant reçu TMZ de manière concomitante à la radiothérapie sur un schéma de 42 jours ont montré un risque particulier de développer des pneumonies à Pneumocystis carinii (PPC). Ainsi, une prophylaxie pour la pneumonie à PPC est-elle requise pour tous les patients recevant TMZ de manière concomitante avec la radiothérapie pour les 42 jours de traitement (avec un maximum de 49 jours) quelque soit le taux de lymphocytes. Si une lymphopénie se produit, ils doivent continuer la prophylaxie jusqu'à retrouver une lymphopénie de Grade ≤ 1.
Il peut y avoir une fréquence plus importante de PPC quand TMZ est administré selon un schéma de traitement plus long. Néanmoins, tous les patients recevant TMZ, particulièrement les patients recevant des stéroïdes, doivent être surveillés attentivement concernant le développement de PPC, quelque soit le schéma de traitement.
Tumeurs malignes
Des cas de syndromes myélodysplasiques et de tumeurs malignes secondaires, incluant la leucémie myéloïde, ont également été observés, très rarement (voir rubrique 4.8).
Traitement antiémétique
Les nausées et les vomissements sont très fréquemment associés à TMZ.
Un traitement antiémétique peut être administré avant ou après administration de TMZ.
Patients adultes atteints d'un glioblastome multiforme nouvellement diagnostiqué
Une prophylaxie antiémétique est recommandée avant la dose initiale en phase concomitante. Une telle prophylaxie est fortement recommandée pendant la phase de monothérapie.
Patients avec un gliome malin en progression ou récidive
Les patients qui ont eu des vomissements sévères (Grade 3 ou 4) au cours des cycles de traitement antérieurs peuvent nécessiter un traitement antiémétique.
Paramètres biologiques
Avant administration, les paramètres biologiques doivent être les suivants: PNN ≥ 1,5 x 109/l et taux de plaquettes ≥ 100 x 109/l. Une Numération Formule Sanguine complète doit être effectuée au Jour 22 (21 jours après la première dose) ou dans un délai de 48 heures suivant ce jour, et chaque semaine jusqu'à un taux PNN ≥ 1,5 x 109/l et un taux de plaquettes ≥ 100 x 109/l. Si le taux de PNN tombe à une valeur < 1,0 x 109/l ou le taux de plaquettes est < 50 x 109/l pendant n'importe quel cycle, la dose doit être diminuée d'un niveau au prochain cycle (voir rubrique 4.2). Les niveaux de doses incluent 100 mg/m2, 150 mg/m2, et 200 mg/m2. La plus basse dose recommandée est 100 mg/m2.
Utilisation en pédiatrie
Il n'existe aucune expérience clinique de l'utilisation de TMZ chez les enfants de moins de 3 ans. L'expérience chez les enfants plus âgés et les adolescents est très limitée (voir rubriques 4.2 et 5.1).
Patients âgés (> 70 ans)
Les patients âgés présentent un risque plus élevé de neutropénie et de thrombocytopénie comparativement aux patients plus jeunes. Par conséquent, une attention particulière est nécessaire lorsque TMZ est administré chez les patients âgés.
Hommes traités
Il est conseillé aux hommes traités par TMZ de ne pas procréer jusqu'à 6 mois après la dernière dose prise et de se renseigner sur la cryoconservation du sperme avant d'initier le traitement (voir rubrique 4.6).
Lactose
Ce médicament contient du lactose. Son utilisation est déconseillée chez les patients présentant une intolérance au galactose, un déficit en lactase de Lapp ou un syndrome de malabsorption du glucose et du galactose (maladies héréditaires rares).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les études d'interaction n'ont été réalisées que chez l'adulte.
Dans une autre étude de phase I, l'administration simultanée de TMZ et de ranitidine ne modifie pas l'absorption du témozolomide ou l'exposition à son métabolite actif le monométhyl triazénoimidazole carboxamide (MTIC).
L'administration de TMZ lors des repas se traduit par une diminution de 33 % de la Cmax et par une diminution de 9 % de l'aire sous la courbe (ASC). Comme on ne peut pas exclure que ce changement de la Cmax ait une signification clinique, Témozolomide Mylan doit être administré en dehors des repas.
Selon une analyse pharmacocinétique de population lors des essais de phase II, l'administration concomitante de dexaméthasone, de prochlorpérazine, de phénytoïne, de carbamazépine, d'ondansétron, d'antagonistes des récepteurs H2, ou de phénobarbital ne modifie pas la clairance du TMZ. L'administration concomitante d'acide valproïque a été associée à une diminution faible mais statistiquement significative de la clairance du TMZ.
Aucune étude n'a été réalisée pour déterminer l'effet du TMZ sur le métabolisme ou l'élimination d'autres médicaments. Cependant, comme le TMZ ne subit pas de métabolisme hépatique et présente une faible liaison aux protéines plasmatiques, il ne devrait pas affecter les paramètres pharmacocinétiques d'autres médicaments (voir rubrique 5.2).
L'utilisation de TMZ en association avec d'autres agents myélosuppresseurs est susceptible d'accroître le risque de myélosuppression.
Il n'existe aucune donnée chez la femme enceinte. Lors des études précliniques conduites chez le rat et le lapin ayant reçu une dose de 150 mg/m2 de TMZ, des effets tératogènes et/ou toxiques pour le ftus ont été démontrés (voir rubrique 5.3). Témozolomide Mylan gélules ne doit pas être administré chez la femme enceinte. Si l'administration est envisagée pendant la grossesse, la patiente doit être prévenue du risque potentiel pour le ftus. Il est conseillé aux femmes en âge de procréer d'utiliser une contraception efficace afin d'éviter toute grossesse lorsqu'elles reçoivent TMZ.
On ne sait pas si TMZ est excrété dans le lait maternel. Par conséquent, l'allaitement doit être interrompu pendant le traitement par TMZ.
Fertilité masculine
TMZ peut avoir des effets génotoxiques. Par conséquent, il est conseillé aux hommes traités par ce dernier de ne pas procréer jusqu'à 6 mois après avoir reçu la dernière dose et de se renseigner sur la cryoconservation du sperme avant d'initier le traitement, compte tenu de la possibilité d'infertilité irréversible due à la thérapie avec le TMZ.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets sur l'aptitude à conduire des véhicules et à utiliser des machines n'ont pas été étudiés. L'aptitude à conduire des véhicules et à utiliser des machines peut être altérée chez les patients traités avec TMZ en raison de la fatigue et de la somnolence.
Au sein de chaque fréquence de groupe, les effets indésirables doivent être présentés suivant un ordre décroissant de gravité.
Expérience issue d'essai clinique
Chez les patients traités avec TMZ, que celui-ci soit utilisé en association avec la radiothérapie ou en monothérapie suivi d'une radiothérapie pour un glioblastome multiforme nouvellement diagnostiqué, ou qu'il soit administré en monothérapie chez les patients atteints d'un gliome en progression ou récidive, les effets indésirables très fréquents rapportés étaient similaires: nausées, vomissements, constipation, anorexie, mal de tête et fatigue. Des convulsions ont été rapportées très fréquemment chez les patients ayant un glioblastome multiforme nouvellement diagnostiqué en monothérapie, et un rash a été rapporté très fréquemment chez les patients ayant un glioblastome multiforme nouvellement diagnostiqué recevant TMZ et la radiothérapie de manière concomitante et également en monothérapie, et fréquemment chez les patients présentant un gliome en récidive. La plupart des effets indésirables hématologiques ont été rapportés fréquemment ou très fréquemment dans les deux indications (Tableaux 4 et 5); la fréquence des anomalies des paramètres biologiques de Grade 3-4 est mentionnée après chaque tableau.
Dans les tableaux, les effets indésirables sont listés selon la Classification des Systèmes d'Organe et par fréquence. Les groupes de fréquence sont définis selon la convention suivante: très fréquent (≥ 1/10); fréquent (≥ 1/100, < 1/10); peu fréquent (≥ 1/1 000, < 1/100). Au sein de chaque groupe de fréquence, les effets indésirables doivent être présentés suivant un ordre décroissant de gravité.
Glioblastome multiforme nouvellement diagnostiqué
Le tableau 4 rapporte les événements indésirables liés au traitement observés chez les patients atteints d'un glioblastome multiforme nouvellement diagnostiqué pendant les phases concomitante et de monothérapie du traitement.
Tableau 4: Effets liés au traitement observés pendant les phases concomitante et de monothérapie du traitement chez les patients atteints d'un glioblastome multiforme nouvellement diagnostiqué
|
Classification des systèmes d'organe |
TMZ + RT concomitante (n=288*) |
TMZ en monothérapie (n=224) |
|
|
Infections et infestations |
|
||
|
Fréquent: |
Infection, Herpes simplex, infection des plaies, pharyngite, candidose orale |
Infection, candidose orale |
|
|
Peu fréquent: |
|
Herpes simplex, zona, symptômes pseudo-grippaux |
|
|
Affections hématologiques et du système lymphatique |
|
||
|
Fréquent: |
Neutropénie, thrombocytopénie, lymphopénie, leucopénie |
Neutropénie fébrile, thrombocytopénie, anémie, leucopénie |
|
|
Peu fréquent: |
Neutropénie fébrile, anémie |
Lymphopénie, pétéchie |
|
|
Affections endocriniennes |
|
||
|
Peu fréquent: |
Syndrome cushingoïde |
Syndrome cushingoïde |
|
|
Troubles du métabolisme et de la nutrition |
|
||
|
Très fréquent |
Anorexie |
Anorexie |
|
|
Fréquent |
Hyperglycémie, perte de poids |
Perte de poids |
|
|
Peu fréquent |
Hypokaliémie, augmentation des phosphatases alcalines, prise de poids |
Hyperglycémie, prise de poids |
|
|
Affections psychiatriques |
|
||
|
Fréquent: |
Anxiété, instabilité émotionnelle, insomnie |
Anxiété, dépression, instabilité émotionnelle, insomnie |
|
|
Peu fréquent: |
Agitation, apathie, trouble du comportement, dépression, hallucination |
Hallucination, amnésie |
|
|
Affections du système nerveux |
|
||
|
Très fréquent: |
Céphalée |
Convulsions, céphalée |
|
|
Fréquent: |
Convulsions, baisse de conscience, somnolence, aphasie, trouble de l'équilibre, étourdissements, confusion, troubles de la mémoire, concentration altérée, neuropathie, paresthésie, trouble de la parole, tremblements |
Hémiparésie, aphasie, troubles de l'équilibre,somnolence, confusion, étourdissements, troubles de la mémoire, concentration altérée, dysphasie, troubles neurologiques (NOS), neuropathie, neuropathie périphérique, paresthésie, trouble de la parole, tremblements |
|
|
Peu fréquent: |
Etat de mal épileptique, trouble extrapyramidal, hémiparésie, ataxie, altération de la cognition, dysphasie, démarche anormale, hyperesthésie, hypoesthésie, troubles neurologiques (NOS), neuropathie périphérique |
Hémiplegie, ataxie, coordination anormale, démarche anormale, hyperesthésie, trouble sensoriel |
|
|
Affections oculaires |
|
||
|
Fréquent: |
Vision floue |
Trouble du champ visuel, vision floue, diplopie |
|
|
Peu fréquent: |
Hémianopsie, acuité visuelle réduite, trouble de la vision, défaut du champ visuel, douleur oculaire |
Acuité visuelle réduite, douleur oculaire, sécheresse oculaire |
|
|
Affections de l'oreille et du labyrinthe |
|
||
|
Fréquent: |
Baisse de l'audition |
Baisse de l'audition, acouphène |
|
|
Peu fréquent: |
Otite moyenne, acouphène, hyperacousie, douleur à l'oreille |
Surdité, vertige, douleur à l'oreille |
|
|
Affections cardiaques |
|
||
|
Fréquent: |
Palpitation |
|
|
|
Affections vasculaires |
|
||
|
Fréquent: |
Hémorragie, dème, dème des jambes |
Hémorragie, thrombose veineuse profonde, dème des jambes |
|
|
Peu fréquent: |
Hémorragie cérébrale, hypertension |
Embolie pulmonaire, dème, dème périphérique |
|
|
Affections respiratoires, thoraciques et médiastinales |
|
||
|
Fréquent: |
Dyspnée, toux |
Dyspnée, toux |
|
|
Peu fréquent: |
Pneumonie, infection des voies aériennes hautes, congestion nasale |
Pneumonie, sinusite, infection des voies aériennes hautes, bronchite |
|
|
Affections gastro-intestinales |
|
||
|
Très fréquent: |
Constipation, nausées, vomissements |
Constipation, nausées, vomissements |
|
|
Fréquent: |
Stomatite, diarrhée, douleur abdominale, dyspepsie, dysphagie |
Stomatite, diarrhée, dyspepsie, dysphagie, bouche sèche |
|
|
Peu fréquent: |
|
Distension abdominale, incontinence fécale, troubles gastro-intestinaux (NOS), gastro-entérite, hémorroïdes |
|
|
Affections de la peau et du tissu sous-cutané |
|
||
|
Très fréquent: |
Rash, alopécie |
Rash, alopécie |
|
|
Fréquent: |
Dermatite, sécheresse cutanée, érythème, prurit |
Sécheresse cutanée, prurit |
|
|
Peu fréquent: |
Exfoliation cutanée, réaction de photosensitivité, pigmentation anormale |
Erythème, pigmentation anormale, transpiration accrue |
|
|
Affections musculo-squelettiques et systémiques |
|
||
|
Fréquent: |
Faiblesse musculaire, arthralgie |
Faiblesse musculaire, arthralgie, douleur musculo-squelettique, myalgie |
|
|
Peu fréquent: |
Myopathie, douleur dorsale, douleur musculo-squelettique, myalgie |
Myopathie, douleur dorsale |
|
|
Affections du rein et des voies urinaires |
|
||
|
Fréquent: |
Miction fréquente, incontinence urinaire |
Incontinence urinaire |
|
|
Peu fréquent: |
|
Dysurie |
|
|
Affections des organes de reproduction et du sein |
|
||
|
Peu fréquent: |
Impuissance |
Hémorragie vaginale, ménorragie, aménorrhée, vaginite, douleur mammaire |
|
|
Troubles généraux et anomalies au site d'administration |
|
||
|
Très fréquent: |
Fatigue |
Fatigue |
|
|
Fréquent: |
Réaction allergique, fièvre, lésions radiques, dème de la face, douleur, perversion du goût |
Réaction allergique, fièvre, lésions radiques, douleur, perversion du goût |
|
|
Peu fréquent: |
Asthénie, bouffées vasomotrices, bouffées de chaleur, aggravation de l'état, raideur, décoloration de la langue, parosmie, soif |
Asthénie, dème de la face, douleur, aggravation de l'état, raideur, trouble dentaire, perversion du goût |
|
|
Investigations |
|
||
|
Fréquent: |
Augmentation des ALAT |
Augmentation des ALAT |
|
|
Peu fréquent: |
Augmentation des enzymes hépatiques, augmentation des Gamma GT, augmentation des ASAT |
|
|
*Un patient randomisé dans le bras radiothérapie seule a reçu TMZ + RT.
Résultats de laboratoire
Une myélosuppression (neutropénie et thrombocytopénie), connue comme étant la toxicité dose-limitante de la plupart des agents cytotoxiques, y compris le TMZ, a été observée. Parmi les anomalies de laboratoire associées à des événements indésirables apparues au cours de la phase concomitante et de monothérapie, les anomalies de neutrophiles de Grade 3 ou 4 incluant les événements neutropéniques étaient observés chez 8 % des patients. Les anomalies de Grades 3 ou 4 des thrombocytes, incluant les évènements de thrombocytopénie ont été observées chez 14 % des patients qui recevaient TMZ.
Gliome malin en récidive ou progression
Lors des essais cliniques, les effets indésirables liés au traitement les plus fréquemment rapportés ont été des troubles gastro-intestinaux, plus particulièrement nausées (43 %) et vomissements (36 %). Ces réactions ont été habituellement de Grade 1 ou 2 (0 à 5 épisodes de vomissements par 24 heures) et ont disparu spontanément ou ont été rapidement contrôlés par un traitement antiémétique standard. L'incidence des nausées et vomissements sévères a été de 4 %.
Le tableau 5 comprend les réactions indésirables rapportées lors des essais cliniques dans le cadre de gliome malin en progression ou récidive et suite à la mise sur le marché du TMZ.
Tableau 5: Effets indésirables chez les patients atteints d'un gliome malin en progression ou récidive
|
Infections et infestations |
|
|
|
Rare: |
Infections opportunistes, incluant PPC |
|
|
Affections hématologiques et du système lymphatique |
|
|
|
Très fréquent: |
Neutropénie ou lymphopénie (Grade 3-4), thrombocytopénie (Grade 3-4) |
|
|
Peu fréquent: |
Pancytopénie, anémie (Grade 3-4), leucopénie |
|
|
Troubles du métabolisme et de la nutrition |
|
|
|
Très fréquent: |
Anorexie |
|
|
Fréquent: |
Perte de poids |
|
|
Affections du système nerveux |
|
|
|
Très fréquent: |
Céphalée |
|
|
Fréquent: |
Somnolence, étourdissements, paresthésie |
|
|
Affections respiratoires, thoraciques et médiastinales |
|
|
|
Fréquent: |
Dyspnée |
|
|
Affections gastro-intestinales |
|
|
|
Très fréquent: |
Vomissements, nausées, constipation |
|
|
Fréquent: |
Diarrhée, douleur abdominale, dyspepsie |
|
|
Affections de la peau et du tissu sous-cutanée |
|
|
|
Fréquent: |
Rash, prurit, alopécie |
|
|
Très rare: |
Erythème multiforme, érythrodermie, urticaire, exanthème |
|
|
Troubles généraux et anomalies au site d'administration |
|
|
|
Très fréquent: |
Fatigue |
|
|
Fréquent: |
Fièvre, asthénie, raideur, malaise, douleur, perversion du goût |
|
|
Très rare: |
Réactions allergiques, incluant anaphylaxie, angidème |
|
Résultats de laboratoire
Une thrombocytopénie et une neutropénie de Grade 3 ou 4 sont survenues respectivement chez 19 % et 17 %, des patients traités pour gliome malin. Cela a entraîné une hospitalisation et/ou un arrêt de TMZ respectivement chez 8 % et 4 % des patients. La myélosuppression était prévisible (habituellement lors des premiers cycles de traitement, avec un nadir entre le Jour 21 et le Jour 28), et rapidement réversible, généralement en 1 - 2 semaines. Il n'a pas été observé de myélosuppression cumulative. La présence de thrombocytopénie peut augmenter le risque de saignements, et la présence de neutropénie ou de leucopénie peut augmenter le risque d'infection.
Genre
Dans une analyse pharmacocinétique de population d'un essai clinique, il y a eu 101 femmes et 169 hommes pour qui les taux de nadir des neutrophiles étaient disponibles et 110 femmes et 174 hommes pour qui les taux de nadir des plaquettes étaient disponibles. Il y a eu des taux supérieurs de neutropénie de Grade 4 (PNN < 0,5 x 109/l), 12 % vs 5 %, et de thrombocytopénie (< 20 x 109/l), 9 % vs 3 %, chez les femmes vs chez les hommes durant le premier cycle du traitement. Dans une série de 400 sujets ayant un gliome en récidive, une neutropénie de Grade 4 est survenue chez 8 % des femmes vs 4 % des hommes et une thrombocytopénie de Grade 4 chez 8 % des femmes vs 3 % des hommes durant le premier cycle du traitement. Dans une étude de 288 sujets avec un glioblastome multiforme nouvellement diagnostiqué, une neutropénie de Grade 4 survenait chez 3 % des femmes vs 0 % des hommes et une thrombocytopénie de Grade 4 chez 1 % des femmes vs 0 % des hommes durant le premier cycle du traitement.
Depuis la commercialisation:
Les agents antinéoplasiques, et particulièrement les agents alkylants, ont été associés à un risque potentiel de syndrome myélodysplasique (SMD) et des tumeurs malignes secondaires, incluant la leucémie. De très rares cas de SMD et de tumeurs malignes secondaires, incluant la leucémie myéloïde ont été rapportés chez des patients recevant des traitements comprenant du TMZ. Une pancytopénie prolongée, qui peut engendrer une anémie aplastique a été très rarement rapportée.
Des cas de nécrolyse épidermique toxique et de syndrome de Stevens-Johnson ont été très rarement rapportés.
Des cas de pneumopathies ou de pneumopathies interstitielles ont été très rarement rapportés.
Les doses de 500, 750, 1 000 et 1 250 mg/m2 (dose totale par cycle de 5 jours) ont été évaluées cliniquement chez les patients. La toxicité dose-limitante a été la toxicité hématologique et était rapportée avec toute dose mais attendue pour être plus sévère aux doses supérieures. Un surdosage de 10 000 mg (dose totale pour un seul cycle, sur 5 jours) a été constaté chez un patient et les réactions indésirables rapportées étaient pancytopénie, pyrexie, défaillance de multiples organes et décès. Chez des patients ayant pris la dose recommandée pendant plus de 5 jours de traitement (jusqu'à 64 jours) les effets indésirables incluaient une aplasie médullaire, avec ou sans infection, dans certains cas sévère et prolongée et pouvant entraîner un décès. En cas de surdosage, un bilan hématologique est nécessaire. Des soins intensifs doivent être mis en place si nécessaire.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique: AGENTS ANTINEOPLASIQUES - AUTRES AGENTS ALKYLANTS, Code ATC: L01AX03
Le TMZ est un dérivé triazène, qui subit une conversion chimique rapide à pH physiologique en monométhyl triazenoimidazole carboxamide (MTIC) actif. La cytotoxicité du MTIC est vraisemblablement due principalement à une alkylation de la guanine en position O6 et à une alkylation supplémentaire en position N7. Les lésions cytotoxiques qui sont développées par la suite sont supposées entraîner une réparation aberrante de l'ADN méthylé.
Glioblastome multiforme nouvellement diagnostiqué
Un total de 573 patients ont été randomisés pour recevoir soit TMZ + RT (n=287) soit RT seule (n=286). Les patients dans le bras TMZ + RT ont reçu TMZ concomitant (75 mg/m2) une fois par jour, en commençant le premier jour de la RT jusqu'au dernier jour de la RT, pendant 42 jours (avec un maximum de 49 jours). Ceci a été suivi de TMZ en monothérapie (150 - 200 mg/m2) les Jours 1 - 5 de chaque cycle de 28 jours jusqu'à 6 cycles, commençant 4 semaines après la fin de la RT. Les patients dans le bras contrôle ont reçu seulement de la RT. La prophylaxie de la pneumonie à Pneumocystis carinii (PPC) a été exigée pendant le traitement par RT et TMZ associés.
Le TMZ a été administré comme traitement d'entretien dans la phase de suivi chez 161 des 282 patients (57 %) dans le bras radiothérapie seule, et 62 des 277 patients (22 %) dans le bras TMZ + RT.
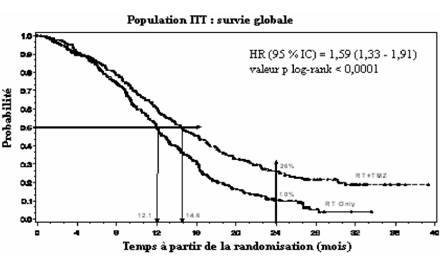
Le hazard ratio (HR) pour la survie globale était 1,59 (95 % IC pour HR = 1,33 - 1,91) avec un log-rank p < 0,0001 en faveur du bras TMZ. La probabilité estimée de survie à 2 ans ou plus (26 % vs 10 %) est plus importante pour le bras radiothérapie + TMZ. L'addition de TMZ de manière concomitante à la RT, suivie de TMZ en monothérapie dans le traitement des patients avec un glioblastome multiforme nouvellement diagnostiqué a démontré une amélioration de la survie globale (SG) statistiquement significative comparée à la RT seule (Figure 1).
Figure 1 Courbe de Kaplan-Meier pour la survie globale (population Intent-to-Treat)

Les résultats de l'étude n'étaient pas cohérents dans le sous-groupe de patients avec un faible « performance status » (OMS, PS=2, n=70), où la survie globale et le temps de progression étaient similaires dans les deux bras. Cependant, aucun risque inacceptable ne semble avoir été décelé dans ce groupe de patients.
Gliome malin en progression ou récidive
Les données d'efficacité clinique chez les patients atteints de glioblastome multiforme (indice de performance Karnofsky [IPK] ≥ 70), en progression ou récidivant après une chirurgie et une radiothérapie, proviennent de deux essais cliniques avec TMZ par voie orale. L'un était un essai non comparatif chez 138 patients (29 % avaient reçu une chimiothérapie préalable), et l'autre était un essai randomisé contrôlé contre référence active comparant TMZ vs procarbazine chez un total de 225 patients (67 % avaient reçu une chimiothérapie préalable à base de nitrosourée). Dans les deux essais, le critère d'évaluation principal était la survie sans progression (SSP) définie par Imagerie de Résonnance Médicale (IRM) ou une aggravation neurologique. Dans l'essai non comparatif, la SSP à 6 mois était de 19 %, la survie médiane sans progression était de 2,1 mois, et la survie médiane globale de 5,4 mois. Le taux de réponse objective (TRO) défini par des IRM était de 8 %.
Dans l'essai randomisé contrôlé contre référence active, la SSP à 6 mois était significativement plus importante pour le TMZ que pour la procarbazine (21 % versus 8 %, respectivement - Chi2: p = 0,008) avec une SSP moyenne de 2,89 et 1,88 mois respectivement (log rank p = 0,0063). La survie médiane était de 7,34 et 5,66 mois respectivement pour le TMZ et la procarbazine (log rank p = 0,33). A 6 mois, le pourcentage des patients survivants était significativement plus élevé dans le bras TMZ (60 %) comparé au bras procarbazine (44 %) (Chi2: p = 0,019). Chez les patients préalablement traités par chimiothérapie un bénéfice a été noté pour ceux ayant un IPK ≥ 80.
Les données sur la durée jusqu'à aggravation de l'état neurologique comme celles sur la durée jusqu'à aggravation de l'indice de performance (Diminution jusqu'à un IPK < 70 ou diminution d'au moins 30 points) étaient en faveur du TMZ par rapport à la procarbazine. Les temps médians jusqu'à progression pour ces critères d'évaluation sont plus longs pour le TMZ que pour la procarbazine, entre 0,7 et 2,1 mois (log rank p = < 0,01 à 0,03).
Astrocytome anaplasique en récidive
Lors d'un essai de phase II prospectif, multicentrique évaluant la sécurité et l'efficacité du TMZ oral dans le traitement des patients atteints d'astrocytome anaplasique en première rechute, la SSP à 6 mois était de 46 %. La médiane de la SSP était de 5,4 mois. La médiane de la survie globale était de 14,6 mois. Le taux de réponse, basé sur une revue centralisée, était de 35 % (13 RC et 43 RP) sur la population en intention de traiter (ITT) n=162. Chez 43 patients la stabilité de la maladie a été rapportée. La survie sans évènement à 6 mois pour la population en intention de traiter était de 44 % avec une médiane de survie sans évènement de 4,6 mois, ce qui était identique aux résultats de survie sans progression. Pour la population histologiquement éligible, les résultats d'efficacité étaient identiques. L'obtention d'une réponse radiologique objective ou le maintien d'une stabilisation sans progression était fortement associé à une qualité de vie maintenue ou améliorée.
Enfants
TMZ oral a été étudié chez les enfants (3-18 ans) atteints d'un gliome du tronc cérébral en récidive ou d'un astrocytome de haut Grade en récidive, administré quotidiennement pendant 5 jours tous les 28 jours. La tolérance au TMZ était similaire à celle de l'adulte.
5.2. Propriétés pharmacocinétiques
Le TMZ est spontanément hydrolysé au pH physiologique, principalement en ses métabolites actifs, 3-méthyl-(triazen-1-yl) imidazole-4-carboxamide (MTIC). Le MTIC est spontanément hydrolysé en 5-amino-imidazole-4-carboxamide (AIC), un intermédiaire connu dans la biosynthèse de la purine et de l'acide nucléique, et en méthylhydrazine, métabolite actif alkylant supposé. Il semble que la cytotoxicité du MTIC soit principalement due à l'alkylation de l'ADN essentiellement aux positions O6 et N7 de la guanine. Concernant l'ASC du TMZ, l'exposition aux MTIC et AIC est ~ 2,4 % et 23 %, respectivement. In vivo, le t1/2 du MTIC était similaire à celui du TMZ, 1,8 heures.
Absorption
Après administration orale chez l'adulte, le TMZ est rapidement absorbé avec des pics de concentration observés parfois dès 20 minutes après administration (temps moyens compris entre 0,5 et 1,5 heures). Après administration orale de TMZ marqué au 14C, l'excrétion fécale moyenne de 14C dans les 7 jours suivant l'administration était de 0,8 % signe d'une absorption complète.
Distribution
Le TMZ est faiblement lié aux protéines plasmatiques (10 à 20 %), et par conséquent, est peu susceptible d'interagir avec des produits très fortement liés aux protéines.
Les études cliniques utilisant la technique de TEP (Tomographie par Emission de Positrons) et les données précliniques suggèrent que le TMZ traverse rapidement la barrière hémato-encéphalique et se retrouve dans le liquide céphalo-rachidien (LCR). La pénétration dans le LCR a été confirmée chez un patient; sur la base de l'ASC du TMZ l'exposition du LCR était approximativement 30 % de celle du plasma, ce qui est cohérent avec les données chez l'animal.
Elimination
La demi-vie plasmatique (t1/2) est approximativement de 1,8 heures. La voie principale d'élimination du 14C est la voie rénale. Après administration orale, environ 5 à 10 % de la dose sont retrouvés sous forme inchangée dans les urines dans les 24 heures, et le reste est excrété sous forme d'acide témozolomide, de 5-aminoimidazole-4-carboxamide (AIC) ou de métabolites polaires non identifiés.
L'augmentation des concentrations plasmatiques est dose-dépendante. La clairance plasmatique, le volume de distribution et la demi-vie sont indépendants de la dose.
Populations spéciales
L'analyse des paramètres pharmacocinétiques de population du TMZ a montré que la clairance du TMZ est indépendante de l'âge, de la fonction rénale ou de la consommation de tabac. Dans une autre étude pharmacocinétique, les profils pharmacocinétiques des patients atteints de dysfonctionnement hépatique faible à modéré étaient identiques à ceux observés chez les patients dont la fonction hépatique était normale.
Les enfants présentent une ASC plus élevée que les adultes; cependant, la dose maximale tolérée (DMT) est de 1 000 mg/m2 par cycle de traitement à la fois chez l'enfant et chez l'adulte.
5.3. Données de sécurité préclinique
Des études de toxicité à cycle unique (5 jours de traitement, 23 jours sans traitement), à 3 et 6 cycles ont été réalisées chez le rat et le chien. Les principales cibles de la toxicité ont été la moelle osseuse, le système lymphoréticulaire, les testicules, le tractus gastro-intestinal et, pour des doses plus fortes, létales chez 60 % à 100 % des rats et des chiens testés, une dégénérescence rétinienne est survenue. La plupart des phénomènes toxiques ont été réversibles, à l'exception des effets secondaires sur le système de reproduction mâle et de la dégénérescence rétinienne. Cependant, comme les doses impliquées dans cette dégénérescence appartiennent à l'intervalle de doses létales, et qu'aucun effet semblable n'a été observé lors des études cliniques, ce résultat n'a pas de signification clinique.
Le TMZ est un agent alkylant embryotoxique, tératogène et génotoxique. Le TMZ est plus toxique chez le rat et le chien que chez l'homme, et la dose thérapeutique est proche de la dose létale minimale chez le rat et le chien. Les diminutions dose-dépendantes du nombre des leucocytes et des plaquettes apparaissent comme des indicateurs sensibles de la toxicité. Différents types de néoplasmes ont été observés lors de l'étude de toxicité après 6 cycles de traitement chez le rat, dont carcinome mammaire, kérato-acanthome cutané et adénome baso-cellulaire alors qu'aucune tumeur, ni aucun changement prénéoplasique n'a été observé au cours des études chez le chien. Le rat semble être particulièrement sensible aux effets oncogènes du TMZ, avec l'apparition des premières tumeurs dans les 3 mois suivant le début du traitement. La période de latence est très courte, même pour un agent alkylant.
Les résultats des tests d'Ames/salmonella et d'aberration chromosomique sur lymphocyte humain démontrent l'existence d'un potentiel mutagène.
Contenu de la gélule: lactose anhydre, carboxyméthylamidon sodique type A, silice colloïdale anhydre, acide tartrique, acide stéarique.
Enveloppe de la gélule: gélatine, dioxyde de titane (E171).
Encre d'impression: laque, propylène glycol, dioxyde de titane (E171), oxyde de fer jaune (E172), laque aluminique indigo carmin (E132).
Sans objet.
3 ans.
Après ouverture, le médicament doit être utilisé dans les 21 jours.
Présentation en sachet-dose
3 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas + 30°C. A conserver dans lemballage extérieur dorigine à labri de la lumière. Conserver le flacon soigneusement fermé à labri de lhumidité.
Présentation en sachet-dose
A conserver à une température ne dépassant pas + 30°C. A conserver dans lemballage extérieur dorigine à labri de la lumière.
6.5. Nature et contenu de l'emballage extérieur
5 ou 20 gélules en flacons de verre teinté munis de bouchon sécurité-enfant en polypropylène blanc avec un sellage dinduction en polyéthylène. Létui contient un flacon.
Présentation en sachet-dose
Les sachets-dose se composent de polyéthylène, daluminium et de polyéthylène téréphtalate.
Chaque sachet-dose contient une gélule et est dispensé dans un étui en carton.
Létui contient 5 ou 20 gélules, individuellement scellées dans des sachets-dose.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières délimination et de manipulation
Les gélules ne doivent pas être ouvertes. Lorsqu'une gélule est détériorée, tout contact entre la poudre et la peau ou les muqueuses doit être évité. En cas de contact de TEMOZOLOMIDE MYLAN avec la peau ou les muqueuses, laver immédiatement et abondamment à l'eau et au savon.
Les patients devront être avertis de tenir les gélules hors de la portée et de la vue des enfants, de préférence dans un endroit fermé à clé. L'ingestion accidentelle peut être mortelle pour les enfants.
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Le personnel enceinte ne doivent pas manipuler ce produit.
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
MYLAN S.A.S.
117 ALLEE DES PARCS
69800 SAINT-PRIEST
FRANCE
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 577 103-8 ou 34009 577 103 8 5: 5 gélules en flacon (verre teinté).
· 577 104-4 ou 34009 577 104 4 6: 20 gélules en flacon (verre teinté).
· 269 958-2 ou 34009 269 958 2 9 : 5 gélules en sachet-dose.
· 269 959-9 ou 34009 269 959 9 7 : 20 gélules en sachet-dose.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste I.
Médicament soumis à prescription hospitalière. Prescription réservée aux spécialistes en oncologie ou en hématologie ou aux médecins compétents en cancérologie. Médicament nécessitant une surveillance particulière pendant le traitement.