RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 24/12/2015
TRIAFEMI, comprimé
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Norgestimate ................................................................................................................................ 0,180 mg
Ethinylestradiol ............................................................................................................................. 0,035 mg
Pour un comprimé blanc.
Norgestimate ................................................................................................................................ 0,215 mg
Ethinylestradiol ............................................................................................................................. 0,035 mg
Pour un comprimé bleu ciel.
Norgestimate ................................................................................................................................ 0,250 mg
Ethinylestradiol ............................................................................................................................. 0,035 mg
Pour un comprimé bleu foncé.
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé.
7 comprimés blancs, 7 comprimés bleu ciel, 7 comprimés bleu foncé.
4.1. Indications thérapeutiques
La décision de prescrire TRIAFEMI doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thrombo-embolie veineuse (TEV), ainsi que du risque de TEV associé à TRIAFEMI en comparaison aux autres CHC (Contraceptifs Hormonaux Combinés) (voir rubriques 4.3 et 4.4).
4.2. Posologie et mode d'administration
Prendre régulièrement et sans oubli 1 comprimé par jour au même moment de la journée, pendant 21 jours consécutifs, avec un arrêt de 7 jours entre chaque plaquette.
Début du traitement de l'acné et de la contraception orale
1er comprimé à prendre le 1er jour des règles.
Relais d'un autre estroprogestatif:
1er comprimé: après un arrêt de 7 jours si la précédente plaquette contenait 21 comprimés (6 jours si elle en contenait 22 et sans intervalle si elle en contenait 28).
En cas d'absence d'hémorragie de privation pendant les 6 ou 7 jours qui suivent l'arrêt de la pilule précédente s'assurer de l'absence de grossesse avant de commencer le traitement.
Le traitement devra être poursuivi plusieurs mois; les premiers signes d'amélioration clinique de l'acné se manifestent au bout de 2 mois, parfois plus.
|
Cas d'oubli d'un ou de plusieurs comprimés |
L'oubli d'un comprimé expose à un risque de grossesse.
Si l'oubli est constaté dans les 12 heures qui suivent l'heure habituelle de la prise, prendre immédiatement le comprimé oublié, et poursuivre le traitement normalement en prenant le comprimé suivant à l'heure habituelle.
Si l'oubli est constaté plus de 12 heures après l'heure normale de la prise, la sécurité contraceptive n'est plus assurée. Prendre immédiatement le dernier comprimé oublié et poursuivre le traitement contraceptif oral jusqu'à la fin de la plaquette, en utilisant simultanément une méthode contraceptive de type mécanique (préservatifs, spermicides...) jusqu'à la reprise de la plaquette suivante, y compris pendant les règles.
Les contraceptifs hormonaux combinés (CHC) ne doivent pas être utilisés dans les situations suivantes.
En cas de survenue pour la première fois de l'une de ces pathologies lors de la prise d'une contraception orale, interrompre immédiatement le traitement.
· Hypersensibilité aux substances actives ou à l'un des excipients.
· Présence ou risque de thrombo-embolie veineuse (TEV) :
o Thrombo-embolie veineuse présence de TEV (patient traité par des anticoagulants) ou antécédents de TEV (p. ex. thrombose veineuse profonde [TVP] ou embolie pulmonaire [EP]) ;
o Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie veineuse, telle quune résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S ;
o Intervention chirurgicale majeure avec immobilisation prolongée (voir rubrique 4.4) ;
o Risque élevé de thrombo-embolie veineuse dû à la présence de multiples facteurs de risque (voir rubrique 4.4).
· Présence ou risque de thrombo-embolie artérielle (TEA) :
o Thrombo-embolie artérielle présence ou antécédents de thrombo-embolie artérielle (p. ex. infarctus du myocarde [IM]) ou de prodromes (p. ex. angine de poitrine) ;
o Affection cérébrovasculaire présence ou antécédents daccident vasculaire cérébral (AVC) ou de prodromes (p. ex. accident ischémique transitoire [AIT]) ;
o Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie artérielle, telle quune hyperhomocystéinémie ou la présence danticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique) ;
o Antécédents de migraine avec signes neurologiques focaux ;
o Risque élevé de thrombo-embolie artérielle dû à la présence de multiples facteurs de risque (voir rubrique 4.4) ou dun facteur de risque sévère tel que :
§ diabète avec symptômes vasculaires,
§ hypertension artérielle sévère,
§ dyslipoprotéinémie sévère.
· Tumeurs malignes du sein et de l'utérus.
· Affections hépatiques sévères ou récentes.
· Tumeurs hypophysaires.
· Hémorragies génitales non diagnostiquées.
· Connectivites.
· Porphyries.
· En association avec le millepertuis.
Ce médicament est généralement déconseillé dans les situations suivantes :
· Tabagisme.
· Affections métaboliques: diabète non compliqué, hyperlipidémies (hypertriglycéridémie, hypercholestérolémie).
· Obésité (indice de masse corporelle = Poids/ Taille2 > 30 kg/m2).
· Otosclérose.
· Tumeurs bénignes du sein et dystrophies utérines (hyperplasie, fibrome).
· Hyperprolactinémie avec ou sans galactorrhée.
· Insuffisance rénale.
· Cholestase récurrente ou prurit récidivant lors d'une grossesse antérieure.
· Herpès gestationis.
· En association avec les inducteurs enzymatiques (voir rubrique 4.5).
· Allaitement (voir rubrique 4.6).
4.4. Mises en garde spéciales et précautions d'emploi
Si la patiente présente lun des troubles ou lun des facteurs de risque mentionnés ci-dessous, la pertinence du traitement par TRIAFEMI doit être discutée avec elle.
En cas daggravation ou de survenue de lun de ces troubles ou facteurs de risque, la nécessité dinterrompre lutilisation de TRIAFEMI doit être discutée entre le médecin et la patiente.
· Troubles circulatoires
Risque de thrombo-embolie veineuse (TEV)
Le risque de TEV est augmenté chez les femmes qui utilisent un contraceptif hormonal combiné (CHC) en comparaison aux femmes qui nen utilisent pas. Les CHC contenant du lévonorgestrel, du norgestimate (incluant TRIAFEMI) ou de la noréthistérone sont associés au risque de TEV le plus faible. La décision dutiliser TRIAFEMI doit être prise uniquement après concertation avec la patiente afin de sassurer quelle comprend le risque de TEV associé à TRIAFEMI linfluence de ses facteurs de risque actuels sur ce risque et le fait que le risque de TEV est maximal pendant la première année dutilisation. Certaines données indiquent également une augmentation du risque lors de la reprise dun CHC après une interruption de 4 semaines ou plus.
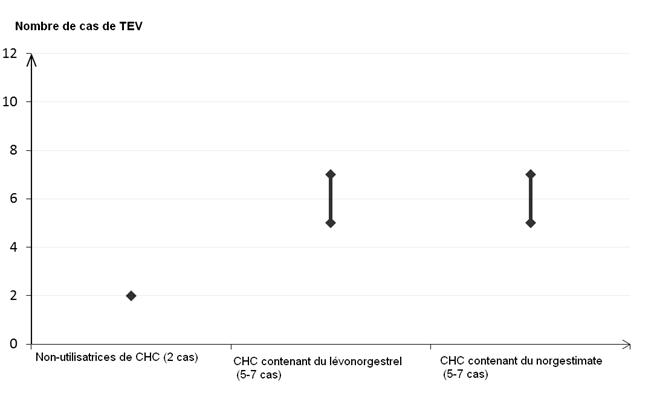
Parmi les femmes qui nutilisent pas de CHC et qui ne sont pas enceintes, environ 2 sur 10 000 développeront une TEV sur une période dun an. Cependant, chez une femme donnée, le risque peut être considérablement plus élevé, selon les facteurs de risque quelle présente (voir ci-dessous).
On estime que sur 10 000 femmes qui utilisent un CHC contenant du lévonorgestrel, environ 61 développeront une TEV sur une période dun an.
Les données disponibles à ce jour suggèrent que le risque de TEV associé à lutilisation de CHC contenant du norgestimate est similaire à celui associé à lutilisation de CHC contenant du lévonorgestrel.
Ce nombre de TEV par année est inférieur à celui attendu pendant la grossesse ou en période post-partum.
La TEV peut être fatale dans 1 à 2 % des cas.
1. Point central de lintervalle de 5‑7 pour 10 000 années-femmes sur la base dun risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non-utilisation dun CHC, denviron 2,3 à 3,6
Nombre de cas de TEV pour 10 000 femmes sur une période dun an
De façon extrêmement rare, des cas de thrombose ont été signalés chez des utilisatrices de CHC dans dautres vaisseaux sanguins, p. ex. les veines et artères hépatiques, mésentériques, rénales ou rétiniennes.
Facteurs de risque de TEV
Le risque de complications thrombo-emboliques veineuses chez les utilisatrices de CHC peut être considérablement accru si dautres facteurs de risque sont présents, en particulier si ceux-ci sont multiples (voir le tableau ci-dessous).
TRIAFEMI est contre-indiqué chez les femmes présentant de multiples facteurs de risque, ceux-ci les exposant à un risque élevé de thrombose veineuse (voir rubrique 4.3). Lorsquune femme présente plus dun facteur de risque, il est possible que laugmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement dans ce cas, le risque global de TEV doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique 4.3).
Tableau : Facteurs de risque de TEV
|
Facteur de risque |
Commentaire |
|
Obésité (indice de masse corporelle supérieur à 30 kg/m²). |
Lélévation de lIMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte si dautres facteurs de risque sont présents. |
|
Immobilisation prolongée, intervention chirurgicale majeure, toute intervention chirurgicale sur les jambes ou le bassin, neurochirurgie ou traumatisme majeur.
Remarque : limmobilisation temporaire, y compris les trajets aériens > 4 heures, peut également constituer un facteur de risque de TEV, en particulier chez les femmes présentant dautres facteurs de risque. |
Dans ces situations, il est conseillé de suspendre lutilisation de la pilule (au moins quatre semaines à lavance en cas de chirurgie programmée) et de ne reprendre le CHC que deux semaines au moins après la complète remobilisation. Une autre méthode de contraception doit être utilisée afin déviter une grossesse non désirée. Un traitement anti-thrombotique devra être envisagé si TRIAFEMI na pas été interrompu à lavance.
|
|
Antécédents familiaux (thrombo-embolie veineuse survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans). |
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant lutilisation de CHC. |
|
Autres affections médicales associées à la TEV. |
Cancer, lupus érythémateux disséminé, syndrome hémolytique et urémique, maladies inflammatoires chroniques intestinales (maladie de Crohn ou rectocolite hémorragique) et drépanocytose. |
|
Âge. |
En particulier au-delà de 35 ans. |
Il nexiste aucun consensus quant au rôle éventuel joué par les varices et les thrombophlébites superficielles dans lapparition ou la progression dune thrombose veineuse.
Laugmentation du risque de thrombo-embolie pendant la grossesse, et en particulier pendant les 6 semaines de la période puerpérale, doit être prise en compte (pour des informations concernant « Grossesse et allaitement », voir rubrique 4.6).
Symptômes de TEV (thrombose veineuse profonde et embolie pulmonaire)
Les femmes doivent être informées quen cas dapparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer quelles utilisent un CHC. Les symptômes de la thrombose veineuse profonde (TVP) peuvent inclure :
· gonflement unilatéral dune jambe et/ou dun pied ou le long dune veine de la jambe ;
· douleur ou sensibilité dans une jambe, pouvant nêtre ressentie quen position debout ou lors de la marche ;
· sensation de chaleur, rougeur ou changement de la coloration cutanée de la jambe affectée.
Les symptômes de lembolie pulmonaire (EP) peuvent inclure :
· apparition soudaine et inexpliquée dun essoufflement ou dune accélération de la respiration ;
· toux soudaine, pouvant être associée à une hémoptysie ;
· douleur thoracique aiguë ;
· étourdissements ou sensations vertigineuses sévères ;
· battements cardiaques rapides ou irréguliers.
Certains de ces symptômes (p. ex. « essoufflement », « toux ») ne sont pas spécifiques et peuvent être interprétés à tort comme des signes dévénements plus fréquents ou moins sévères (infections respiratoires, p. ex.).
Les autres signes dune occlusion vasculaire peuvent inclure : douleur soudaine, gonflement et coloration légèrement bleutée dune extrémité.
Si locclusion se produit dans lil, les symptômes peuvent débuter sous la forme dune vision trouble indolore pouvant évoluer vers une perte de la vision. Dans certains cas, la perte de la vision peut survenir presque immédiatement.
Risque de thrombo-embolie artérielle (TEA)
Des études épidémiologiques ont montré une association entre lutilisation de CHC et laugmentation du risque de thrombo-embolie artérielle (infarctus du myocarde) ou daccident cérébrovasculaire (p. ex. accident ischémique transitoire, AVC). Les événements thrombo-emboliques artériels peuvent être fatals.
Facteurs de risque de TEA
Le risque de complications thrombo-emboliques artérielles ou daccident cérébrovasculaire chez les utilisatrices de CHC augmente avec la présence de facteurs de risque (voir le tableau). TRIAFEMI est contre-indiqué chez les femmes présentant un facteur de risque sévère ou de multiples facteurs de risque de TEA qui les exposent à un risque élevé de thrombose artérielle (voir rubrique 4.3).
Lorsquune femme présente plus dun facteur de risque, il est possible que laugmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement dans ce cas, le risque global doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique 4.3).
Tableau : Facteurs de risque de TEA
|
Facteur de risque |
Commentaire |
|
Âge |
En particulier au-delà de 35 ans |
|
Tabagisme |
Il doit être conseillé aux femmes de ne pas fumer si elles souhaitent utiliser un CHC. Il doit être fortement conseillé aux femmes de plus de 35 ans qui continuent de fumer dutiliser une méthode de contraception différente. |
|
Hypertension artérielle |
|
|
Obésité (indice de masse corporelle supérieur à 30 kg/m2) |
Lélévation de lIMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte chez les femmes présentant dautres facteurs de risque. |
|
Antécédents familiaux (thrombo-embolie artérielle survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans) |
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant lutilisation de CHC. |
|
Migraine |
Laccroissement de la fréquence ou de la sévérité des migraines lors de lutilisation dun CHC (qui peut être le prodrome dun événement cérébrovasculaire) peut constituer un motif darrêt immédiat du CHC. |
|
Autres affections médicales associées à des événements indésirables vasculaires |
Diabète, hyperhomocystéinémie, valvulopathie cardiaque et fibrillation auriculaire, dyslipoprotéinémie et lupus érythémateux disséminé |
Symptômes de TEA
Les femmes doivent être informées quen cas dapparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer quelles utilisent un CHC.
Les symptômes dun accident cérébrovasculaire peuvent inclure :
· apparition soudaine dun engourdissement ou dune faiblesse du visage, dun bras ou dune jambe, en particulier dun côté du corps ;
· apparition soudaine de difficultés à marcher, de sensations vertigineuses, dune perte déquilibre ou de coordination ;
· apparition soudaine dune confusion, de difficultés à parler ou à comprendre ;
· apparition soudaine de difficultés à voir dun il ou des deux yeux ;
· céphalée soudaine, sévère ou prolongée, sans cause connue ;
· perte de conscience ou évanouissement avec ou sans crise convulsive.
Des symptômes temporaires suggèrent quil sagit dun accident ischémique transitoire (AIT).
Les symptômes de linfarctus du myocarde (IM) peuvent inclure :
· douleur, gêne, pression, lourdeur, sensation doppression ou dencombrement dans la poitrine, le bras ou sous le sternum ;
· sensation de gêne irradiant vers le dos, la mâchoire, la gorge, le bras, lestomac ;
· sensation dencombrement, dindigestion ou de suffocation ;
· transpiration, nausées, vomissements ou sensations vertigineuses ;
· faiblesse, anxiété ou essoufflement extrêmes ;
· battements cardiaques rapides ou irréguliers.
· Cancers gynécologiques
· Une méta-analyse regroupant les données de 54 études internationales a mis en évidence une légère augmentation du risque de cancer du sein chez les utilisatrices de contraceptifs oraux. L'augmentation du risque ne semble pas dépendante de la durée d'utilisation ni de l'existence de facteurs de risque tels que la nulliparité et les antécédents familiaux de cancer du sein. Cette augmentation est transitoire et disparaît 10 ans après l'arrêt de son utilisation. La surveillance clinique plus régulière des femmes sous contraceptif oral, permettant un diagnostic plus précoce, pourrait jouer un rôle important dans l'augmentation du nombre de cancers du sein diagnostiqué. Les données publiées ne sont pas de nature à remettre en cause l'utilisation des contraceptifs oraux dont les bénéfices sont nettement supérieurs aux risques éventuels.
· Par ailleurs, la contraception orale diminue le risque de cancer de l'ovaire et de l'utérus (endomètre).
· Consultation/examen médical
Avant linstauration ou la reprise dun traitement par TRIAFEMI une recherche complète des antécédents médicaux (y compris les antécédents familiaux) doit être effectuée et la présence dune grossesse doit être exclue. La pression artérielle doit être mesurée et un examen physique doit être réalisé, en ayant à lesprit les contre-indications (voir rubrique 4.3) et les mises en garde (voir rubrique 4.4). Il est important dattirer lattention des patientes sur les informations relatives à la thrombose veineuse et artérielle, y compris le risque associé à TRIAFEMI comparé à celui associé aux autres CHC, les symptômes de la TEV et de la TEA, les facteurs de risque connus et la conduite à tenir en cas de suspicion de thrombose.
Il doit également être indiqué aux patientes de lire attentivement la notice et de suivre les conseils fournis. La fréquence et la nature des examens doivent être définies sur la base des recommandations en vigueur et adaptées à chaque patiente.
Les patientes doivent être averties que les contraceptifs hormonaux ne protègent pas contre linfection par le VIH (SIDA) et les autres maladies sexuellement transmissibles.
Précautions d'emploi
· Une surveillance attentive doit être exercée chez les patientes présentant: épilepsie, migraine, asthme, antécédents vasculaires artériels familiaux et varices.
· La survenue de troubles digestifs intercurrents dans les 4 heures suivant la prise, tels que vomissements ou diarrhée sévère peut entraîner une inefficacité transitoire de la méthode imposer la conduite à tenir préconisée en cas d'oubli de moins de 12 heures. Si ces épisodes se répètent sur plusieurs jours, il est alors nécessaire d'associer une autre méthode contraceptive, en particulier de type mécanique (préservatif masculin, spermicides...) jusqu'à la reprise de la plaquette suivante.
· Des métrorragies et des spottings peuvent apparaître, plus particulièrement pendant les premiers mois d'utilisation. Ils cessent en général spontanément et il n'y a pas lieu d'interrompre le traitement. Si ces saignements persistent ou apparaissent pour la première fois après une utilisation prolongée, la recherche d'une éventuelle cause organique s'impose.
· En cas de chloasma apparu lors d'une grossesse, il est recommandé d'éviter les expositions solaires.
Ce médicament contient du lactose. Son utilisation est déconseillée chez les patients présentant une intolérance au galactose, un déficit en lactase de Lapp ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les interactions entre les contraceptifs estro-progestatifs et d'autres substances peuvent conduire à une augmentation ou une diminution des concentrations plasmatiques destro-progestatifs.
La diminution des concentrations plasmatiques destro-progestatifs peut provoquer une augmentation de l'incidence des saignements intermenstruels et éventuellement réduire l'efficacité du contraceptif estro-progestatif.
Associations contre-indiquées
+ Millepertuis
Diminution des concentrations plasmatiques du contraceptif hormonal, en raison de leffet inducteur enzymatique du millepertuis, avec risque de baisse defficacité voire dannulation de leffet dont les conséquences peuvent être éventuellement graves (survenue dune grossesse).
Associations déconseillées
+ Inducteurs enzymatiques
Anticonvulsivants (phénobarbital, phénytoïne, fosphénytoïne, primidone, carbamazépine, oxcarbazépine), rifabutine, rifampicine, efavirenz, névirapine.
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par linducteur.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique, pendant la durée de lassociation et un cycle suivant.
+ Lamotrigine (voir aussi ci-dessous Association nécessitant des précautions demploi)
Risque de diminution des concentrations et de l'efficacité de la lamotrigine par augmentation de son métabolisme hépatique.
Eviter de mettre en route une contraception orale pendant la période dajustement posologique de la lamotrigine.
+ Modafinil
Risque de diminution de l'efficacité contraceptive, pendant le traitement et un cycle après l'arrêt du traitement par le modafinil, en raison de son potentiel inducteur enzymatique.
Utiliser des contraceptifs oraux normodosés ou une autre méthode contraceptive.
+ Nelfinavir
Risque de diminution de lefficacité contraceptive par diminution des concentrations en contraceptif hormonal.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique (préservatif ou stérilet), pendant la durée de lassociation et un cycle suivant.
+ Inhibiteurs de protéases boostés par ritonavir
Risque de diminution de l'efficacité contraceptive par diminution des concentrations en contraceptif hormonal due à laugmentation de son métabolisme hépatique par le ritonavir.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique (préservatif ou stérilet), pendant la durée de lassociation et un cycle suivant.
+ Topiramate
Pour des doses de topiramate supérieures ou égales à 200 mg/jour : risque de diminution de lefficacité contraceptive par diminution des concentrations en estrogène.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique.
+ Vémurafénib
Risque de diminution des concentrations des estroprogestatifs, avec pour conséquence un risque dinefficacité.
+ Pérampanel
Pour des doses de pérampanel ≥ 12 mg/j : risque de diminution de lefficacité contraceptive.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique.
Associations nécessitant des précautions demploi
+ Bosentan
Risque de diminution de lefficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal.
Utiliser une méthode contraceptive fiable, additionnelle ou alternative, pendant la durée de lassociation et un cycle suivant.
+ Griséofulvine
Risque de diminution de lefficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique, pendant la durée de lassociation et un cycle suivant.
+ Lamotrigine
Risque de diminution des concentrations et de lefficacité de la lamotrigine par augmentation de son métabolisme hépatique.
Surveillance clinique et adaptation de la posologie de la lamotrigine lors de la mise en route dune contraception orale et après son arrêt.
Diminution modérée des concentrations déthinylestradiol. Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique.
Associations à prendre en compte
+ Etoricoxib
Augmentation des concentrations déthinylestradiol par létoricoxib.
Ce médicament n'est pas indiqué pendant la grossesse.
En clinique, à la différence du diéthylstilbestrol, les résultats de nombreuses études épidémiologiques permettent d'écarter, à ce jour, un risque malformatif des estrogènes seuls ou en association en début de grossesse.
Par ailleurs, les risques portant sur la différenciation sexuelle du ftus (en particulier féminin), risques décrits avec d'anciens progestatifs très androgénomimétiques, n'ont pas lieu d'être extrapolés aux progestatifs récents comme celui présenté dans cette spécialité, nettement moins voire pas du tout androgénomimétiques.
En conséquence, la découverte d'une grossesse sous estroprogestatifs n'en justifie pas l'interruption.
Laugmentation du risque de TEV en période post-partum doit être prise en compte lors de la reprise de TRIAFEMI, comprimé (voir rubriques 4.2 et 4.4).
Allaitement
En cas d'allaitement, l'utilisation de ce médicament est déconseillée en raison du passage des estroprogestatifs dans le lait maternel.
Si la femme désire allaiter, un autre moyen de contraception doit être proposé.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Il n'a pas été observé d'effet sur l'aptitude à conduire ou à utiliser des machines.
Description de certains effets indésirables particuliers
Une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant linfarctus du myocarde, lAVC, les accidents ischémiques transitoires, la thrombose veineuse et lembolie pulmonaire, a été observée chez les femmes utilisant des CHC ; ceci est abordé plus en détails en rubrique 4.4.
Effets indésirables rares mais devant faire interrompre le traitement :
· accidents thrombo-emboliques artériels (en particulier infarctus du myocarde, accident vasculaire cérébral) ;
· accidents thrombo-emboliques veineux (phlébite, embolie pulmonaire) ;
· hypertension artérielle, coronaropathies ;
· hyperlipidémies (hypertriglycéridémie et/ou hypercholestérolémie), diabète ;
· mastodynie sévère, mastopathie bénigne ;
· adénome hypophysaire à prolactine (éventuellement révélé par une galactorrhée) ;
· céphalées importantes et inhabituelles, migraines, vertiges, modification de la vision ;
· exacerbation d'une comitialité ;
· adénome hépatique, ictères cholestatiques ;
· chloasma.
Effets indésirables plus fréquents n'empêchant pas habituellement la poursuite du traitement :
· nausées, céphalées banales, prise de poids, irritabilité, jambes lourdes ;
· tension mammaire, saignements intermenstruels, oligoménorrhée, aménorrhée, modification de la libido ;
· irritation oculaire par les lentilles de contacts.
Rarement : séborrhée, hypertrichose.
Autres : lithiase biliaire: augmentation du risque (environ doublé chez les utilisatrices).
Effets à l'arrêt du traitement : aménorrhées post-thérapeutiques.
Des aménorrhées avec anovulation (survenant plus volontiers chez les femmes ayant des antécédents de cycles irréguliers) peuvent s'observer à l'arrêt du traitement. Elles cèdent en général spontanément. En cas de prolongation, avant toute nouvelle prescription, la recherche d'une éventuelle pathologie hypophysaire s'impose.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (Ansm) et réseau des Centres Régionaux de Pharmacovigilance Site internet : www.ansm.sante.fr.
Le surdosage peut se manifester par des signes digestifs (nausées, vomissements...) et des troubles du cycle.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
PROGESTATIFS ET ESTROGENES POUR ADMINISTRATION SEQUENTIELLE
Code ATC: G03B
Estroprogestatif combiné minidosé, triphasique.
Le norgestimate est un progestatif de 3ème génération appartenant à la classe thérapeutique des gonanes.
Cette combinaison estroprogestative agit par suppression des gonadotrophines. Bien que le mécanisme premier de cette action soit l'inhibition de l'ovulation, d'autres modifications ont lieu comme la modification de la glaire cervicale et de l'endomètre.
L'indice de Pearl de cet estroprogestatif (nombre de grossesses pour 100 années femmes) est de 0 à 0,77 (48 598 cycles). L'indice de Pearl tient compte de toutes les grossesses survenues au cours des études y compris chez les femmes n'ayant pas pris correctement les comprimés (oublis).
Cette association augmente le taux de SHBG (Sex Hormone Binding Globulin) et diminue celui de la testostérone libre à l'instar d'associations estroprogestatives comparables.
TRIAFEMI a été testé contre un placebo au cours de 2 études cliniques randomisées et en double aveugle chez des femmes présentant une acné légère à modérée. TRIAFEMI n'a pas été testé contre un autre traitement hormonal antiacnéique.
A partir de travaux in vitro sur des lignées cellulaires humaines transfectées exprimant le récepteur aux androgènes, les propriétés suivantes ont été démontrées mais n'ont pas fait l'objet d'études in vivo:
· le norgestimate et le déacetyl-norgestimate présentent une inhibition compétitive avec les androgènes pour la liaison au récepteur (sur des cellules PALM de cancer prostatique: PC3 Androgen Luciferase MMTV);
· le norgestimate et le déacetyl-norgestimate réduisent le transfert cyto-nucléaire des complexes androgènes-récepteur des androgènes (sur des cellules de mammifères COS7);
· le norgestimate et le déacetyl-norgestimate inhibent faiblement l'activité transcriptionnelle de la luciférase induite par les androgènes (sur des cellules humaines de cancer prostatique PALM) à faible concentration.
5.2. Propriétés pharmacocinétiques
Le norgestimate est actif par lui-même et par ses métabolites: le 17-déacétyl-norgestimate et le norgestrel. Il est rapidement absorbé et intensivement métabolisé. Le pic plasmatique du norgestimate est atteint en 1 heure, celui du 17-déacétyl-norgestimate en 2 heures. La demi-vie du 17-déacétyl-norgestimate est de 16-17 heures.
L'éthinylestradiol est rapidement absorbé. Le pic plasmatique est atteint en 1 à 2 heures. La demi-vie de l'éthinylestradiol est comprise entre 6 et 20 heures. L'éthinylestradiol est excrété dans les urines et les fèces sous forme inchangée et sous forme de métabolites.
5.3. Données de sécurité préclinique
Sans objet.
Comprimé blanc: lactose anhydre, amidon prégélatinisé, stéarate de magnésium.
Comprimé bleu ciel et bleu foncé: lactose anhydre, amidon prégélatinisé, stéarate de magnésium, laque aluminique d'indigotine.
Sans objet.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas +25°C.
6.5. Nature et contenu de l'emballage extérieur
21 comprimés (7 comprimés blancs, 7 comprimés bleu ciel, 7 comprimés bleu foncé) sous plaquette thermoformée (PVC/Aluminium); boîte de 1 ou 3 plaquettes.
6.6. Précautions particulières délimination et de manipulation
Pas d'exigences particulières
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
EFFIK
9/11, RUE JEANNE BRACONNIER
BATIMENT "LE NEWTON"
92366 MEUDON-LA-FORET
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 358 995-0: 21 comprimés sous plaquette thermoformée (PVC/Aluminium). Boîte de 1 plaquette.
· 358 996-7: 21 comprimés sous plaquette thermoformée (PVC/Aluminium). Boîte de 3 plaquettes.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste I.