RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 28/06/2016
1. DENOMINATION DU MEDICAMENT
NEXPLANON 68 mg, implant pour usage sous-cutané
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
NEXPLANON est un implant flexible, purement progestatif, non biodégradable, radio-opaque, préchargé dans un applicateur stérile, jetable.
Etonogestrel 68 mg
Pour un implant.
Le taux de libération de létonogestrel est approximativement de 60‑70 µg/jour en 5 à 6 semaines puis diminue pour atteindre approximativement 35‑45 µg/jour à la fin de la première année, environ 30‑40 µg/jour à la fin de la deuxième année et environ 25‑30 µg/jour à la fin de la troisième année. La conception de lapplicateur permet une utilisation avec une seule main et facilite une insertion sous-cutanée correcte de limplant.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Implant pour usage sous-cutané.
Bâtonnet flexible, souple, blanc à blanc cassé, non biodégradable, radio-opaque, de 4 cm de long et 2 mm de diamètre.
4. DONNEES CLINIQUES
4.1. Indications thérapeutiques
Contraception.
La sécurité et lefficacité ont été établies chez les femmes entre 18 et 40 ans.
4.2. Posologie et mode d'administration
Posologie
1 implant, qui peut être laissé en place pendant 3 ans.
Population pédiatrique
La sécurité et lefficacité de Nexplanon nont pas été étudiées chez les adolescentes de moins de 18 ans.
Mode dadministration
Toute grossesse doit être exclue avant linsertion de NEXPLANON.
Il est fortement recommandé que NEXPLANON soit inséré et retiré uniquement par des professionnels de santé ayant été formés à lutilisation de lapplicateur de NEXPLANON et aux techniques dinsertion et de retrait de limplant NEXPLANON et le cas échéant, quune supervision soit demandée lors de linsertion ou du retrait de limplant.
Des informations supplémentaires et des instructions plus détaillées concernant linsertion et le retrait de limplant seront envoyées gratuitement sur demande (MSD France, tél. 01.80.46.40.40).
Avant dinsérer limplant, lire et suivre attentivement les instructions pour l'insertion et le retrait de l'implant dans la rubrique 4.2. « Comment insérer NEXPLANON » et « Comment retirer NEXPLANON ».
Comment utiliser NEXPLANON
NEXPLANON est un contraceptif hormonal daction prolongée. Un seul implant est inséré en sous-cutané et il peut être laissé en place pendant trois ans. Ne pas retirer limplant plus de trois ans après la date dinsertion. Lutilisatrice doit être informée quelle peut demander le retrait de limplant à nimporte quel moment. Les professionnels de santé habilités à prescrire Nexplanon devront envisager de remplacer limplant plus tôt chez les femmes en surpoids (voir rubrique 4.4.). Après le retrait de limplant, linsertion immédiate dun autre implant assurera la continuité de la protection contraceptive. Si le souhait de la femme est de ne pas continuer avec NEXPLANON, une autre méthode contraceptive doit lui être conseillée pour éviter une grossesse.
La réussite de lutilisation et du retrait de NEXPLANON repose sur une insertion sous-cutanée de limplant réalisée correctement et avec précaution conformément aux instructions.
· Un implant inséré plus profondément quen sous-cutané (insertion profonde) peut ne pas être palpable et la localisation et/ou le retrait peuvent être difficiles (voir rubrique 4.2. « Comment retirer NEXPLANON » et rubrique 4.4.).
· Si limplant nest pas inséré conformément aux instructions, et pas le jour adapté, ceci peut entraîner une grossesse non désirée (voir rubrique 4.2. « Quand insérer NEXPLANON » et rubrique « Comment insérer NEXPLANON »).
Limplant NEXPLANON doit être inséré à la face interne du bras en sous-cutané, JUSTE SOUS LA PEAU EN EVITANT le sillon (gouttière) entre le biceps et le triceps où les principaux vaisseaux sanguins et nerfs se trouvent dans le faisceau neurovasculaire, plus en profondeur dans le tissu sous-cutané,.
Immédiatement après linsertion, la présence de limplant doit être vérifiée par palpation. Si limplant ne peut pas être palpé ou sil y a un doute sur sa présence, voir rubrique 4.2. « Comment insérer NEXPLANON », sous-rubrique « Si limplant nest pas palpable ».
Létui de NEXPLANON contient une Carte Patiente destinée à la patiente mentionnant le numéro de lot de l'implant. Il est demandé au professionnel de santé effectuant l'insertion de noter la date d'insertion, le bras où l'implant est inséré et le jour prévu du retrait sur la Carte Patiente. Létui comprend également des étiquettes adhésives destinées au dossier médical mentionnant le numéro de lot et la date d'insertion.
Quand insérer NEXPLANON
IMPORTANT : Exclure toute grossesse avant linsertion de limplant.
Le moment choisi pour linsertion dépend de la situation contraceptive récente de la femme, comme suit :
Absence préalable de contraception hormonale utilisée au cours du mois précédent
Limplant doit être inséré entre le 1er jour (premier jour des menstruations) et le 5ème jour du cycle menstruel, même si la femme saigne toujours.
Si linsertion a lieu au moment recommandé, une contraception complémentaire n'est pas nécessaire. Si linsertion a lieu à un autre moment que celui recommandé pour linsertion, la patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
Passage dune méthode contraceptive hormonale à NEXPLANON
Relais dun contraceptif hormonal combiné (ex : contraceptif oral combiné (COC), anneau vaginal ou patch transdermique)
Limplant doit être inséré de préférence le lendemain de la prise du dernier comprimé actif (le dernier comprimé contenant les substances actives) de son précédent contraceptif oral combiné ou le jour du retrait de lanneau vaginal ou du patch transdermique. Au plus tard, limplant doit être inséré le lendemain de lintervalle habituel sans comprimé, sans anneau, sans patch ou de la prise de comprimés placebo de son précédent contraceptif hormonal combiné, quand la prochaine prise/insertion/application aurait du avoir lieu. Toutes les méthodes contraceptives (patch transdermique, anneau vaginal) peuvent ne pas être commercialisées dans tous les pays.
Si linsertion a lieu au moment recommandé, une contraception complémentaire n'est pas nécessaire. Si linsertion a lieu à un autre moment que celui recommandé pour linsertion, la patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
Relais dune méthode purement progestative (ex : pilule progestative, injection, implant ou système intra-utérin (SIU) libérant un progestatif)
Comme plusieurs types de méthodes purement progestatives existent, linsertion de limplant doit se faire comme suit :
· Contraceptifs injectables : insérer limplant le jour prévu pour linjection suivante.
· Pilule progestative : la femme peut passer de la pilule purement progestative à NEXPLANON nimporte quel jour du mois. Limplant doit être inséré dans les 24 heures suivant la prise du dernier comprimé.
· Implant/Système intra-utérin (SIU) : insérer limplant le jour du retrait du précédent implant ou du SIU.
Si linsertion a lieu au moment recommandé, une contraception complémentaire n'est pas nécessaire. Si linsertion a lieu à un autre moment que celui recommandé pour linsertion, la patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
Après un avortement ou une fausse couche
· Premier trimestre : limplant devra être inséré dans les cinq jours suivant lavortement ou la fausse couche du premier trimestre.
· Deuxième trimestre : insérer limplant entre le 21ème et le 28ème jour suivant lavortement ou la fausse couche du deuxième trimestre.
Si linsertion a lieu au moment recommandé, une contraception complémentaire n'est pas nécessaire. Si linsertion a lieu à un autre moment que celui recommandé pour linsertion, la patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
Post-partum
· Sans allaitement : limplant devra être inséré entre le 21ème et le 28ème jour après laccouchement. Si linsertion a lieu au moment recommandé, une contraception complémentaire n'est pas nécessaire. Si limplant est inséré plus de 28 jours après laccouchement, la patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
· Avec allaitement : limplant devra être inséré après la 4ème semaine suivant laccouchement (voir rubrique 4.6.). La patiente devra être avertie quelle doit utiliser une méthode contraceptive non hormonale pendant les 7 jours suivant linsertion. Si des rapports sexuels ont déjà eu lieu, une grossesse devra être exclue.
Comment insérer NEXPLANON
La réussite de lutilisation et du retrait de NEXPLANON repose sur une insertion sous-cutanée de limplant dans le bras non dominant réalisée correctement et avec précaution conformément aux instructions. Le professionnel de santé ayant effectué l'insertion ainsi que la patiente doivent être capables de palper limplant sous la peau de la femme après insertion.
Limplant doit être inséré en sous-cutané, juste sous la peau. Un implant inséré plus profondément quen sous-cutané (insertion profonde) peut ne pas être palpable et la localisation et/ou le retrait peuvent être difficiles (voir rubrique 4.2. « Comment retirer NEXPLANON » et rubrique 4.4). Si limplant est inséré profondément, une lésion nerveuse ou vasculaire peut se produire. Des insertions profondes ou incorrectes ont été associées à une paresthésie (due à une lésion nerveuse) et à une migration de limplant (due à une insertion dans le muscle ou dans le fascia), et dans de rares cas, à une insertion intravasculaire.
Linsertion de NEXPLANON doit être effectuée dans des conditions dasepsie et uniquement par un professionnel de santé habilité à prescrire NEXPLANON et familiarisé avec la technique. Linsertion de limplant doit être réalisée uniquement avec lapplicateur préchargé.
Il est recommandé que le professionnel de santé effectuant l'insertion soit assis lors de lintégralité de la procédure dinsertion, ainsi le site dinsertion et le mouvement de laiguille juste sous la peau pourront être bien visibles par le côté.
|
· Demandez à la patiente de sallonger sur le dos sur la table dexamen avec son bras non dominant plié au niveau du coude et tourné vers lextérieur, ainsi, soit son poignet est au même niveau que son oreillle, soit sa main est placée près de son oreille (Figure 1).
|

Figure 1
|
|
· Identifiez le site dinsertion, qui se situe à la face interne du bras non dominant, à environ 8 à 10 cm au‑dessus de lépitrochlée EN EVITANT le sillon (gouttière) entre le biceps et le triceps où les principaux vaisseaux sanguins et nerfs se trouvent dans le faisceau neurovasculaire, plus en profondeur dans le tissu sous cutané (figures 2a et 2b). Limplant doit être inséré en sous-cutané, juste sous la peau (voir rubrique 4.4.)
|
|
|
|
|
|
|
|
|
|
|

Figure 2a
|

Figure 2 b
|
|
|
· Faites deux repères avec un marqueur stérile : un premier point, pour repérer lendroit où limplant sera inséré, et un second point, quelques centimètres au-dessus du premier repère (Figure 2a). Ce second repère servira plus tard de guide pour la direction pendant linsertion.
· Nettoyez le site dinsertion avec une solution antiseptique.
· Anesthésiez la zone dinsertion (par exemple, avec un anesthésique en spray ou en injectant 2 ml de lidocaïne à 1 % juste sous la peau le long du tunnel dinsertion prévu).
· Sortez de son emballage lapplicateur NEXPLANON préchargé stérile jetable contenant limplant. Lapplicateur ne doit pas être utilisé sil y a un doute sur la stérilité.
|
|
· Tenez lapplicateur juste au-dessus de laiguille au niveau de la zone striée. Retirez le capuchon protecteur transparent de laiguille en le faisant glisser horizontalement, dans le sens de la flèche (Figure 3). Si le capuchon ne se retire pas facilement, lapplicateur ne doit pas être utilisé. Vous pouvez voir limplant blanc en regardant dans la pointe de laiguille. Ne touchez pas la manette coulissante violette avant davoir entièrement inséré laiguille sous la peau, car laiguille se rétracterait et libérerait prématurément limplant de lapplicateur.
|

Figure 3
|
|
|
|
|
|
|
· Avec votre main libre, tendez la peau autour du site dinsertion entre le pouce et lindex (Figure 4).
|

Figure 4
|
|
· Piquez la peau avec la pointe de laiguille légèrement inclinée selon un angle inférieur à 30° (Figure 5).
|

Figure 5
|
|
· Amenez lapplicateur en position horizontale. Tout en soulevant la peau avec la pointe de laiguille, introduisez laiguille sur toute sa longueur. Vous pouvez ressentir une légère résistance mais nexercez pas de force excessive (Figure 6). Si laiguille nest pas entièrement insérée, limplant ne sera pas correctement inséré.
· Vous pouvez mieux voir le mouvement de laiguille et son insertion juste sous la peau si vous êtes assis et que vous regardez lapplicateur de côté et NON du dessus. Dans cette position, vous pouvez clairement voir le site dinsertion et le mouvement de laiguille juste sous la peau.
|

Figure 6
|
|
· Maintenez lapplicateur dans la même position avec laiguille insérée sur toute sa longueur. Si nécessaire, vous pouvez utiliser votre main libre pour maintenir lapplicateur dans la même position au cours de la procédure suivante. Déverrouillez la manette coulissante violette en la poussant légèrement vers le bas. Déplacez la manette coulissante complètement en arrière jusquà la butée (Figure 7). Limplant est maintenant dans sa position sous-cutanée finale et laiguille est verrouillée dans le corps de lapplicateur. Lapplicateur peut maintenant être retiré. Si lapplicateur nest pas maintenu dans la même position au cours de la procédure ou si la manette coulissante violette nest pas complètement tirée en arrière, limplant ne sera pas correctement inséré.
|

Figure 7
|
|
· Vérifiez toujours la présence de limplant dans le bras de la patiente par palpation immédiatement après linsertion. En palpant les deux extrémités de limplant, vous devez pouvoir confirmer la présence du bâtonnet de 4 cm (Figure 8). Voir rubrique ci-dessous « Si limplant nest pas palpable ».
|

Figure 8
|
|
· Appliquez un petit pansement adhésif sur le site dinsertion. Demandez à la patiente de palper elle-même limplant.
· Appliquez une compresse stérile avec un bandage compressif pour minimiser le risque decchymose. La patiente peut retirer le bandage compressif au bout de 24 heures et le petit pansement au bout de 3 à 5 jours.
|
|
· Complétez la Carte Patiente et remettez-la à la patiente en lui demandant de la conserver. Complétez également les étiquettes adhésives et collez-les dans le dossier médical de la patiente. Si des dossiers médicaux électroniques sont utilisés, les informations figurant sur létiquette adhésive doivent être enregistrées.
· Lapplicateur est à usage unique et doit être correctement éliminé, conformément aux réglementations nationales délimination des déchets biologiques.
|
|
|
|
Si limplant nest pas palpable
Si vous ne pouvez pas palper limplant ou si vous doutez de sa présence, limplant peut ne pas avoir été inséré ou il peut avoir été inséré profondément :
· Vérifiez lapplicateur. Laiguille doit être complètement rétractée et seul le bout violet de lobturateur doit être visible.
· Utilisez dautres méthodes pour confirmer sa présence. Etant donné la nature radio-opaque de limplant, les méthodes de localisation adaptées sont la radiographie bidimensionnelle et la tomodensitométrie (TDM). Léchographie avec sonde linéaire à haute fréquence (10 MHz ou plus) ou limagerie par résonance magnétique (IRM) peuvent être utilisées. Avant deffectuer une TDM, une échographie ou une IRM pour localiser limplant, il est recommandé de contacter MSD France pour connaître les instructions. En cas déchecs de ces méthodes dimagerie, il est recommandé de vérifier la présence de limplant en mesurant le taux détonogestrel dans un échantillon de sang de la patiente. Dans ce cas, MSD France vous communiquera la procédure appropriée.
· Une méthode contraceptive non hormonale doit être utilisée tant que la présence de limplant nest pas confirmée.
· Une fois que limplant non palpable a été localisé, le retrait est recommandé dès que médicalement approprié (voir ci-dessous « Localisation et retrait dun implant non-palpable » et rubrique 4.4.).
|
Comment retirer NEXPLANON
Avant de débuter la procédure de retrait, le professionnel de santé effectuant le retrait doit consulter la Carte Patiente pour localiser limplant NEXPLANON. Vérifiez la localisation exacte de limplant dans le bras par palpation. Voir la rubrique ci-dessous « Localisation et retrait dun implant non palpable » si limplant ne peut pas être palpé.
Procédure de retrait dun implant palpable
Le retrait de limplant doit uniquement être effectué dans des conditions dasepsie et par un professionnel de santé habilité à prescrire NEXPLANON et familiarisé avec la technique de retrait.
|
· Nettoyez la zone où lincision sera réalisée et appliquez un antiseptique. Localisez limplant par palpation et marquez lextrémité distale (lextrémité la plus proche du coude), par exemple, avec un marqueur stérile (Figure 9).
|

Figure 9
|
|
· Anesthésiez le bras, par exemple, avec 0,5 à 1 ml de lidocaïne à 1 % au niveau du repère indiquant lendroit de lincision (Figure 10). Veillez à injecter lanesthésique local sous limplant pour quil reste près de la surface de la peau.
|

Figure 10
|
|
· Appuyez sur lextrémité proximale de limplant (Figure 11) pour limmobiliser ; un renflement indiquant lextrémité distale de limplant peut apparaître. En partant de lextrémité distale de limplant, faire une incision longitudinale de 2 mm vers le coude.
|

Figure 11
|
|
· Poussez doucement limplant vers lincision jusquà ce que lextrémité soit visible. Saisissez limplant avec une pince (de préférence une pince mosquito courbe) et retirez limplant (Figure 12).
|

Figure 12
|
|
· Si limplant est encapsulé, pratiquez une incision dans la gaine tissulaire et ensuite retirez limplant avec une pince (Figures 13 et 14).
|
|

Figure 13
|

Figure 14
|
|
· Si lextrémité de limplant nest pas visible au niveau de lincision, insérez doucement une pince dans lincision (Figure 15). Tournez la pince avec votre autre main (Figure 16). Avec une seconde pince, disséquez soigneusement le tissu autour de limplant et saisissez limplant (Figure 17). Limplant peut alors être retiré.
|
|

Figure 15
|

Figure 16
|
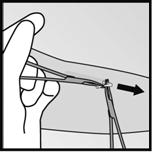
Figure 17
|
|
· Vérifiez que la totalité du bâtonnet, qui mesure 4 cm de long, a été retiré en le mesurant. Des cas dimplants cassés dans le bras des patientes ont été rapportés. Dans certains cas, une difficulté de retrait de limplant cassé a été signalée. Si un implant incomplet (moins de 4 cm) est retiré, le morceau restant devra être retiré en suivant les instructions de cette rubrique.
· Si la femme souhaite continuer à utiliser NEXPLANON, un nouvel implant peut être inséré immédiatement après le retrait du précédent implant en utilisant la même incision (voir rubrique4.2 « Comment remplacer NEXPLANON »).
|
|
|
· Après avoir retiré limplant, fermez lincision avec une suture cutanée adhésive et appliquez un pansement adhésif.
|
|
|
· Appliquez une compresse stérile avec un bandage compressif pour minimiser le risque decchymose. La patiente peut retirer le bandage compressif au bout de 24 heures et le petit pansement au bout de 3 à 5 jours.
|
|
|
|
|
|
|
|
Localisation et retrait dun implant non palpable
Il y a eu des rapports occasionnels de migration de limplant ; habituellement il sagit dun mouvement mineur par rapport à la position initiale (voir aussi rubrique 4.4.) mais cela peut conduire à un implant non palpable à lendroit où il avait été placé. Un implant qui a été inséré profondément ou qui a migré peut ne pas être palpable et cest pourquoi des procédures dimagerie, telles que décrites ci-dessous, peuvent savérer nécessaires pour la localisation.
Un implant non palpable doit toujours être localisé avant dessayer de le retirer, Etant donné la nature radio-opaque de limplant, les méthodes adaptées pour la localisation comprennent la radiographie bidimensionnelle et la tomodensitométrie (TDM). Léchographie avec sonde linéaire à haute fréquence (10 MHz ou plus) ou limagerie par résonance magnétique (IRM) peuvent être utilisées. Une fois limplant localisé dans le bras, limplant doit être retiré selon les instructions de la « Procédure de retrait dun implant palpable », et lutilisation du guidage échographique pendant le retrait doit être envisagée.
Si limplant ne peut pas être trouvé dans le bras après des tentatives exhaustives de localisation, envisagez dappliquer les techniques dimagerie au niveau du thorax, car des cas extrêmement rares de migration dans le système vasculaire pulmonaire ont été rapportés. Si limplant est localisé dans le thorax, des interventions chirurgicales ou endovasculaires peuvent être nécessaires pour le retrait ; des professionnels de santé familiarisés avec lanatomie thoracique doivent être consultés.
Si, à tout moment, ces méthodes dimagerie échouent à localiser limplant, la détermination du taux sanguin détonogestrel peut être utilisée pour vérifier la présence de limplant. Veuillez contacter MSD France pour plus de conseils.
Le retrait de limplant ne peut être effectué que dans des conditions dasepsie par un professionnel de santé familiarisé avec la technique de retrait. Si limplant a migré dans le bras, le retrait peut nécessiter une intervention chirurgicale mineure avec une incision plus grande ou une intervention chirurgicale en salle dopération. Le retrait dimplants insérés profondément doit être effectué avec précaution pour éviter toute lésion des structures nerveuses ou vasculaires profondes dans le bras et doit être réalisé par des professionnels de santé familiarisés avec lanatomie du bras.
Une chirurgie exploratoire sans connaissance de la localisation exacte de limplant est fortement déconseillée.
Si limplant ne peut être retiré, veuillez contacter MSD France pour plus de conseils.
Comment remplacer NEXPLANON
Un remplacement immédiat peut être réalisé après le retrait du précédent implant et la procédure est semblable à la procédure dinsertion décrite dans la rubrique 4.2 « Comment insérer NEXPLANON ».
Le nouvel implant peut être inséré dans le même bras et par lincision effectuée pour retirer le précédent implant. Si la même incision est utilisée pour insérer le nouvel implant, anesthésiez le site dinsertion en injectant un anesthésique, par exemple 2 ml de lidocaïne à 1 %, juste sous la peau à partir de lincision de retrait et le long du « canal dinsertion » et suivez les étapes suivantes des instructions dinsertion.
4.3. Contre-indications
· Accident thromboembolique veineux évolutif.
· Tumeurs malignes, connues ou suspectées, sensibles aux stéroïdes sexuels.
· Présence ou antécédent de tumeurs du foie (bénigne ou maligne).
· Présence ou antécédent daffection hépatique sévère tant que les paramètres de la fonction hépatique ne se sont pas normalisés.
· Hémorragies génitales non diagnostiquées.
· Hypersensibilité à la substance active ou à lun des excipients listés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
En présence de lune des conditions ou de lun des facteurs de risque mentionnés ci-dessous, la balance bénéfice/risque de lutilisation dun progestatif doit être évaluée individuellement et discutée avec la patiente avant quelle ne décide dutiliser NEXPLANON. En cas daggravation, dexacerbation ou de première apparition dune de ces conditions, la femme doit contacter un médecin ou le professionnel de santé qui lui a prescrit NEXPLANON. Celui-ci doit alors décider de larrêt éventuel de lutilisation de NEXPLANON.
Cancer du sein :
Le risque de cancer du sein augmente généralement avec lâge. Pendant lutilisation de contraceptifs oraux (combinés) [CO], le risque de diagnostic dun cancer du sein est légèrement augmenté. Laugmentation de ce risque disparaît progressivement au cours des 10 ans suivant larrêt de lutilisation de CO et nest pas liée à la durée dutilisation, mais à lâge de la femme au moment de lutilisation du CO. Le nombre attendu de cas diagnostiqués pour 10 000 femmes qui utilisent des CO combinés (jusquà 10 ans après larrêt) comparativement à celles ne les ayant jamais utilisés pendant la même période a été calculé pour les groupes dâge respectifs comme étant : 4,5/4 (16‑19 ans), 17,5/16 (20‑24 ans), 48,7/44 (25‑29 ans), 110/100 (30‑34 ans), 180/160 (35‑39 ans) et 260/230 (40‑44 ans). Le risque chez les utilisatrices de méthodes contraceptives uniquement progestatives est peut-être du même ordre que celui associé aux CO combinés. Cependant, pour ces méthodes, la preuve est moins concluante. Comparativement au risque de cancer du sein au cours dune vie, laugmentation du risque associé aux CO est faible. Les cas de cancers du sein diagnostiqués chez les utilisatrices de CO tendent à être moins avancés que chez les non‑utilisatrices de CO. Laugmentation du risque observé chez les utilisatrices de CO peut être liée à un diagnostic plus précoce, aux effets biologiques des CO ou à lassociation des deux.
Troubles hépatiques :
En cas de troubles hépatiques aigus ou chroniques, la femme doit être adressée à un spécialiste pour examen et conseils.
Evènements thrombotiques et vasculaires :
Des études épidémiologiques ont associé lutilisation des contraceptifs oraux combinés (estrogène + progestatif) à une augmentation de lincidence daccidents thromboemboliques veineux (TEV, thrombose veineuse profonde et embolie pulmonaire) et daccidents thromboemboliques artériels (TEA, infarctus du myocarde et accident vasculaire cérébral ischémique). La pertinence clinique de ces résultats pour létonogestrel (le métabolite actif du désogestrel), utilisé comme contraceptif purement progestatif en labsence dun composant estrogénique, nest pas connue.
Des données épidémiologiques limitées ne suggèrent pas daugmentation du risque de TEV ou de TEA chez les femmes utilisant limplant ; cependant, des TEV et des TEA ont été rapportés depuis la commercialisation chez les femmes utilisant des implants à létonogestrel. Il est recommandé dévaluer les facteurs de risque connus pour augmenter le risque de TEV et de TEA . Les femmes ayant des antécédents daccidents thromboemboliques doivent être averties de la possibilité dune récidive. Limplant doit être retiré en cas de thrombose. Le retrait de limplant doit aussi être considéré en cas dimmobilisation de longue durée liée à une intervention chirurgicale ou à une maladie.
Pression artérielle élevée :
Si une hypertension artérielle prolongée se développe pendant lutilisation de NEXPLANON, ou si une augmentation significative de la pression artérielle ne répond pas convenablement à une thérapeutique antihypertensive, lutilisation de NEXPLANON doit être arrêtée.
Effet sur le métabolisme des glucides :
Lutilisation de contraceptifs contenant des progestatifs peut avoir un effet sur la résistance périphérique à linsuline et sur la tolérance au glucose. Par conséquent, les femmes diabétiques doivent être attentivement suivies au cours des premiers mois dutilisation de NEXPLANON.
Chloasma :
Un chloasma peut occasionnellement apparaître, notamment chez les femmes ayant des antécédents de chloasma gravidique. Les femmes ayant des prédispositions au chloasma doivent éviter de sexposer au soleil ou aux ultraviolets au cours de lutilisation de NEXPLANON.
Poids corporel :
Leffet contraceptif de NEXPLANON est lié aux concentrations plasmatiques détonogestrel, qui sont inversement proportionnelles au poids corporel, et qui diminuent avec le temps après linsertion. Lexpérience clinique chez les femmes en surpoids au cours de la 3ème année dutilisation est limitée. Il ne peut donc être exclu que leffet contraceptif chez ces femmes au cours de la 3ème année dutilisation puisse être inférieur à celui observé chez les femmes de poids normal. Les professionnels de santé habilités à prescrire NEXPLANON doivent donc envisager de remplacer plus tôt limplant chez les femmes en surpoids.
Complications dinsertion :
Des cas de migration de limplant dans le bras depuis le site dinsertion ont été rapportés, pouvant être liés à une insertion profonde (voir rubrique 4.2. « Comment insérer NEXPLANON ») ou à des pressions extérieures (ex : manipulation de limplant ou sports de contact). Depuis la commercialisation, de rares cas dimplants localisés dans les vaisseaux du bras et dans lartère pulmonaire ont également été rapportés, pouvant être liés à des insertions profondes ou une insertion intravasculaire. Dans les cas où limplant a migré dans le bras depuis le site dinsertion, la localisation de limplant peut être rendue plus difficile et le retrait peut nécessiter une intervention chirurgicale mineure avec une incision plus large ou une intervention chirurgicale dans une salle dopération. Dans les cas où limplant a migré dans lartère pulmonaire, une intervention endovasculaire ou chirurgicale peut être nécessaire pour le retrait (voir rubrique 4.2. « Comment retirer NEXPLANON »). Si, à tout moment, limplant ne peut être palpé, il doit être localisé et le retrait est recommandé dès que médicalement approprié. Si limplant nest pas retiré, son effet contraceptif et le risque deffets indésirables liés au progestatif pourront persister au-delà de la durée désirée par la femme.
Une expulsion peut survenir en particulier si limplant na pas été inséré conformément aux instructions données à la rubrique 4.2. « Comment insérer NEXPLANON », ou à la suite dune réaction inflammatoire locale.
Kystes ovariens :
Avec tous les contraceptifs hormonaux faiblement dosés, le développement folliculaire persiste et occasionnellement un follicule peut continuer à croître dépassant la taille quil atteindrait au cours dun cycle normal. En général, ces follicules hypertrophiés disparaissent spontanément. Ils sont souvent asymptomatiques ; dans certains cas, ils sont associés à de légères douleurs abdominales. Ils nécessitent rarement une intervention chirurgicale.
Grossesses extra-utérines :
Avec les pilules uniquement progestatives traditionnelles, la protection vis-à-vis des grossesses extra‑utérines nest pas aussi bonne quavec les CO combinés, en raison de la survenue fréquente dovulations au cours de leur utilisation. Bien que NEXPLANON inhibe lovulation, une grossesse extra‑utérine doit être envisagée au cours dun diagnostic différentiel si la femme présente une aménorrhée ou des douleurs abdominales.
Autres événements :
Les événements suivants ont été rapportés à la fois lors dune grossesse et lors de lutilisation de stéroïdes sexuels, mais limputabilité de ces manifestations à lutilisation de progestatifs na pas été démontrée : ictère et/ou prurit lié à une cholestase ; formation de lithiase biliaire ; porphyrie ; lupus érythémateux disséminé ; syndrome hémolytique et urémique ; chorée de Sydenham ; herpès gestationnel ; perte daudition liée à une otosclérose et angidème (héréditaire).
Examen / consultation médical(e)
Avant linsertion ou la réinsertion de NEXPLANON, un interrogatoire médical complet (incluant les antécédents médicaux familiaux) doit être fait et une grossesse doit être exclue. La pression artérielle doit être mesurée et un examen physique doit être réalisé, avec recherche des contre-indications (voir rubrique 4.3.) et des mises en garde (voir rubrique 4.4.). Il est recommandé que la femme revienne pour un contrôle médical trois mois après linsertion de NEXPLANON. Au cours de ce contrôle, le professionnel de santé devra mesurer la pression artérielle et vérifier si la femme a des questions, des plaintes ou si des effets indésirables sont apparus. La fréquence et la nature des examens médicaux réguliers futurs doivent être adaptées à chaque femme, en fonction de lavis médical.
Les femmes seront informées que NEXPLANON ne protège pas du VIH (SIDA) ni des autres infections sexuellement transmissibles.
Diminution de lefficacité
Lefficacité de NEXPLANON peut être réduite en cas de traitement concomitant (voir rubrique 4.5.).
Changements du profil de saignement vaginal
Pendant lutilisation de NEXPLANON, il est probable que les femmes observent des changements de leur profil de saignement vaginal qui seront imprédictibles. Ceux-ci peuvent inclure lapparition de saignements vaginaux irréguliers (absents, moins fréquents, plus fréquents ou continus) et des changements de lintensité des saignements (réduits ou augmentés) ou de leur durée. Des aménorrhées ont été rapportées chez environ 1 femme sur 5 tandis que chez dautres femmes (1 femme sur 5), il a été rapporté des saignements fréquents et/ou prolongés. Chez beaucoup de femmes, le profil de saignement observé au cours des trois premiers mois est généralement prédictif du futur profil de saignement.
Une information, des conseils et lutilisation dun calendrier des saignements peuvent améliorer ladhésion de la femme à son profil de saignement. Lévaluation des saignements vaginaux doit être faite au cas par cas et peut inclure un examen visant à éliminer une pathologie gynécologique ou une grossesse.
Implant cassé ou plié in situ
Des cas dimplants cassés ou pliés dans le bras des patientes ont été rapportés. Sur la base des données in vitro, lorsque limplant est cassé ou plié, le taux de diffusion de létonogestrel peut être légèrement augmenté.
Il nest pas attendu deffet cliniquement significatif avec ce changement.
Lorsque limplant est retiré, il est important de lenlever dans son intégralité (voir rubrique 4.2. « Comment retirer NEXPLANON »).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Note : Les informations concernant les médicaments prescrits en association avec NEXPLANON doivent être consultées afin didentifier les interactions éventuelles.
Influence des autres médicaments sur NEXPLANON
Les interactions entre les contraceptifs hormonaux et les autres médicaments peuvent conduire à des hémorragies de privation et/ou à un échec de leffet contraceptif. Les interactions suivantes ont été rapportées dans la littérature (principalement avec les contraceptifs combinés mais occasionnellement aussi avec les contraceptifs purement progestatifs).
Métabolisme hépatique
Les interactions peuvent se produire avec des médicaments qui induisent des enzymes hépatiques, en particulier les enzymes du cytochrome P450, lesquelles peuvent conduire à une augmentation de la clairance des hormones sexuelles (ex : phénytoïne, phénobarbital, primidone, bosentan, carbamazépine, rifampicine, et les traitements anti-VIH (ex : ritonavir, nelfinavir, névirapine, éfavirenz) et aussi oxcarbazépine, topiramate, felbamate, griséofulvine et les produits à base de plantes contenant du millepertuis (hypericum perforatum)).
Prise en charge
Les femmes traitées avec lun des médicaments mentionnés ci-dessus doivent utiliser une méthode contraceptive non hormonale en complément de NEXPLANON. Avec des inducteurs des enzymes hépatiques, la méthode contraceptive non hormonale doit être utilisée pendant la durée du traitement concomitant et pendant 28 jours après larrêt de celui-ci.
Chez les femmes traitées à long terme avec des inducteurs enzymatiques hépatiques, il est recommandé de retirer limplant et de conseiller une méthode contraceptive qui ne soit pas modifiée par des interactions médicamenteuses.
Augmentation des taux plasmatiques hormonaux liés à une administration concomitante de médicaments
Les médicaments (ex : kétoconazole) inhibiteurs des enzymes hépatiques, comme le CYP3A4, peuvent augmenter les taux plasmatiques hormonaux.
Influence de NEXPLANON sur les autres médicaments
Les contraceptifs hormonaux peuvent modifier le métabolisme dautres médicaments. Par conséquent, les concentrations plasmatiques et tissulaires peuvent être soit augmentées (ex : ciclosporine), soit diminuées (ex : lamotrigine).
Tests biologiques
Les données obtenues avec les CO combinés ont montré que les stéroïdes contraceptifs peuvent influencer les résultats de certains tests biologiques, dont les paramètres biochimiques hépatiques, thyroïdiens, surrénaliens et rénaux, les taux sériques de protéines (porteuses), comme la globuline se liant aux corticostéroïdes (corticosteroid binding globulin) et les fractions lipidiques/lipoprotéiniques, les paramètres du métabolisme des hydrates de carbone et les paramètres de la coagulation et de la fibrinolyse. Les modifications restent généralement dans les valeurs normales. Il nest pas établi si ceci sapplique aussi aux contraceptifs purement progestatifs.
4.6. Fertilité, grossesse et allaitement
Grossesse
NEXPLANON nest pas indiqué pendant la grossesse. Si une grossesse survient au cours de lutilisation de NEXPLANON, limplant doit être retiré. Les études chez lanimal ont montré que des doses très élevées de substances progestatives peuvent causer une masculinisation des ftus féminins. De vastes études épidémiologiques nont mis en évidence ni daugmentation du risque de malformations chez les enfants nés de femmes ayant utilisé des CO avant leur grossesse, ni deffet tératogène lors de lutilisation de CO par inadvertance au cours de la grossesse. Bien que cela soit probablement le cas pour tous les CO, il nest pas démontré quil en soit de même pour NEXPLANON.
Les données de pharmacovigilance de différents médicaments contenant de létonogestrel et du désogestrel (létonogestrel est un métabolite du désogestrel) nindiquent pas non plus de risque augmenté.
Allaitement
Des données cliniques indiquent que NEXPLANON ne modifie pas la production ou la qualité (concentrations en protéines, lactose ou lipides) du lait maternel. Cependant, de faibles quantités détonogestrel sont excrétées dans le lait maternel. En se basant sur une ingestion moyenne quotidienne de lait de 150 ml/kg, la dose moyenne détonogestrel reçue par lenfant est estimée à 27 ng/kg/jour après un mois. Ceci correspond approximativement à 2,2 % de la dose quotidienne maternelle moyenne ajustée au poids et approximativement à 0,2 % de la dose maternelle quotidienne estimée en valeur absolue. Par la suite, la concentration en étonogestrel dans le lait diminue avec le temps pendant la période dallaitement.
Des données à long terme, limitées, sont disponibles chez 38 enfants, dont les mères ont commencé à utiliser limplant entre la 4ème et la 8ème semaine après laccouchement. Ils ont été allaités pendant une période moyenne de 14 mois et un suivi a été effectué jusquà lâge de 36 mois. Lévaluation de la croissance, du développement physique et psychomoteur na montré aucune différence par rapport aux enfants allaités dont les mères avaient un DIU (n = 33). Néanmoins, le développement et la croissance de lenfant devront être suivis avec précaution. En se basant sur les données disponibles, NEXPLANON peut être utilisé pendant lallaitement et doit être inséré après la 4ème semaine suivant laccouchement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Compte-tenu du profil pharmacodynamique, NEXPLANON na aucun effet ou quun effet négligeable sur l'aptitude à conduire des véhicules et à utiliser des machines.
4.8. Effets indésirables
Pendant lutilisation de NEXPLANON, il est probable que les femmes observent des changements de leur profil de saignement vaginal qui seront imprédictibles. Ceux‑ci peuvent inclure lapparition de saignements vaginaux irréguliers (absents, moins fréquents, plus fréquents ou continus) et des changements de lintensité des saignements (réduits ou augmentés) ou de leur durée. Des aménorrhées ont été rapportées chez environ 1 femme sur 5 tandis que chez dautres femmes (1 femme sur 5), il a été rapporté des saignements fréquents et/ou prolongés. Occasionnellement, des saignements abondants ont été rapportés. Lors des essais cliniques, les changements du profil de saignement ont été la raison la plus fréquente darrêt du traitement (environ 11 %). Chez beaucoup de femmes, le profil de saignement observé au cours des trois premiers mois est généralement prédictif du futur profil de saignement.
Les effets indésirables rapportés au cours des essais cliniques et possiblement liés à lutilisation de NEXPLANON ont été listés dans le tableau ci-dessous :
|
Classe de systèmes
dorganes
|
Réactions indésirables en terme MedDRA1
|
|
Très fréquent
(≥1/10)
|
Fréquent
(≥1/100 à <1/10)
|
Peu fréquent
(≥1/1000 à <1/100)
|
|
Infections et infestations
|
Infection vaginale
|
|
Pharyngite, rhinite, infection des voies urinaires
|
|
Affections du système immunitaire
|
|
|
Hypersensibilité
|
|
Affections du métabolisme et de la nutrition
|
|
Augmentation de lappétit
|
|
|
Affections psychiatriques
|
|
Instabilité émotionnelle, humeur dépressive, nervosité, diminution de la libido
|
Anxiété, insomnie
|
|
Affections du système nerveux
|
Céphalées
|
Etourdissements
|
Migraine, somnolence
|
|
Affections vasculaires
|
|
Bouffées de chaleur
|
|
|
Affections gastro‑intestinales
|
|
Douleur abdominale, nausée, flatulences
|
Vomissements, constipation, diarrhée
|
|
Affections de la peau et du tissu sous-cutané
|
Acné
|
Alopécie
|
Hypertrichose, rash, prurit
|
|
Affections musculo‑squelettiques et systémiques
|
|
|
Dorsalgies, arthralgies, myalgies, douleurs musculo-squelettiques
|
|
Affections du rein et des voies urinaires
|
|
|
Dysurie
|
|
Affections des organes de reproduction et du sein
|
Tensions mammaires, mastodynie, règles irrégulières
|
Dysménorrhée, kyste ovarien
|
Pertes vaginales, gêne vulvovaginale, galactorrhée, augmentation du volume des seins, prurit génital
|
|
Troubles généraux et anomalies au site dadministration
|
|
Douleur au site dinsertion, réaction au site dinsertion, fatigue, symptômes pseudo‑grippaux, douleur
|
Pyrexie, dème
|
|
Investigations
|
Prise de poids
|
Perte de poids
|
|
1 les termes MedDRA (version 10.1) les plus appropriés pour décrire certaines réactions indésirables ont été repris. Les synonymes et les conditions apparentées ne sont pas mentionnés mais doivent aussi être pris en compte.
Au cours de la surveillance post-commercialisation, une augmentation de la pression artérielle cliniquement significative a été observée dans de rares cas. Des cas de séborrhée ont aussi été rapportés. Des réactions anaphylactiques, une urticaire, un angio-dème, une aggravation d'un angio‑dème et/ou une aggravation dun dème angioneurotique héréditaire peuvent survenir. Linsertion et/ou le retrait de limplant peuvent entraîner des ecchymoses, une légère irritation locale, des douleurs ou des démangeaisons. Une fibrose au site d'insertion peut se produire, une cicatrice peut se former ou un abcès peut se développer. Des paresthésies ou des sensations pseudo‑paresthésiques peuvent survenir. Une expulsion ou une migration de limplant y compris, rarement, dans la paroi thoracique, ont été rapportées. Dans de rares cas, des implants ont été trouvés dans le système vasculaire y compris lartère pulmonaire. Dans certains cas dimplants trouvés dans lartère pulmonaire, une douleur thoracique et/ou une dyspnée ont été rapportées ; dautres cas ont été rapportés comme asymptomatiques (voir rubrique 4.4.). Si les instructions ne sont pas suivies (voir rubrique 4.2.), des insertions incorrectes, des difficultés de localisation et de retrait de limplant peuvent se produire. Une intervention chirurgicale peut être nécessaire pour le retrait de limplant.
Dans de rare cas, des grossesses extra-utérines ont été rapportées (voir rubrique 4.4.).
Chez les femmes utilisant des contraceptifs (oraux combinés), un certain nombre deffets indésirables (graves) ont été rapportés. Ils comprennent : des accidents thromboemboliques veineux, des accidents thromboemboliques artériels, des tumeurs hormono‑dépendantes (ex : tumeurs hépatiques, cancer du sein) et des chloasmas, plusieurs dentre eux sont détaillés dans la rubrique 4.4.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr.
4.9. Surdosage
Un implant doit toujours être retiré avant den insérer un nouveau. Aucune donnée nest disponible sur un surdosage avec létonogestrel. Il na pas été rapporté deffet délétère grave lié à un surdosage avec les contraceptifs en général.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Contraceptif hormonal à usage systémique, progestatifs, code ATC : G03AC08
Mécanisme daction
Limplant NEXPLANON est un implant non biodégradable, radio-opaque, contenant de létonogestrel destiné à un usage sous-cutané, préchargé dans un applicateur stérile, jetable. Létonogestrel est le métabolite biologiquement actif du désogestrel, un progestatif largement utilisé dans les CO. Sa structure est dérivée de la 19‑nortestostérone et il se lie avec une haute affinité aux récepteurs de la progestérone dans les organes cibles. Leffet contraceptif de létonogestrel est principalement dû à une inhibition de lovulation. Il na pas été observé dovulation durant les deux premières années dutilisation de limplant et rarement durant la troisième année. En plus de linhibition de lovulation, létonogestrel entraîne aussi des modifications de la glaire cervicale, qui gênent le passage des spermatozoïdes.
Efficacité et sécurité clinique
Les essais cliniques ont été conduits chez des femmes entre 18 et 40 ans. Bien quaucune comparaison directe nait été faite, lefficacité contraceptive est au moins comparable à celle des CO combinés. Lors des études cliniques, aucune grossesse na été observé pour les 35 057 cycles dexposition ; lindice de Pearl étudié est de 0,00 (intervalle de confiance à 95 % : 0,00 0,14). Cependant, il faut savoir quen pratique aucune méthode ne peut être considérée comme efficace à 100 %. Ce taux élevé defficacité contraceptive est obtenu, entre autre, parce que laction contraceptive de NEXPLANON est indépendante de lobservance dun traitement par la femme elle-même. Laction contraceptive de létonogestrel est réversible, ce qui se manifeste par un retour rapide à un cycle menstruel normal après le retrait de limplant. Bien que létonogestrel inhibe lovulation, lactivité ovarienne nest pas complètement supprimée. Les concentrations moyennes en estradiol restent supérieures au taux observé en phase folliculaire précoce. Dans une étude sur 2 ans, au cours de laquelle la densité minérale osseuse de 44 utilisatrices a été comparée à celle dun groupe témoin de 29 femmes utilisant un DIU, aucun effet indésirable relatif à la masse osseuse na été observé. Aucun effet cliniquement significatif sur le métabolisme des lipides na été observé. Lutilisation de contraceptifs contenant un progestatif peut avoir un effet sur la résistance à linsuline et la tolérance au glucose. Des essais cliniques additionnels ont indiqué que les utilisatrices de NEXPLANON auraient souvent des menstruations moins douloureuses (dysménorrhées).
5.2. Propriétés pharmacocinétiques
Absorption
Après linsertion de limplant, létonogestrel est rapidement absorbé dans la circulation. Les concentrations permettant linhibition de lovulation sont atteintes en 1 jour. Les concentrations sériques maximales (entre 472 et 1270 pg/ml) sont atteintes en 1 à 13 jours. Le taux de libération de limplant diminue avec le temps. En conséquence, les concentrations sériques diminuent rapidement au cours des premiers mois. A la fin de la première année, une concentration moyenne dapproximativement 200 pg/ml (entre 150‑261 pg/ml) est observée, celle-ci diminue lentement jusquà 156 pg/ml (entre 111‑202 pg/ml) à la fin de la troisième année. Les variations observées dans les concentrations sériques peuvent être, en partie, attribuées aux différences de poids corporel.
Distribution
Létonogestrel est lié à 95,5‑99 % aux protéines sériques, principalement à lalbumine et avec une importance moindre à la protéine porteuse des stéroïdes sexuels (SHBG). Le volume central de distribution et le volume total de distribution sont respectivement de 27 L et de 220 L, et ils ne se modifient quasiment pas au cours de lutilisation de NEXPLANON.
Biotransformation
Létonogestrel subit une hydroxylation et une réduction. Les métabolites sont conjugués aux sulfates et aux glucuronides. Des études sur lanimal montrent que la circulation entérohépatique ne contribue probablement pas à lactivité progestative de létonogestrel.
Élimination
Après une administration intraveineuse détonogestrel, la demi‑vie délimination moyenne est approximativement de 25 heures et la clairance sérique est approximativement de 7,5 L/heure. La clairance et la demi‑vie délimination restent constantes pendant la période de traitement. Lexcrétion de létonogestrel et de ses métabolites, sous forme de stéroïdes libres ou sous forme conjuguée, est urinaire ou fécale (avec un ratio de 1,5/1). Après insertion chez une femme qui allaite, létonogestrel est excrété dans le lait maternel avec un ratio lait/sérum de 0,44/0,50 au cours des quatre premiers mois. Chez la femme qui allaite, la dose moyenne détonogestrel ingérée par lenfant est denviron 0,2 % de la dose maternelle quotidienne estimée en valeur absolue (2,2 % lorsque les valeurs sont normalisées par kg de poids corporel). Les concentrations diminuent de façon progressive et statistiquement significative au cours du temps.
5.3. Données de sécurité préclinique
Les études de toxicologie nont pas révélé deffets autres que ceux qui peuvent être expliqués par les propriétés hormonales de létonogestrel, sans tenir compte de la voie dadministration.
6. DONNEES PHARMACEUTIQUES
6.1. Liste des excipients
Implant
Noyau : copolymère éthylène / acétate de vinyle (28% dacétate de vinyle, 43 mg)
sulfate de baryum (15 mg)
stéarate de magnésium (0,1 mg).
Enveloppe : copolymère éthylène / acétate de vinyle (15% dacétate de vinyle, 15 mg).
6.2. Incompatibilités
Sans objet.
6.3. Durée de conservation
5 ans.
NEXPLANON ne doit pas être inséré après la date de péremption mentionnée sur le conditionnement extérieur.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de conditions particulières de conservation.
A conserver dans le conditionnement primaire dorigine.
6.5. Nature et contenu de l'emballage extérieur
La plaquette thermoformée contient un implant (4 cm de long et 2 mm de diamètre) qui est préchargé dans laiguille en acier inoxydable dun applicateur stérile, prêt à lemploi, jetable. Lapplicateur contenant limplant est conditionné sous plaquette thermoformée en polyéthylène téréphtalate glycol (PETG) transparent scellée avec un opercule en polyéthylène haute densité (PEHD). Le contenu de la plaquette thermoformée est stérile à moins que le conditionnement soit endommagé ou ouvert.
Boîte de 1 ou de 5 implants.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières délimination et de manipulation
Voir rubrique 4.2.
Lapplicateur est à usage unique.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
MSD FRANCE
34, AVENUE LEONARD DE VINCI
92400 COURBEVOIE
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 351 544-3 ou 34009 351 544 3 9 : 1 implant préchargé dans laiguille (acier inoxydable) dun applicateur (acrylonitrile butadiène styrène) sous plaquette thermoformée (polyéthylène téréphtalate glycol). Boîte de 1 implant.
· 587 005-9 ou 34009 587 005 9 0 : 1 implant préchargé dans laiguille (acier inoxydable) dun applicateur (acrylonitrile butadiène styrène) sous plaquette thermoformée (polyéthylène téréphtalate glycol). Boîte de 5 implants.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter ultérieurement par le titulaire]
<Date de première autorisation:{JJ mois AAAA}>
<Date de dernier renouvellement:{JJ mois AAAA}>
<{JJ mois AAAA}>
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
11. DOSIMETRIE
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste I

















