RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 04/05/2022
MAXILASE MAUX DE GORGE ALPHA-AMYLASE 200 U. CEIP/ml, sirop
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Alpha-amylase......................................................................................................... 20 000 U. CEIP*
Pour 100 ml de sirop.
*Soit 14 286 Unités Pharmacopée Européenne pour 100 ml.
Une unité CEIP correspond à la quantité d'enzyme en mg qui catalyse l'hydrolyse de 1 mg d'amidon en 10 secondes dans les conditions du dosage.
Une cuillère à café contient 3,2 g de saccharose.
Une cuillère à soupe contient 9,6 g de saccharose.
Excipient(s) à effet notoire : saccharose (64 g), parahydroxybenzoate de méthyle sodé (E219) (0,0940 g), parahydroxybenzoate de propyle sodé (E217) (0,03 g).
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
Traitement d'appoint des états congestifs de l'oropharynx.
NB : Devant les signes cliniques généraux d'infection bactérienne, une antibiothérapie par voie générale doit être envisagée.
4.2. Posologie et mode d'administration
Adulte : 1 cuillère à soupe (15 ml), 3 fois par jour.
Population pédiatrique
Enfant de plus de 3 ans (plus de 15 kg) : 2 cuillerées à café (10 ml), 3 fois par jour.
Nourrisson et enfant de 6 mois à 3 ans (7 kg à 15 kg) : 1 cuillère à café (5 ml), 3 fois par jour.
En l'absence d'amélioration au bout de 5 jours de traitement, il est nécessaire de prendre un avis médical.
Ce médicament est contre-indiqué dans les situations suivantes :
· Hypersensibilité à l'alpha-amylase ou à l'un des excipients mentionnés à la rubrique 6.1, notamment les parabènes.
4.4. Mises en garde spéciales et précautions d'emploi
Ce médicament contient du saccharose. Son utilisation est déconseillée chez les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase-isomaltase.
Ce médicament contient 3,2 g de saccharose par cuillère à café (5 ml) et 9,6 g de saccharose par cuillère à soupe (15 ml) dont il faut tenir compte dans la ration journalière en cas de régime pauvre en sucre ou de diabète.
Ce médicament contient du parahydroxybenzoate de méthyle sodé (E219) et du parahydroxybenzoate de propyle sodé (E217) et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient moins de 1 mmol (23 mg) de sodium par cuillère à soupe de 15 ml, cest-à-dire quil est essentiellement « sans sodium ».
Précautions d'emploi
En cas d'apparition d'autres symptômes (maux de gorge importants, céphalées, nausées, vomissements...) ou de fièvre associée, la conduite à tenir doit être réévaluée.
Ce médicament ne doit pas être utilisé de façon prolongée sans avis médical.
Hypersensibilité : Des réactions dhypersensibilité, y compris des réactions de type anaphylactique et des chocs anaphylactiques, peuvent survenir dès la première prise (voir rubrique 4.8) et peuvent mettre en jeu le pronostic vital. Dans ces cas, ladministration dalpha-amylase doit être interrompue immédiatement et un traitement médical adapté doit être instauré.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les données disponibles à ce jour ne laissent pas supposer l'existence d'interactions cliniquement significatives.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n'existe pas de données de tératogénèse chez l'animal.
En clinique, aucun effet malformatif ou ftotoxique n'est apparu à ce jour. Toutefois, le suivi de grossesses exposées à ce médicament est insuffisant pour pouvoir exclure tout risque.
En conséquence, par mesure de précaution, il est préférable de ne pas utiliser ce médicament pendant la grossesse.
En l'absence de données sur le passage de l'alpha-amylase dans le lait maternel, l'utilisation de Maxilase est à éviter pendant l'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Aucun effet sur l'aptitude à conduire des véhicules et à l'utilisation des machines n'a été observé.
Les effets indésirables sont classés par système organe et par fréquence de la façon suivante : très fréquent (>1/100, < 1/10) ; peu fréquent (> 1/1 000, < 1/100) ; rare (> 1/10 000, < 1/1 000) ; très rare (< 1/10 000) et les fréquences indéterminées (qui ne peuvent pas être estimées sur la base des données disponibles).
Affections de la peau et du tissu sous-cutané
Fréquence indéterminée : angio-dème, urticaire, prurit, éruption cutanée, éruption maculopapuleuse.
Affections du système immunitaire
Fréquence indéterminée : hypersensibilité, réaction anaphylactique, choc anaphylactique (voir rubrique 4.4).
Affections respiratoires, thoraciques et médiastinales
Fréquence indéterminée : bronchospasme.
Affections gastro-intestinales
Fréquence indéterminée : nausées, vomissements
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Sans objet.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ENZYMES A VISEE ANTI-INFLAMMATOIRE
5.2. Propriétés pharmacocinétiques
5.3. Données de sécurité préclinique
Solution de saccharose, parahydroxybenzoate de méthyle sodé (E219), parahydroxybenzoate de propyle sodé (E217), acide citrique monohydraté, glycérol, huile essentielle soluble de mandarine S 164**, eau purifiée.
** Composition de l'huile essentielle soluble de mandarine S 164 : huiles essentielles non rectifiées d'orange et de mandarine, huile essentielle déterpénée de mandarine, saccharose, gomme adragante, eau purifiée.
18 mois.
6.4. Précautions particulières de conservation
A conserver à une température inférieure à 25°C.
6.5. Nature et contenu de l'emballage extérieur
125 ml ou 200 ml de sirop en flacon (verre jaune de type III) muni d'un bouchon sécurité enfant (polypropylène) avec un joint (polyéthylène).
6.6. Précautions particulières délimination et de manipulation
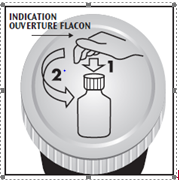
Pour ouvrir le flacon, il faut tourner le bouchon sécurité-enfant en appuyant dessus, comme indiqué sur le schéma ci-après :
|
|
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
82 AVENUE RASPAIL
94250 GENTILLY
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 34009 306 529 9 2 : 125 ml de sirop en flacon (verre jaune) avec bouchon sécurité enfant.
· 34009 343 486 8 6 : 200 ml de sirop en flacon (verre jaune) avec bouchon sécurité enfant.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament non soumis à prescription médicale.