NOTICE
ANSM - Mis à jour le : 12/06/2013
Dénomination du médicament
DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée
Triptoréline
Encadré
Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
· Gardez cette notice, vous pourriez avoir besoin de la relire.
· Si vous avez toute autre question, si vous avez un doute, demandez plus d'informations à votre médecin ou à votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez jamais à quelqu'un d'autre, même en cas de symptômes identiques, cela pourrait lui être nocif.
· Si l'un des effets indésirables devient grave ou si vous remarquez un effet indésirable non mentionné dans cette notice, parlez-en à votre médecin ou à votre pharmacien.
Sommaire notice
Dans cette notice :
1. QU'EST-CE QUE DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ET DANS QUELS CAS EST-IL UTILISE ?
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D'UTILISER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
3. COMMENT UTILISER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
5. COMMENT CONSERVER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
6. INFORMATIONS SUPPLEMENTAIRES
1. QU'EST-CE QUE DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique
Analogue de lhormone entraînant la libération des gonadotrophines.
Indications thérapeutiques
DECAPEPTYL LP 22,5 mg contient de la triptoréline, qui est semblable à une hormone appelée lhormone entraînant la libération de gonadotrophines (GnRH). Cest une forme à libération prolongée conçue pour libérer lentement 22,5 mg de triptoréline sur une période de 6 mois (vingt-quatre semaines). Il agit en abaissant le taux de lhormone masculine, la testostérone, dans le corps.
DECAPEPTYL LP 22,5 mg est utilisé pour traiter le cancer de la prostate hormono-dépendant localement avancé, seul ou pendant et après une radiothérapie. Il est aussi utilisé pour traiter le cancer de la prostate hormono-dépendant étendu à dautres parties du corps (cancer métastatique).
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D'UTILISER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
Liste des informations nécessaires avant la prise du médicament
Sans objet.
Contre-indications
Nutilisez jamais DECAPEPTYL LP 22,5 mg :
· Si vous êtes allergique (hypersensible) à la triptoréline, à lhormone entraînant la libération des gonadotrophines (GnRH), aux autres analogues de la GnRH ou à lun des autres composants contenus dans DECAPEPTYL LP 22,5 mg.
Précautions d'emploi ; mises en garde spéciales
Faites attention avec DECAPEPTYL LP 22,5 mg :
· Des cas de dépression, pouvant être sévère ont été rapportés chez des patients traités par DECAPEPTYL LP 22,5 mg. Si une humeur dépressive apparaît alors que vous êtes traité par DECAPEPTYL LP 22,5 mg, informez votre médecin.
· si vous prenez des médicaments pour prévenir la coagulation du sang (anticoagulants) car des bleus pourraient apparaître au site dinjection en raison de linjection intramusculaire.
· Au début du traitement, il y aura une augmentation de la quantité de testostérone dans votre corps. Ceci peut entraîner une aggravation des symptômes du cancer. Contactez votre médecin si cela se produit. Votre médecin pourra vous prescrire des médicaments (un anti-androgène) pour éviter que vos symptômes ne saggravent.
· Au cours des premières semaines de traitement, DECAPEPTYL LP 22,5 mg, comme les autres analogues de la GnRH, peut, dans des cas isolés, entraîner une compression de la moelle épinière ou un blocage de lurètre (par lequel passe lurine). Dans ces cas, votre médecin mettra en place un suivi particulier et vous prescrira un traitement adapté.
· Après castration chirurgicale, la triptoréline ninduit pas de réduction supplémentaire du taux de testostérone et par conséquent ne doit pas être utilisée après orchidectomie.
· Des tests diagnostiques de la fonction gonadotrope hypophysaire conduits durant le traitement et après linterruption de la thérapie avec DECAPEPTYL LP 22,5 mg peuvent être faussés.
· Le traitement par DECAPEPTYL LP 22,5 mg, comme par les autres analogues de la GnRH, peut entraîner une perte osseuse, une ostéoporose et un risque accru de fracture osseuse, si vous êtes un grand consommateur dalcool, si vous êtes fumeur, sil y a des cas dostéoporose (maladie qui affecte la résistance des os) dans votre famille, si vous avez une mauvaise alimentation ou si vous prenez des antiépileptiques (médicaments utilisés pour traiter diverses formes d'épilepsie) ou des corticoïdes (dérivés de la cortisone).
· Si vous êtes diabétique ou si vous souffrez de problèmes cardiaques ou vasculaires, vous devez en informer votre médecin.
· Si vous avez, sans que cela nait été découvert jusque-là, une augmentation du volume (tumeur bénigne) de la glande hypophysaire, elle pourrait être découverte au cours du traitement par DECAPEPTYL LP 22,5 mg. Les symptômes incluent lapparition de maux de tête soudains, des vomissements, des problèmes de vue et une paralysie des yeux.
Si vous êtes concernés par un des signes cités ci-dessus, parlez-en à votre médecin.
Enfants
DECAPEPTYL LP 22,5 mg nest pas indiqué chez les nouveau-nés, les enfants et les adolescents.
Interactions avec d'autres médicaments
Prise d'autres médicaments
Si vous prenez ou avez pris récemment un autre médicament, y compris un médicament obtenu sans ordonnance, parlez-en à votre médecin ou à votre pharmacien.
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Grossesse et allaitement
DECAPEPTYL LP 22,5 mg nest pas destiné à être utilisé chez la femme.
Sportifs
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Conduite de véhicules et utilisation de machines
Même si DECAPEPTYL LP 22,5 mg est utilisé comme indiqué, il peut modifier les réactions à un point tel que la capacité à conduire ou à utiliser des machines est altérée. Ceci est particulièrement vrai en cas dassociation à la prise dalcool. Vous pouvez ressentir des étourdissements, de la fatigue ou avoir des problèmes de vue tels quune vision trouble. Ce sont des effets indésirables possibles du traitement ou de la maladie traitée. Si vous ressentez un de ces effets indésirables, vous ne devez pas conduire ou utiliser des machines.
Liste des excipients à effet notoire
Informations importantes concernant certains composants de DECAPEPTYL LP 22,5 mg
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, cest-à-dire qu'il est essentiellement "sans sodium" et peut être administré si vous suivez un régime alimentaire pauvre en sodium.
3. COMMENT UTILISER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
Instructions pour un bon usage
DECAPEPTYL LP 22,5 mg doit être administré sous surveillance médicale.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
Le traitement du cancer de la prostate avec DECAPEPTYL LP 22,5 mg nécessite un traitement à long terme.
Dans le traitement du cancer de la prostate hormono-dépendant pendant et après une radiothérapie, la durée de traitement recommandée est de 2 à 3 ans.
La dose habituelle est de 1 flacon de DECAPEPTYL LP 22,5 mg administré par injection intramusculaire tous les 6 mois (24 semaines).
Votre médecin pourra vous prescrire des analyses de sang afin de mesurer lefficacité du traitement.
Symptômes et instructions en cas de surdosage
Sans objet.
Instructions en cas d'omission d'une ou de plusieurs doses
Sans objet.
Risque de syndrome de sevrage
Si vous avez limpression que les effets de DECAPEPTYL LP 22,5 mg sont trop forts ou trop faibles, parlez-en à votre médecin ou à votre pharmacien.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Comme tous les médicaments, DECAPEPTYL LP 22,5 mg est susceptible d'avoir des effets indésirables, bien que tout le monde ny soit pas sujet.
Comme il a été observé avec dautres agonistes de la GnRH ou après castration chirurgicale, les effets indésirables les plus communément observés lors du traitement avec la triptoréline étaient dus à ses effets pharmacologiques attendus. Ces effets incluaient des bouffées de chaleur (50%), des troubles de lérection (4%) et une diminution de la libido (3%).
Une augmentation des lymphocytes a été rapportée chez des patients traités par des analogues de la GnRH.
A lexception de réactions immuno-allergiques et au site dinjection, tous les effets indésirables sont connus pour être liés aux changements des taux de testostérone.
Comme avec les autres agonistes de la GnRH, des réactions dhypersensibilité et des réactions allergiques (anaphylactiques) ont été rapportées avec la triptoréline.
Très fréquents (concernent plus de 1 patient sur 10)
· Bouffées de chaleur.
· Sensation de faiblesse.
· Transpiration excessive.
· Douleur dorsale.
· Fourmillements dans les jambes.
Fréquents (concernent de 1 à 10 patients sur 100)
· Nausées.
· Fatigue, réactions au site dinjection (rougeur, inflammation et/ou douleur), douleurs osseuses et musculaires, douleurs des extrémités des membres, dème (accumulation de liquide dans les tissus).
· Sensations vertigineuses, maux de tête.
· Troubles de lérection, baisse de la libido.
· Altération de lhumeur, dépression.
Peu fréquents (concernent de 1 à 10 patients sur 1 000)
· Bourdonnements doreilles.
· Douleur abdominale, constipation, diarrhée, vomissements.
· Somnolence, frissons, état de sommeil profond, douleur.
· Modification de certains examens sanguins (incluant une augmentation des marqueurs du foie).
· Prise de poids.
· Perte dappétit, goutte (douleur intense et gonflement des articulations, généralement du gros orteil).
· Augmentation de lappétit.
· Douleur articulaire, crampe musculaire, faiblesse musculaire, douleur musculaire.
· Fourmillements ou engourdissement.
· Insomnie, irritabilité.
· Gonflement des seins, douleur des seins, réduction de la taille des testicules, douleur testiculaire.
· Difficulté à respirer.
· Acné, chute des cheveux, démangeaisons, éruption cutanée.
· Tension artérielle élevée.
Rares (concernent de 1 à 10 patients sur 10 000)
· Coloration rouge ou violette de la peau.
· Diabète.
· Vertiges.
· Sensation anormale dans les yeux, troubles de la vision.
· Ballonnements, flatulence, bouche sèche, anomalies du goût.
· Douleur thoracique.
· Difficulté à rester debout.
· Symptômes pseudo-grippaux, fièvre.
· Réaction allergique, réaction anaphylactique (réaction allergique grave pouvant provoquer des sensations de vertiges ou des difficultés à respirer).
· Inflammation du nez et de la gorge.
· Augmentation de la température du corps.
· Perte de poids.
· Raideur articulaire, gonflement des articulations, raideur musculo-squelettique, arthrose.
· Troubles de la mémoire.
· Etat confusionnel, baisse de lactivité, euphorie.
· Trouble de léjaculation.
· Respiration courte en position couchée.
· Ampoules cutanées.
· Saignement de nez.
· Tension artérielle basse.
Au cours de la surveillance post-commercialisation des effets indésirables suivants ont également été rapportés : vision floue, tension artérielle augmentée, malaise général, douleurs osseuses, anxiété et formation rapide de papules due à un gonflement de la peau ou des muqueuses (urticaire).
Votre médecin décidera des mesures à prendre.
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables deviennent graves, veuillez en informer votre médecin ou votre pharmacien.
5. COMMENT CONSERVER DECAPEPTYL LP 22,5 mg, poudre et solvant pour suspension injectable à libération prolongée ?
Tenir hors de la portée et de la vue des enfants.
Date de péremption
Ne pas utiliser DECAPEPTYL LP 22,5 mg après la date de péremption mentionnée sur la boîte et sur les étiquettes après EXP. La date d'expiration fait référence au dernier jour du mois.
Conditions de conservation
A conserver à une température ne dépassant pas 25°C.
Après reconstitution: la suspension reconstituée doit être utilisée immédiatement.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
Les médicaments ne doivent pas être jetés au tout à l'égout ou avec les ordures ménagères. Demandez à votre pharmacien ce qu'il faut faire des médicaments inutilisés. Ces mesures permettront de protéger l'environnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Que contient DECAPEPTYL LP 22,5 mg ?
La substance active est:
Triptoréline.
Un flacon de poudre contient 22,5 mg de triptoréline sous forme d'embonate de triptoréline.
Après reconstitution avec 2 ml de solvant, 1 ml de suspension reconstituée contient 11,25 mg de triptoréline.
Les autres composants sont:
Poudre: polymère D, L -lactide co-glycolide, mannitol, carmelllose sodique, polysorbate 80.
Solvant: eau pour préparations injectable.
Forme pharmaceutique et contenu
Qu'est-ce que DECAPEPTYL LP 22,5 mg et contenu de l'emballage extérieur ?
Ce médicament se présente sous forme de poudre et solvant pour suspension injectable à libération prolongée, la poudre est blanche à blanc cassé et le solvant est une solution limpide.
Boîte de 1 flacon, 1 ampoule et 1 blister contenant une seringue et deux aiguilles.
Nom et adresse du titulaire de l'autorisation de mise sur le marché et du titulaire de l'autorisation de fabrication responsable de la libération des lots, si différent
Titulaire
IPSEN PHARMA
65 QUAI GEORGES GORSE
92100 BOULOGNE-BILLANCOURT
FRANCE
Exploitant
IPSEN PHARMA
65 QUAI GEORGES GORSE
92100 BOULOGNE-BILLANCOURT
FRANCE
Fabricant
IPSEN PHARMA BIOTECH
PARC D'ACTIVITE DU PLATEAU DE SIGNES
CHEMIN DEPARTEMENTAL N°402
83870 SIGNES
FRANCE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet
Date dapprobation de la notice
La dernière date à laquelle cette notice a été approuvée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet
Informations Internet
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).
Informations réservées aux professionnels de santé
Les informations suivantes sont destinées exclusivement aux professionnels de santé (voir rubrique 3) :
Instructions dutilisation
1. Préparation du patient avant la reconstitution
Préparer le patient en désinfectant le muscle fessier au site dinjection. Cette étape doit être réalisée en premier car la suspension doit être injectée immédiatement après la reconstitution.
2. Préparation de linjection
La présence de bulles au dessus du lyophilisat est un aspect normal du produit.
· Sortez l'ampoule contenant le solvant. Si une partie de la solution est bloquée dans le haut de lampoule, la tapoter afin de la faire descendre dans le corps de lampoule.
· Sortez le flacon contenant la poudre. La poudre éventuellement accumulée en haut du flacon doit être ramenée au fond du flacon par tapotement.
· Retirer le capuchon en plastique du flacon.
· Visser une aiguille sur la seringue. Ne pas retirer le capuchon de laiguille à ce stade.
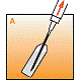
· Casser le haut de lampoule en positionnant le point face à soi.
|
|
· Retirer le capuchon de laiguille. Insérer laiguille dans lampoule et prélever la totalité du solvant dans la seringue.
|
|
|
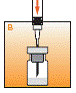
· Enfoncer verticalement laiguille au travers du bouchon en plastique du flacon. Injecter le solvant lentement, de façon à, si possible, rincer toute la partie supérieure du flacon.
|
|

|
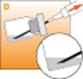
· Remonter l'aiguille au dessus du niveau du liquide et reconstituer la suspension en balançant doucement le flacon, c'est-à-dire en lagitant horizontalement.
Agiter le temps nécessaire à lobtention dune suspension homogène et laiteuse.
· Vérifier labsence dagglomérats (en cas dagglomérats poursuivre lagitation jusquà complète homogénéisation).
|
|
|
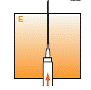
· Quand la suspension est homogène, descendre laiguille et aspirer toute la suspension dans la seringue (sans retourner le flacon). Une petite quantité de suspension restera dans le flacon et devra être éliminée. Un excès de poudre et de solvant est prévu lors de la fabrication pour autoriser cette perte lors de la préparation de la seringue.
|
|
|
· Enlever laiguille utilisée pour la reconstitution en la saisissant par lembout coloré. Fixer lautre aiguille sur le bout de la seringue (visser complètement).
· Enlever le capuchon de laiguille.
|
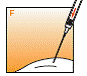
2. Injecter
|
|
· Amorcer laiguille en vidant lair contenu dans la seringue immédiatement avant linjection. Pour éviter que la suspension précipite, injecter immédiatement dans le muscle fessier préalablement désinfecté.
|
3. Après utilisation
Jeter les aiguilles dans des containers adaptés.
Autres
Sans objet.





