ANSM - Mis à jour le : 06/09/2013
DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution
Dorzolamide/timolol
Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
· Gardez cette notice, vous pourriez avoir besoin de la relire.
· Si vous avez toute autre question, si vous avez un doute, demandez plus d'informations à votre médecin ou à votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez jamais à quelqu'un d'autre, même en cas de symptômes identiques, cela pourrait lui être nocif.
· Si l'un des effets indésirables devient grave ou si vous remarquez un effet indésirable non mentionné dans cette notice, parlez-en à votre médecin ou à votre pharmacien.
Dans cette notice :
1. QU'EST-CE QUE DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D'UTILISER DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
3. COMMENT UTILISER DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
5. COMMENT CONSERVER DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
6. INFORMATIONS SUPPLEMENTAIRES
Antiglaucomateux et myotiques, bêta-bloquants, Timolol, associations.
DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution contient deux médicaments: dorzolamide et timolol.
· Le dorzolamide appartient à une classe de médicaments appelés "inhibiteurs de l'anhydrase carbonique".
· Le timolol appartient à une classe de médicaments appelés "bêta-bloquants".
DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution est indiqué pour faire baisser la pression intra-oculaire élevée (PIO) chez les patients présentant un glaucome lorsqu'un collyre bêta- bloquant administré seul est insuffisant.
Liste des informations nécessaires avant la prise du médicament
Sans objet.
· Si vous êtes allergique (hypersensible) au dorzolamide, au timolol, aux bêta-bloquants ou à lun des autres composants.
· Si vous souffrez ou avez souffert dans le passé de troubles respiratoires tels que lasthme ou la bronchopneumopathie chronique obstructive.
· Si vous avez une maladie rénale sévère ou des antécédents de calculs rénaux.
· Si vous avez une anomalie du pH sanguin (trouble de l'équilibre acido-basique).
· Si vous avez une maladie cardiaque dont certains troubles du rythme cardiaque qui produisent un rythme cardiaque anormalement lent ou une insuffisance cardiaque grave.
Si vous n'êtes pas sûr de pouvoir utiliser DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution, contactez votre médecin ou votre pharmacien.
Précautions d'emploi ; mises en garde spéciales
Faites attention avec DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution:
Avant dutiliser ce médicament, indiquez à votre médecin si vous souffrez ou avez souffert dans le passé de :
o maladie coronarienne, insuffisance cardiaque, hypotension artérielle
o troubles de la fréquence cardiaque, une bradycardie par exemple
o de troubles respiratoires, dasthme ou de broncho-pneumopathie chronique obstructive
o de troubles artériels périphériques, tels quune maladie de Raynaud ou un syndrome de Raynaud)
o de diabète, car le timolol peut masquer les signes et symptômes dune hypoglycémie
o dhyperactivité de la thyroïde, car le timolol peut en masquer les signes et symptômes
Si vous avez des antécédents de problèmes cardiaques, votre médecin peut souhaiter contrôler votre fréquence cardiaque ou d'autres paramètres de la fonction cardiaque au cours de l'utilisation de DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution.
Informez votre médecin si vous avez ou avez eu des problèmes hépatique, si vous avez une faiblesse musculaire ou si on vous a diagnostiqué comme ayant une myasthénie maligne.
Vous devez également informé votre médecin si vous avez ou avez eu dans le passé de l'asthme ou d'autres problèmes pulmonaires, une angine de poitrine de Prinzmetal (douleur dans la poitrine au repos), d'autres problèmes cardiaques (incluant certains types de troubles du rythme cardiaque induisant des battements cardiaques lents ou une insuffisance cardiaque sévère), des problèmes de circulation, une pression artérielle basse, du diabète ou une hypoglycémie (faible quantité de sucre dans le sang), des problèmes de thyroïde ou d'allergies après la prise d'un médicament.
Si vous développez une conjonctivite (rougeur et irritation de l'il ou des yeux), gonflement de l'il ou de la paupière, rash cutané, ou des démangeaisons dans ou à proximité de l'il, contactez immédiatement votre médecin. De tels symptômes peuvent être dû à une réaction allergique ou bien un effet secondaire de DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution (voir rubrique « effets secondaires ».).
Informez votre médecin si vous développez une infection oculaire, avez une blessure à l'il, avez une intervention chirurgicale oculaire, développez d'autres réactions ou si les symptômes s'aggravent.
Si vous portez des lentilles de contact souples, vous devez retirer vos lentilles avant d'utiliser ce médicament et attendre au moins 15 minutes avant de les remettre car ce médicament contient un conservateur le chlorure de benzalkonium qui peut décolorer vos lentilles de contact.
Avant toute anesthésie chirurgicale (même chez le dentiste), prévenez le médecin que vous prenez Dorzolamide/Timolol Mylan, car il peut se produire une chute brutale de la pression artérielle liée à lagent anesthésique et le timolol peut modifier les effets de certains médicaments utilisés au cours de lanesthésie.
Utilisation chez l'enfant
Chez le nourrisson et l'enfant, l'expérience avec DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution est limitée.
Utilisation chez les personnes âgées
Dans les études avec DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution, les effets ont été similaires chez les patients âgés et les patients plus jeunes.
Interactions avec d'autres médicaments
Dorzolamide/Timolol peut modifier les effets dautres médicaments que vous prenez ou être modifié par eux, y compris par dautres collyres utilisés pour le traitement du glaucome. Informez votre médecin que vous prenez ou avez lintention de prendre des médicaments antihypertenseurs ou pour le traitement de troubles cardiaques ou du diabète. Si vous prenez ou avez pris récemment un autre médicament, y compris un médicament délivré sans ordonnance, parlez-en à votre médecin ou à votre pharmacien. Ceci est particulièrement important si lun des points ci-dessous sapplique à vous :
· vous prenez des médicaments pour diminuer la pression artérielle ou pour traiter une maladie cardiaque (tels qu'inhibiteur calcique, bêta-bloquant ou digoxine).
· vous prenez des médicaments pour traiter un rythme cardiaque irrégulier ou perturbé tels que la quinidine ou de la digoxine.
· vous utilisez un autre collyre qui contient un bêta-bloquant.
· vous prenez un autre inhibiteur de l'anhydrase carbonique tel que l'acétazolamide, que ce soit un médicament que vous prenez par voie orale, sous forme de collyre ou toutes autres voies d'administration.
· vous prenez un médicament de la famille des inhibiteurs de la monoamine oxydase (IMAO), ou un inhibiteur sélectif de la recapture de la sérotonine (ISRS), ces médicaments étant utilisés pour traiter votre dépression ou d'autres maladies.
· vous prenez un médicament parasympathomimétique qui vous a été prescrit pour vous aider à uriner. Les parasympathomimétiques appartiennent à une famille de médicaments qui sont parfois également utilisés pour aider à la restauration d'un transit intestinal normal.
· vous prenez des narcotiques tels que la morphine utilisée pour traiter des douleurs modérées à fortes, ou si vous prenez de fortes doses d'aspirine. Bien qu'il n'y ait aucune preuve d'interaction entre le chlorhydrate de dorzalamide et l'aspirine, d'autres médicaments qui sont proches du chlorhydrate de dorzolamide et qui sont pris par voie orale, sont connus pour interagir avec l'aspirine.
· vous prenez un médicament pour traiter le diabète ou glycémie élevée.
· vous prenez de l'adrénaline (épinéphrine).
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Nutilisez pas Dorzolamide/Timolol Mylan 20 mg/ml 5 mg/ml, collyre en solution si vous êtes enceinte, sauf si votre médecin lestime nécessaire. Nutilisez pas Dorzolamide/Timolol Mylan 20 mg/ml 5 mg/ml, collyre en solution si vous allaitez. Le timolol peut passer dans votre lait.
Demandez conseil à votre médecin avant de prendre un médicament pendant que vous allaitez.
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Conduite de véhicules et utilisation de machines:
Il existe des effets indésirables associés à DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution, tels que vision trouble qui peuvent altérer l'aptitude à conduire ou à utiliser des machines. Ne pas conduire ou utiliser de machines avant que vous ne vous sentiez bien ou que votre vision soit claire.
Liste des excipients à effet notoire
Informations importantes concernant certains composants de DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution:
En raison de la présence de chlorure de benzalkonium, ce médicament peut provoquer une irritation des yeux.
Eviter le contact avec les lentilles de contact souples. Retirer les lentilles de contact avant application et attendre au moins 15 minutes avant de les remettre.
Le chlorure de benzalkonium peut décolorer les lentilles de contact souple.
3. COMMENT UTILISER DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
Instructions pour un bon usage
Sans objet.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
La posologie adéquate et la durée du traitement seront établies par votre médecin.
La dose habituelle est d'une goutte dans l'il (les yeux) atteint(s), deux fois par jour par exemple le matin et le soir.
En cas d'utilisation concomitante de DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution avec un autre collyre: les instillations successives de chaque collyre doivent être espacées d'au moins 10 minutes.
Ne modifiez pas la posologie de ce médicament sans en avertir votre médecin. Si vous devez arrêter votre traitement, contactez votre médecin immédiatement.
Evitez tout contact de l'extrémité du flacon avec l'il ou les parties avoisinantes. Il pourrait en effet se contaminer par des bactéries qui peuvent entraîner des lésions graves de l'il, voire même la perte de la vision. Pour éviter toute contamination possible du flacon, lavez-vous les mains avant utilisation de ce collyre et empêchez tout contact de l'embout du flacon avec son environnement.
Pour garantir la délivrance d'une dose conforme, l'embout ne doit pas être élargi.
Mode d'emploi:
Il est recommandé de vous laver les mains avant l'instillation de votre collyre.
Il est peut-être plus facile d'instiller le collyre devant un miroir.

1. Avant d'utiliser le médicament pour la première fois, assurez-vous que la bague d'inviolabilité située au niveau du col du flacon n'est pas rompue. Un espace entre le flacon et le bouchon est normal sur un flacon non ouvert.
2. Retirez le bouchon du flacon.
3. Inclinez votre tête en arrière et tirez légèrement la paupière inférieure vers le bas de manière à former une petite poche entre la paupière et l'il.
4. Renversez le flacon et pressez-le doucement jusqu'à ce qu'une seule goutte tombe dans l'il comme indiqué par votre médecin. NE TOUCHEZ PAS L'IL OU LA PAUPIERE AVEC L'EMBOUT DU FLACON.
5. Répétez les étapes 3 et 4 pour l'autre il si votre médecin vous l'a prescrit.
6. Remettez le bouchon et fermez le flacon immédiatement après l'avoir utilisé.
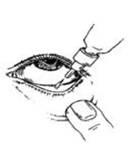
Après avoir utilisé Dorzolamide/Timolol, comprimez le coin de votre oeil, du côté du nez (photo X), avec un doigt pendant 2 minutes. Ceci contribue à empêcher le timolol de passer dans le reste de votre corps.
Symptômes et instructions en cas de surdosage
Si vous avez utilisé plus de DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution que vous n'auriez dû:
Il est important de respecter la dose prescrite par votre médecin. Si vous instillez trop de gouttes dans votre il ou si vous avalez le contenu du flacon, parmi d'autres effets, vous pouvez avoir notamment des étourdissements, des difficultés à respirer, ou sentir que votre rythme cardiaque ralentit. Contactez immédiatement votre médecin.
Instructions en cas d'omission d'une ou de plusieurs doses
Si vous oubliez d'utiliser DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution:
Il est important de prendre DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution comme votre médecin vous l'a prescrit. Si vous oubliez d'instiller une goutte à l'heure prévue, instillez-la le plus tôt possible après l'oubli. Cependant, s'il est presque l'heure de l'instillation suivante, reprenez votre médicament normalement à l'heure habituelle suivante. Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d'utiliser DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution:
Si vous voulez arrêter ce médicament parlez-en d'abord à votre médecin.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez conseil à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Comme tous les médicaments, DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution est susceptible d'avoir des effets indésirables, bien que tout le monde n'y soit pas sujet.
Il est généralement possible de continuer à utiliser le collyre, à moins que les effets ne soient sévères. Si vous êtes inquiet, parlez-en à votre médecin ou à votre pharmacien. Narrêtez pas dutiliser Dorzolamide /Timolol sans en avoir parlé à votre médecin.
Si vous avez des réactions allergiques incluant une urticaire, un gonflement du visage, des lèvres, de la langue, et/ou de la gorge qui peuvent provoquer une difficulté à respirer ou à avaler, arrêtez DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution et consultez immédiatement votre médecin.
Les effets indésirables suivants ont été rapportés avec DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution:
Trés fréquent (apparaissant chez plus de 1 patient traité sur 10):
Brûlures et picotements des yeux, altération du goût.
Fréquent (apparaissant chez 1 à 10 patients traités sur 100):
Rougeur de/et autour de l'il(des yeux), larmoiement ou démangeaisons de l'il(des yeux), et effets sur la surface de l'il(des yeux), gonflement et/ou irritation de/et autour de l'il(des yeux), sensation d'avoir quelque chose dans l'il (érosion de la cornée), baisse de la sensibilité cornéenne (ne pas se rendre compte de la présence d'un corps étranger dans l'il et absence de sensation de douleur), douleur oculaire, yeux secs, vision trouble, maux de tête, sinusite (sensation de tension dans le nez ou de nez plein), nausées et fatigue.
Peu fréquent (apparaissant chez 1 à 10 patients traités sur 1 000):
Etourdissement, dépression, inflammation de l'iris, vision trouble (dû à l'interruption d'un traitement par collyre myotique dans certains cas), rythme cardiaque lent, évanouissement, indigestion et calculs rénaux (souvent marqués par un début soudain de douleurs importantes de type crampes, localisées dans le bas du dos et/ou sur le côté, dans l'aine ou l'abdomen).
Rare (apparaissant chez 1 à 10 patients traités sur 10 000):
Lupus érythémateux disséminé (une maladie immunitaire qui peut entraîner une inflammation des organes internes), fourmillement ou engourdissement des mains ou des pieds, insomnie, cauchemars, perte de mémoire, faiblesse des muscles, diminution de la libido, accident vasculaire cérébral, myopie transitoire qui peut cesser à l'arrêt du traitement, décollement de la choroïde (après chirurgie filtrante), chute des paupières, vision double, lésions croûteuses palpébrales, dème de la cornée (avec des symptômes de troubles visuels), pression oculaire basse, bourdonnements dans les oreilles, pression artérielle basse, rythme cardiaque irrégulier, douleur thoracique, palpitations (battements du cur plus rapides et/ou irréguliers), crise cardiaque, flux sanguin réduit vers le cerveau, gonflement ou froideur des mains et des pieds et mauvaise circulation des bras et des jambes, crampes et/ou douleur des jambes pendant la marche (claudication), essoufflement, insuffisance respiratoire, nez bouché ou qui coule, saignement de nez, difficulté à respirer, toux, irritation de la gorge, sécheresse buccale, diarrhée, dermite de contact, perte de cheveux, psoriasis ou aggravation de psoriasis, maladie de La Peyronie (pouvant causer une courbure du pénis), faiblesse/fatigue, réactions de type allergique telles que éruption, urticaire, démangeaisons, en de rares cas gonflement des lèvres, des yeux et de la bouche, respiration sifflante.
Comme avec dautres médicaments ophtalmiques à usage topique, le timolol passe dans le sang. Il peut en résulter les mêmes effets indésirables quavec les bêta-bloquants pris par voie générale. Après application ophtalmique topique, la fréquence des effets indésirables est moindre quaprès administration systémique. Les effets indésirables mentionnés incluent les réactions observées au sein de la classe des bêta-bloquants ophtalmiques :
o Réactions allergiques systémiques : oedème angio-neurotique, urticaire, éruption cutanée localisée ou généralisée, prurit, réaction anaphylactique.
o Hypoglycémie.
o Insomnie, dépression, cauchemars, pertes de mémoire.
o Syncopes, accident vasculaire cérébral, ischémie cérébrale, aggravation des signes et symptômes de myasthénie, vertiges, paresthésies et céphalées.
o Signes et symptômes dirritation oculaire (sensation de brûlure, picotements, prurit, larmoiement, rougeur), blépharite, kératite, flou visuel et décollement de la choroïde après intervention de filtration, diminution de la sensibilité cornéenne, sécheresse oculaire, ulcérations cornéennes, ptosis, diplopie.
o Bradycardie, douleur thoracique, palpitations, oedème, troubles du rythme, insuffisance cardiaque congestive, bloc atrio-ventriculaire, arrêt cardiaque, insuffisance cardiaque.
o Hypotension artérielle, phénomène de Raynaud, mains et pieds froids.
o Bronchospasme (surtout chez les patients atteints dune maladie bronchospastique préexistante), dyspnée, toux.
o Dysgueusie, nausées, dyspepsie, diarrhée, sécheresse buccale, douleurs abdominales, vomissements.
o Alopécie, éruption psoriasiforme ou exacerbation dun psoriasis, éruption cutanée.
o Myalgies.
o Troubles de la fonction sexuelle, diminution de la libido.
o Asthénie/fatigue.
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables deviennent graves, veuillez en informer votre médecin ou votre pharmacien en particulier si vous constatez des troubles de la vision en utilisant ce médicament après une intervention chirurgicale oculaire.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (Ansm) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.ansm.sante.fr. En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
Tenir hors de la portée et de la vue des enfants.
Ne pas utiliser DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution après la date de péremption mentionnée sur l'étiquette, la boîte après {EXP}. La date d'expiration fait référence au dernier jour du mois.
Pas de précautions particulières de conservation.
Ce médicament doit être utilisé dans les 28 jours qui suivent l'ouverture du flacon. Vous devez donc jeter le flacon 4 semaines après l'avoir ouvert même s'il reste un peu de solution. Pour vous aider à vous en rappeler, inscrivez la date à laquelle vous avez ouvert le flacon dans le cadre prévu à cet effet sur la boîte.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
Les médicaments ne doivent pas être jetés au tout à l'égout ou avec les ordures ménagères. Demandez à votre pharmacien ce qu'il faut faire des médicaments inutilisés. Ces mesures permettront de protéger l'environnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Que contient DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution ?
Les substances actives sont: le chlorhydrate de dorzolamide et le maléate de timolol.
Chaque millilitre contient 22,26 mg de chlorhydrate de dorzolamide correspondant à 20 mg de dorzolamide et 6,83 mg de maléate de timolol correspondant à 5 mg de timolol.
Les autres composants sont:
L'hydroxyéthylcellulose, le mannitol, le citrate de sodium, l'hydroxyde de sodium pour l'ajustement du pH et l'eau pour préparations injectables. Le chlorure de benzalkonium est ajouté comme conservateur.
Forme pharmaceutique et contenu
Qu'est-ce que DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution et contenu de l'emballage extérieur ?
DORZOLAMIDE/TIMOLOL MYLAN 20 mg/ml + 5 mg/ml, collyre en solution est une solution stérile, incolore, claire et légèrement visqueuse.
Flacon à usage ophtalmique blanc opaque (PE de densité intermédiaire), muni d'un embout compte-gouttes scellé (PEBD) et avec un bouchon à vis (PEHD) et une bague d'inviolabilité au niveau du col, contenant 5 ml de collyre en solution.
Boîte de 1, 3 ou 6 flacons de 5 ml.
Toutes les présentations peuvent ne pas être commercialisées.
MYLAN SAS
117 ALLEE DES PARCS
69800 SAINT PRIEST
MYLAN SAS
117 ALLEE DES PARCS
69800 SAINT PRIEST
PHARMATHEN SA
6, DERVENAKION STR.,
15351 PALLINI, ATTIKI
GRECE
ou
FAMAR SA, PLANT A
63 AGIOU DIMITRIOU STREET,
174 56 ALIMOS
GRECE
ou
MYLAN SAS
117, ALLEE DES PARCS
69 800 SAINT-PRIEST
FRANCE
ou
MYLAN SAS
ZAC DES GAULNES
69 330 MEYZIEU
FRANCE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants:
Conformément à la réglementation en vigueur.
Date dapprobation de la notice
La dernière date à laquelle cette notice a été approuvée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lAnsm (France).
Informations réservées aux professionnels de santé
Sans objet.
Sans objet.