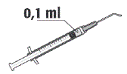NOTICE
ANSM - Mis à jour le : 26/08/2014
Dénomination du médicament
APROKAM 50 mg, poudre pour solution injectable
Céfuroxime
Encadré
Veuillez lire attentivement l'intégralité de cette notice avant dutiliser ce médicament.
· Gardez cette notice, vous pourriez avoir besoin de la relire.
· Si vous avez toute autre question, si vous avez un doute, demandez plus dinformations à votre médecin ou à votre pharmacien ou infirmière.
· Ce médicament vous a été personnellement prescrit. Ne le donnez jamais à quelquun dautre, même en cas de symptômes identiques, cela pourrait lui être nocif.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice.
Sommaire notice
Dans cette notice :
1. Qu'est-ce que APROKAM 50 mg, poudre pour solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser APROKAM 50 mg, poudre pour solution injectable?
3. Comment utiliser APROKAM 50 mg, poudre pour solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver APROKAM 50 mg, poudre pour solution injectable ?
6. Informations supplémentaires.
1. QUEST-CE QUE APROKAM 50 mg, poudre pour solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique
APROKAM 50 mg poudre pour solution injectable contient une substance active, la céfuroxime (sous forme de céfuroxime sodique), qui appartient au groupe dantibiotiques appelé les céphalosporines. Les antibiotiques sont utilisés pour tuer les bactéries ou « germes » responsables des infections.
Indications thérapeutiques
· Ce médicament sera utilisé si vous allez subir une intervention chirurgicale de lil pour cataracte (opacification du cristallin).
· Votre chirurgien ophtalmologiste vous administra ce médicament par injection dans lil à la fin de lintervention chirurgicale de la cataracte, afin de prévenir une infection de lil.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DUTILISER APROKAM 50 mg, poudre pour solution injectable ?
Liste des informations nécessaires avant la prise du médicament
Sans objet.
Contre-indications
Nutilisez jamais APROKAM :
· si vous êtes allergique (hypersensible) à la céfuroxime ou à tout autre antibiotique du groupe des céphalosporines.
Précautions d'emploi ; mises en garde spéciales
Faites attention avec APROKAM :
Prévenez votre médecin ou pharmacien ou infirmier/ère avant que ne soit utilisé APROKAM :
· si vous êtes allergique à dautres antibiotiques comme la pénicilline.
· si vous présentez un risque dinfection due à une bactérie appelée Staphylococcus aureus résistant à la méticilline.
· si vous présentez un risque davoir une infection qui peut être sévère.
· sil vous a été diagnostiqué une cataracte compliquée.
· si une autre chirurgie de lil est planifiée en même temps que celle pour votre cataracte.
· si vous avez une maladie grave de la thyroïde.
APROKAM est uniquement administré par injection dans lil (injection intra-camérulaire).
APROKAM doit être administré dans les conditions aseptiques recommandées pour la chirurgie de la cataracte (cela veut dire dans un environnement propre et sans germe).
Un flacon dAPROKAM doit être utilisé pour un seul patient.
Interactions avec d'autres médicaments
Utilisation d'autres médicaments
Informez votre médecin ou pharmacien si vous prenez ou avez récemment pris tout autre médicament.
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Grossesse et allaitement
· Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez de lêtre, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
· APROKAM vous sera administré uniquement si les bénéfices sont supérieurs aux risques potentiels.
Sportifs
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Sans objet.
Liste des excipients à effet notoire
Sans objet.
3. COMMENT UTILISER APROKAM 50 mg, poudre pour solution injectable ?
Instructions pour un bon usage
· Les injections dAPROKAM seront réalisées par un chirurgien ophtalmologiste à la fin de la chirurgie de la cataracte.
· APROKAM est une poudre stérile qui doit être dissoute dans une solution saline pour injection avant dêtre administrée.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
Sans objet.
Symptômes et instructions en cas de surdosage
Si vous avez utilisé plus de APROKAM que vous nauriez dû :
Dune façon générale, ce traitement sera administré par un professionnel de santé. Si vous pensez avoir reçu trop de produit, parlez-en à votre médecin ou à votre infirmier/ère.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
Instructions en cas d'omission d'une ou de plusieurs doses
Si vous oubliez dutiliser APROKAM 50 mg, poudre pour solution injectable :
Dune façon générale, ce traitement sera administré par un professionnel de santé. Si vous pensez que la dose a été oubliée, parlez-en à votre médecin ou à votre infirmier/ère.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
Risque de syndrome de sevrage
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Comme tous les médicaments, APROKAM est susceptible d'avoir des effets indésirables, bien que tout le monde ny soit pas sujet.
Leffet indésirable suivant est très rare (affectant moins de 1 patient sur 10 000) :
· Réaction allergique sévère pouvant occasionner des difficultés à respirer ou provoquer des vertiges.
Si vous présentez nimporte quel effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère, y compris si leffet indésirable nest pas mentionné dans cette notice.
5. COMMENT CONSERVER APROKAM 50 mg, poudre pour solution injectable ?
Tenir hors de la portée et de la vue des enfants.
Date de péremption
Ne pas utiliser APROKAM après la date de péremption mentionnée sur la boîte et létiquette du flacon après EXP. La date dexpiration fait référence au dernier jour du mois.
Conditions de conservation
A conserver à une température ne dépassant pas 25°C. Conserver le flacon dans lemballage extérieur à labri de la lumière.
Pour usage unique seulement.
Après reconstitution : le produit doit être utilisé immédiatement.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
Les médicaments ne doivent pas être jetés au tout à légout ou avec les ordures ménagères. Demandez à votre pharmacien ce quil faut faire des médicaments inutilisés. Ces mesures permettront de protéger lenvironnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Que contient APROKAM ?
La substance active est : la céfuroxime (sous forme de céfuroxime sodique).
Chaque flacon contient 50 mg de céfuroxime.
Après reconstitution, 0,1 ml de solution contient 1 mg de céfuroxime.
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose, c'est-à-dire est considéré « sans sodium ».
Il ny a pas dautres composants.
Forme pharmaceutique et contenu
Quest ce quAPROKAM et contenu de lemballage extérieur ?
APROKAM est une poudre pour solution injectable, la poudre est blanche à presque blanche et est fournie dans un flacon en verre.
Chaque boite contient un ou dix ou vingt flacons. Toutes les présentations peuvent ne pas être commercialisées.
Nom et adresse du titulaire de l'autorisation de mise sur le marché et du titulaire de l'autorisation de fabrication responsable de la libération des lots, si différent
Titulaire
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Exploitant
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Fabricant
BIOPHARMA S.R.L.
VIA DELLE GERBERE, 22/30 (LOC. S. PALOMBA)
00134 ROMA (RM)
ITALIE
ou
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants :
Conformément à la réglementation en vigueur.
Date dapprobation de la notice
La dernière date à laquelle cette notice a été approuvée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet.
Informations Internet
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lAnsm (France).
Informations réservées aux professionnels de santé
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
Incompatibilité
Aucune incompatibilité avec les produits utilisés le plus couramment dans la chirurgie de la cataracte na été rapportée dans la littérature.
Ce médicament ne doit pas être mélangé avec dautres médicaments à lexception de ceux mentionnés ci-dessous [solution pour injection de chlorure de sodium 9 mg/ml (0,9%)].
Comment préparer et administrer APROKAM
Flacon à usage unique seulement pour administration par voie intra-camérulaire.
APROKAM doit être administré, après reconstitution, par injection intra-oculaire dans la chambre antérieure de lil (injection intra-camérulaire), par un chirurgien ophtalmologiste, dans les conditions dasepsie recommandées pour la chirurgie de la cataracte.
La solution reconstituée doit être inspectée visuellement et doit être utilisée uniquement si elle est incolore à jaunâtre et sans particule visible.
Le produit doit être utilisé immédiatement après reconstitution et ne doit pas être ré-utilisé.
|
La dose recommandée de céfuroxime est de 1 mg dans 0,1 ml de solution pour injection de chlorure de sodium 9 mg/ml (0,9%).
NE PAS INJECTER UNE DOSE SUPERIEURE A CELLE RECOMMANDEE
|
Flacon pour usage unique seulement.
Utiliser un flacon pour un patient seulement. Coller létiquette drapeau du flacon dans le dossier patient.
|
Pour préparer le produit pour ladministration intra-camérulaire, veuillez suivre de façon stricte les instructions suivantes :
|
|

Doit être désinfecté
|
1. Vérifier lintégrité de la capsule flip-off avant de la retirer.
|
|

|
2. Désinfecter la partie extérieure du bouchon en caoutchouc du flacon avant de passer à létape 3.
|
|
|
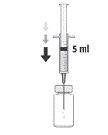
3. Injecter de façon aseptique dans le flacon, 5 ml de solution pour injection de chlorure de sodium 9 mg/ml (0,9%), en utilisant une aiguille stérile.
|
|
|
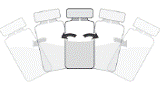
4. Secouer doucement le flacon jusquà ce que la solution soit sans particule visible.
|
|
|
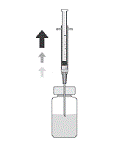
5. A laide dune seringue stérile de 1 ml, aspirer de façon aseptique au moins 0,1 ml de solution.
|
|
|
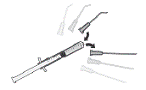
6. Déconnecter laiguille de la seringue et assembler la seringue avec une canule stérile appropriée pour la chambre antérieure.
|
|
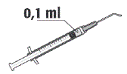
|
7. Expulser doucement lair de la seringue et ajuster la dose à la marque 0,1 ml de la seringue. La seringue est prête pour linjection.
|
|
Après utilisation, jeter la solution reconstituée restante. Ne pas la garder pour une utilisation ultérieure.
|
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Autres
Sans objet.