ANSM - Mis à jour le : 04/08/2014
MINIRIN 0,1 mg/ml, solution pour administration endonasale
Acétate de desmopressine
Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
· Gardez cette notice, vous pourriez avoir besoin de la relire.
· Si vous avez toute autre question, si vous avez un doute, demandez plus d'informations à votre médecin ou à votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez jamais à quelqu'un d'autre, même en cas de symptômes identiques, cela pourrait lui être nocif.
· Si l'un des effets indésirables devient grave ou si vous remarquez un effet indésirable non mentionné dans cette notice, parlez-en à votre médecin ou à votre pharmacien.
Dans cette notice :
1. QU'EST-CE QUE MINIRIN 0,1 mg/ml, solution pour administration endonasale ET DANS QUELS CAS EST-IL UTILISE ?
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D'UTILISER MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
3. COMMENT UTILISER MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
5. COMMENT CONSERVER MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
6. INFORMATIONS SUPPLEMENTAIRES
HORMONE ANTIDIURETIQUE
· Traitement du diabète d'origine centrale pitresso-sensible (maladie due à un déficit en hormone antidiurétique, ce qui entraîne l'émission d'une quantité anormalement abondante d'urine et une soif intense et permanente).
· Etude du pouvoir de concentration du rein.
Liste des informations nécessaires avant la prise du médicament
Sans objet.
N'utilisez jamais MINIRIN 0,1 mg/ml, solution pour administration endonasale dans les cas suivants:
· allergie connue à ce médicament,
· insuffisance cardiaque,
· maladie nécessitant un traitement par les diurétiques,
· insuffisance rénale modérée ou sévère,
· hyponatrémie (diminution de la concentration de sodium dans le sang),
· syndrôme de sécrétion inappropriée d'hormone anti-diurétique,
· polydypsie (soif excessive) ou potomanie (avec production d'urine excessive),
· maladies empêchant l'utilisation correcte du dispositif telles que: confusion mentale sévère, démence, certaines maladies neurologiques,
· traitement de l'énurésie nocturne et de la nycturie où seules les formes orales sont indiquées.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Précautions d'emploi ; mises en garde spéciales
Faites attention avec MINIRIN 0,1 mg/ml, solution pour administration endonasale:
Mises en garde spéciales
Adapter la posologie chez les jeunes enfants et les personnes âgées pour éviter tout risque d'intoxication par l'eau.
Respectez strictement les doses prescrites par votre médecin.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Précautions d'emploi
|
La prise de ce médicament est associée à un risque de rétention d'eau excessi ve pouvant se traduire par des maux de tête, un manque d'appétit, des nausées, des vomissements, une prise de poids rapide, un état confusionnel, voire des convulsions. Si vous constatez ces symptômes, le traitement doit être diminué, voire suspendu quelques heures, et les apports hydriques restreints. Contactez votre médecin rapidement. |
Il est recommandé de respecter un intervalle de 12 heures entre chaque administration.
En cas d'infection intercurrente entraînant fièvre, vomissements, diarrhée, il faut avertir immédiatement votre médecin.
A forte dose, le médicament peut entraîner une légère élévation de la tension artérielle qui disparaît en diminuant les doses.
Prévenez votre médecin si vous présentez l'une des maladies suivantes:
· maladie des artères coronaires (vaisseaux sanguins nourrissant le cur) ou hypertension artérielle,
· maladie de la thyroïde ou de la glande surrénale,
· mucoviscidose.
Chez l'enfant, l'administration doit être réalisée sous la surveillance d'un adulte.
NE JAMAIS LAISSEZ A LA PORTEE DES ENFANTS.
EN CAS DE DOUTE, NE PAS HESITER A DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Interactions avec d'autres médicaments
Prise ou utilisation d'autres médicaments
Si vous prenez ou avez pris récemment un autre médicament, y compris un médicament obtenu sans ordonnance, parlez-en à votre médecin ou à votre pharmacien.
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Grossesse - Allaitement
Ce médicament ne sera utilisé pendant la grossesse ou l'allaitement que sur les conseils de votre médecin. Si vous découvrez que vous êtes enceinte pendant le traitement, consultez votre médecin.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Sans objet.
Liste des excipients à effet notoire
Sans objet.
3. COMMENT UTILISER MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
Instructions pour un bon usage
Sans objet.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
Il sagit dune préparation pour administration par voie endonasale seulement.
1- Dans le traitement du diabète insipide pitresso-sensible, la posologie doit être ajustée à chaque cas.
Les posologies usuelles sont :
— nourrissons : 0,05 à 0,1 ml dune solution diluée au 10ème par votre pharmacien (0,5 à 1 µg),
— enfants : 0,05 à 0,1 ml (5 à 10 µg) 1 à 2 fois par jour,
— adultes : 0,1 à 0,2 ml (10 à 20 µg) 1 à 2 fois par jour.
Dans certains cas des doses plus faibles peuvent être prescrites.
2- Etude du pouvoir de concentration du rein
— 0,1 ml (10 µg) si le poids est inférieur à 10 kg,
— 0,2 ml (20 µg) si le poids est compris entre 10 et 30 kg,
— 0,3 ml (30 µg) si le poids est compris entre 30 et 50 kg,
— 0,4 ml (40 µg) si le poids est supérieur à 50 kg.
La prise de liquide doit être limitée pendant les 12 heures suivant ladministration du médicament.
Mode et voie dadministration[1]
Ce médicament est utilisé par voie endonasale uniquement.
Veuillez respecter les recommandations suivantes pour utiliser ce médicament. Si vous avez le moindre doute,
demandez conseil à votre médecin ou à votre pharmacien.

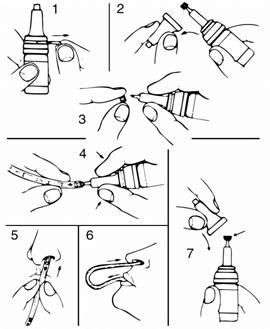
Tirez sur la languette puis enlevez le capuchon de protection du flacon (schémas 1 et 2).
Cassez lextrémité supérieure de lembout compte-gouttes et conservez-la (schéma 3).
Prenez le tube et fixez lextrémité portant une flèche sur lembout compte-gouttes du flacon. Orientez lautre extrémité du tube vers le haut, en le courbant légèrement avec la main. Inclinez ensuite la tête du flacon vers le bas et pressez lembout compte-gouttes du flacon afin de remplir le tube jusquà la graduation désirée. La graduation non numérotée entre lextrémité du tube et la graduation 0,05ml correspond à environ 0,025ml (schéma 4).
Positionnez le flacon à lhorizontale. Saisissez le tube entre le pouce et lindex, avec lautre main, à environ un centimètre de lembout compte-gouttes puis détachez le tube du flacon, tout en conservant lemplacement de vos doigts sur le tube. Afin déviter la formation de bulles, maintenez une pression constante sur lembout compte-gouttes jusquau moment de la séparation du flacon et du tube (schéma 4).
Introduire lextrémité du tube portant une flèche dans le nez jusquà ce que le bout des doigts touche la narine (schéma 5).
Placez lautre extrémité du tube dans la bouche. Retenez votre respiration. Renversez la tête en arrière, puis soufflez fortement et brièvement dans le tube, par la bouche, de façon à ce que la solution atteigne la cavité nasale, sans passer dans la gorge (schéma 6).
Après usage, fermez lembout compte-gouttes et remettez le capuchon. Nettoyez le tube à leau et faites le sécher (schéma 7).
Si le tube savère difficile à remplir, on peut utiliser une seringue à insuline pour prélever la dose voulue et linjecter dans le tube.
Fréquence dadministration
Se conformer strictement à la prescription de votre médecin.
Durée du traitement
Se conformer strictement à la prescription de votre médecin.
Symptômes et instructions en cas de surdosage
Si vous avez pris plus de MINIRIN 0,1 mg/ml, solution pour administration endonasale que vous n'auriez dû:
Un surdosage en desmopressine peut favoriser une intoxication par l'eau se manifestant par des maux de tête, un manque d'appétit, des nausées, des vomissements, une prise de poids rapide, un état confusionnel, voire des convulsions.
Si vous constatez ces symptômes, le traitement doit être diminué, voire suspendu quelques heures, et les apports hydriques restreints.
Vous devez contacter rapidement votre médecin.
Instructions en cas d'omission d'une ou de plusieurs doses
Si vous oubliez de prendre MINIRIN 0,1 mg/ml, solution pour administration endonasale:
NE PRENEZ PAS DE DOSE DOUBLE POUR COMPENSER LA DOSE QUE VOUS AVEZ OUBLIE DE PRENDRE.
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Ont été fréquemment décrits les effets suivants: maux de tête, nausées, douleurs abdominales, et congestion nasale;
Plus rarement ont été observés : vomissements, prise de poids rapide, état confusionnel, convulsions, hyponatrémie.
Ces symptômes peuvent traduire une rétention d'eau plus ou moins importante, ils s'observent en général avec des doses élevées de desmopresssine et disparaissent lorsque la posologie est diminuée. En cas de survenue de ces symptômes, prévenez rapidement votre médecin afin qu'il prenne les mesures nécessaires adaptées à votre cas (Voir également Mises en garde).
Ce médicament contient du chlorobutanol pouvant provoquer une réaction allergique.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou, votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via lAgence nationale de sécurité du médicament et des produits de santé (Ansm) et le réseau des Centres Régionaux de Pharmacovigilance. Site internet : www.ansm.sante.fr. En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
Tenir hors de la portée et de la vue des enfants.
Ne pas utiliser MINIRIN 0,1 mg/ml, solution pour administration endonasale après la date de péremption mentionnée sur la boîte.
Ce médicament doit être conservé à une température comprise entre 2°C et 8°C (au réfrigérateur) et à l'abri de la lumière.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
Les médicaments ne doivent pas être jetés au tout à l'égout ou avec les ordures ménagères. Demandez à votre pharmacien ce qu'il faut faire des médicaments inutilisés. Ces mesures permettront de protéger l'environnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Que contient MINIRIN 0,1 mg/ml, solution pour administration endonasale ?
La substance active est:
Acétate de desmopressine trihydraté ............................................................................................. 0,100 mg
Pour 1 ml.
Les autres composants sont:
Chlorure de sodium, chlorobutanol, acide chlorhydrique, eau purifiée.
Forme pharmaceutique et contenu
Qu'est-ce que MINIRIN 0,1 mg/ml, solution pour administration endonasale et contenu de l'emballage extérieur ?
Ce médicament se présente sous forme de solution pour administration endonasale.
Flacon de 2,5 ml.
FERRING SAS
7, RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
FERRING S.A.S
7, RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
WITTLAND 11
24109 KIEL
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
Date dapprobation de la notice
La dernière date à laquelle cette notice a été approuvée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lAfssaps (France).
Informations réservées aux professionnels de santé
Sans objet.
Sans objet.
[1] Le texte modifié tient compte du test de lisibilité déposé avec le renouvellement en 2009. Surligné en bleu.
Le texte surligné en jaune concerne la modification générée par le changement du dispositif dadministration.