NOTICE
ANSM - Mis à jour le : 28/08/2015
Dénomination du médicament
FLUARIX, suspension injectable en seringue préremplie
Vaccin grippal inactivé à virion fragmenté
Encadré
Veuillez lire attentivement cette notice avant que vous ou votre enfant ne receviez ce vaccin car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit à vous ou à votre enfant. Ne le donnez pas à dautres personnes.
· Si vous ou votre enfant ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
Sommaire notice
Que contient cette notice ?
1. Qu'est-ce que FLUARIX et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant dutiliser FLUARIX ?
3. Comment utiliser FLUARIX ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FLUARIX ?
6. Informations supplémentaires.
1. QUEST-CE QUE FLUARIX ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique
Sans objet.
Indications thérapeutiques
FLUARIX est un vaccin. Ce vaccin vous aide, vous ou votre enfant, à vous protéger contre la grippe, en particulier si vous ou votre enfant présentez un risque élevé de complications associées. FLUARIX doit être utilisé selon les recommandations officielles.
Lorsquune personne reçoit le vaccin FLUARIX, le système immunitaire (le système de défense naturelle de lorganisme) développe sa propre protection (anticorps) contre la maladie. Aucun des composants contenus dans le vaccin ne peut provoquer la grippe.
La grippe est une maladie qui peut se propager rapidement et qui est causée par différentes souches de virus qui peuvent changer chaque année. Cest pourquoi, vous ou votre enfant pouvez avoir besoin dêtre vacciné chaque année. Le plus grand risque de contracter la grippe se situe pendant les mois les plus froids, entre octobre et mars. Si vous ou votre enfant navez pas été vacciné durant lautomne, il est encore possible de lêtre jusquau printemps car vous ou votre enfant courrez le risque de contracter la grippe jusquà cette période. Votre médecin vous recommandera le meilleur moment pour vous faire vacciner.
FLUARIX vous protègera, vous ou votre enfant, contre les trois souches contenues dans le vaccin environ 2 à 3 semaines après linjection.
La période dincubation de la grippe est de quelques jours ; ainsi, si vous ou votre enfant êtes exposé à la grippe juste avant ou juste après la vaccination, vous ou votre enfant pouvez encore développer la maladie.
Le vaccin ne protégera ni vous ni votre enfant contre un rhume même si certains des symptômes sont similaires à ceux de la grippe.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DUTILISER FLUARIX ?
Liste des informations nécessaires avant la prise du médicament
Pour être certain que FLUARIX vous est adapté ou est adapté à votre enfant, il est important dindiquer à votre médecin si lun des points ci-dessous vous concerne, vous ou votre enfant. Si vous ne comprenez pas quelque chose, demandez à votre médecin ou à votre pharmacien de vous lexpliquer.
Contre-indications
Nutilisez jamais FLUARIX
· si vous ou votre enfant êtes allergique aux substances actives ou à lun des autres composants contenus dans ce médicament (mentionné dans la rubrique 6) ou à tout composant pouvant être présent en très faible quantité tel que des ufs (protéines de poulet, ovalbumine), formaldéhyde, sulfate de gentamicine ou désoxycholate de sodium.
· si vous ou votre enfant avez une maladie avec une température élevée ou une infection aiguë, la vaccination doit être différée après la guérison.
Précautions d'emploi ; mises en garde spéciales
Avertissements et précautions
Adressez-vous à votre médecin ou votre pharmacien avant que vous ou votre enfant ne receviez FLUARIX
· si vous ou votre enfant avez un système immunitaire affaibli (immunodéficience ou prise de médicaments affectant le système immunitaire)
· si, pour quelque raison que ce soit, vous ou votre enfant devez faire une analyse de sang dans les jours qui suivent la vaccination grippale. En effet des tests sanguins faussement positifs ont été observés chez certains patients ayant été récemment vaccinés.
Un évanouissement peut survenir (surtout chez les adolescents) après, voire même avant, toute injection avec une aiguille. Aussi parlez-en à votre médecin ou infirmier(e) si vous ou votre enfant vous êtes évanoui lors dune précédente injection.
Comme pour tous les vaccins, FLUARIX peut ne pas protéger complètement toutes les personnes vaccinées.
Interactions avec d'autres médicaments
Autres médicaments et FLUARIX
Informez votre médecin ou votre pharmacien si vous ou votre enfant prenez ou avez pris récemment ou pourriez prendre tout autre médicament.
FLUARIX peut être administré en même temps que dautres vaccins mais sur des membres différents. Dans ce cas, les effets indésirables pourront être intensifiés.
La réponse immunologique peut être diminuée en cas de traitement par immunosuppresseurs tels que les corticostéroïdes, les médicaments cytotoxiques ou la radiothérapie.
Interactions avec les aliments et les boissons
Sans objet.
Interactions avec les produits de phytothérapie ou thérapies alternatives
Sans objet.
Utilisation pendant la grossesse et l'allaitement
Grossesse, allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Les vaccins grippaux inactivés peuvent être utilisés à tous les stades de la grossesse. Les données de sécurité disponibles sont plus importantes pour le deuxième et le troisième trimestre de la grossesse que pour le premier trimestre. Cependant, les données dutilisation des vaccins grippaux inactivés dans le monde nindiquent pas dissues anormales pour le ftus et la mère, attribuables au vaccin.
FLUARIX peut être administré en cas dallaitement.
Votre médecin ou votre pharmacien sera en mesure de décider si vous pouvez être vaccinée par FLUARIX. Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Sportifs
Sans objet.
Effets sur l'aptitude à conduire des véhicules ou à utiliser des machines
Conduite de véhicules et utilisation de machines
FLUARIX na aucun effet ou quun effet négligeable sur laptitude à conduire des véhicules et à utiliser des machines.
Liste des excipients à effet notoire
Fluarix contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c'est-à-dire quil est quasiment sans sodium.
Fluarix contient du potassium
Ce médicament contient moins de 1 mmol (39 mg) de potassium par dose, c'est-à-dire quil est quasiment sans potassium.
Fluarix contient de léthanol
Ce médicament contient de petites quantités déthanol (alcool), inférieures à 100 mg par dose.
3. COMMENT UTILISER FLUARIX ?
Instructions pour un bon usage
Sans objet.
Posologie, Mode et/ou voie(s) d'administration, Fréquence d'administration et Durée du traitement
Posologie
Les adultes recevront une dose de 0,5 ml.
Utilisation chez lenfant :
Les enfants à partir de 36 mois recevront une dose de 0,5 ml.
Les enfants de 6 mois à 35 mois peuvent recevoir soit une dose de 0,25 ml, soit une dose de 0,5 ml, selon les recommandations nationales en vigueur.
Si votre enfant a moins de 9 ans et n'a pas été vacciné auparavant contre la grippe, une seconde dose devra être injectée après un intervalle dau moins 4 semaines.
Mode dadministration
Votre médecin administrera la dose recommandée de vaccin par une injection dans le muscle ou profondément sous la peau.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin ou à votre pharmacien.
Symptômes et instructions en cas de surdosage
Sans objet.
Instructions en cas d'omission d'une ou de plusieurs doses
Sans objet.
Risque de syndrome de sevrage
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Description des effets indésirables
Comme tous les médicaments, ce vaccin peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Au cours des essais cliniques, les effets indésirables fréquents suivants (rapportés chez plus d1 personne sur 100 mais chez moins d1 personne sur 10) ont été observés :
· maux de tête,
· sueurs,
· douleurs musculaires (myalgies), douleurs articulaires (arthralgies),
· fièvre, sensation générale de malaise, frissons, fatigue,
· réactions locales : rougeur, gonflement, douleur, bleu (ecchymose), dureté (induration) autour de la zone où le vaccin a été injecté.
Ces réactions disparaissent généralement sans traitement en 1 ou 2 jours.
Les effets indésirables suivants ont été rapportés au cours dessais cliniques chez des enfants et adolescents âgés de 6 mois à 17 ans :
Très fréquent (pouvant survenir pour plus d'1 dose de vaccin sur 10) :
· irritabilité2,
· perte d'appétit2,
· somnolence2,
· maux de tête3,
· douleurs articulaires3,
· douleurs musculaires3,
· fièvre2,
· fatigue3,
· réactions locales : rougeur1, gonflement1, douleur1.
Fréquent (pouvant survenir jusquà 1 dose de vaccin sur 10) :
· symptômes gastro-intestinaux3,
· frissons3,
· fièvre3.
1rapporté chez les enfants âgés de 6 mois à 17 ans
2rapporté chez les enfants âgés de 6 mois à <6 ans
3rapporté chez les enfants âgés de 6 ans à 17 ans
En plus des effets indésirables fréquents mentionnés ci-dessus, les effets indésirables suivants sont survenus après la mise sur le marché du vaccin :
· réactions allergiques :
o écoulement au niveau des yeux avec démangeaisons et croutes au niveau des paupières (conjonctivite),
o conduisant dans de rares cas à une urgence médicale avec un système circulatoire ne permettant pas de maintenir une circulation sanguine suffisante au niveau des différents organes (choc),
o gonflement situé préférentiellement au niveau de la tête et du cou incluant le visage, les lèvres, la langue, la gorge ou d'autres parties du corps (angidème) dans de très rares cas,
· réactions cutanées qui peuvent sétendre sur tout le corps incluant démangeaisons (prurit, urticaire), éruption,
· inflammation des vaisseaux (vascularite) pouvant se traduire par des éruptions cutanées et dans de très rares cas par des problèmes rénaux transitoires,
· douleur siégeant sur le trajet du nerf (névralgie), anomalies de la perception des sensations de toucher, de douleur, de chaud et de froid (paresthésie), convulsions associées à de la fièvre, troubles neurologiques pouvant se traduire par une raideur du cou, de la confusion, des engourdissements, des douleurs et une faiblesse des membres, une perte de léquilibre, une perte des réflexes, une paralysie dune partie ou de tout le corps (encéphalomyélite, névrite et syndrome de Guillain-Barré),
· diminution temporaire du nombre de certains éléments du sang appelés plaquettes ; un faible nombre de celles-ci peut se traduire par des bleus ou saignements excessifs (thrombocytopénie transitoire),
· gonflement transitoire des glandes du cou, des aisselles ou de l'aine (lymphadénopathie transitoire).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des centres régionaux de Pharmacovigilance Site internet : www.ansm.sante.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament
5. COMMENT CONSERVER FLUARIX ?
Tenir ce vaccin hors de la vue et de la portée des enfants.
Date de péremption
Nutilisez pas ce vaccin après la date de péremption mentionnée sur lemballage extérieur après le terme EXP. La date dexpiration fait référence au dernier jour de ce mois.
Conditions de conservation
A conserver au réfrigérateur (entre 2°C et 8°C).
Ne pas congeler.
Conserver la seringue dans lemballage extérieur, à labri de la lumière.
Si nécessaire, mises en garde contre certains signes visibles de détérioration
Ne jetez aucun médicament au tout-à-légout ni avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. INFORMATIONS SUPPLEMENTAIRES
Liste complète des substances actives et des excipients
Ce que contient FLUARIX
Les substances actives sont les virus de la grippe (inactivé, fragmenté) des souches suivantes* :
A/California/7/2009 (H1N1) pdm09 - souche analogue (A/Christchurch/16/2010, NIB-74xp) 15 microgrammes HA**
A/Switzerland/9715293/2013 (H3N2) - souche analogue (A/Switzerland/9715293/2013, NIB-88) 15 microgrammes HA**
B/Phuket/3073/2013
15 microgrammes HA**
Pour une dose de 0,5 ml.
*Cultivées sur ufs embryonnés de poules provenant délevages sains.
**Hémagglutinine.
Ce vaccin est conforme aux recommandations de lOrganisation Mondiale de la Santé (OMS) (dans lHémisphère Nord) et à la recommandation de lUnion Européenne pour la saison 2015/2016.
Les autres composants sont du chlorure de sodium, du phosphate disodique dodécahydraté, du phosphate monopotassique, du chlorure de potassium, du chlorure de magnésium hexahydraté, de lhydrogénosuccinate dalpha tocophéryle, du polysorbate 80, de loctoxinol 10 et de leau pour préparations injectables.
Forme pharmaceutique et contenu
Aspect de FLUARIX et contenu de lemballage extérieur
FLUARIX est une suspension injectable en seringue préremplie avec aiguille sertie, avec aiguille séparée ou sans aiguille (0,5 ml) :
· avec aiguille sertie : boîte de 1, de 10 ou de 20
· avec 1 aiguille séparée : boîte de 1, de 10 ou de 20
· avec 2 aiguilles séparées : boîte de 1
· sans aiguille : boîte de 1, de 10 ou de 20
Toutes les présentations peuvent ne pas être commercialisées.
Nom et adresse du titulaire de l'autorisation de mise sur le marché et du titulaire de l'autorisation de fabrication responsable de la libération des lots, si différent
Titulaire de lautorisation de mise sur le marché et fabricant
Titulaire
LABORATOIRE GLAXOSMITHKLINE
100, ROUTE DE VERSAILLES
78163 MARLY-LE-ROI CEDEX
Exploitant
LABORATOIRE GLAXOSMITHKLINE
100, ROUTE DE VERSAILLES
78163 MARLY-LE-ROI CEDEX
Fabricant
GLAXOSMITHKLINE BIOLOGICALS
BRANCH OF GLAXOSMITHKLINE BEECHAM PHARMA GMBH & CO. KG
ZIRKUSSTRASSE 40
D-01069 DRESDEN
Allemagne
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Conformément à la réglementation en vigueur.
Date dapprobation de la notice
La dernière date à laquelle cette notice a été révisée est le {date}.
AMM sous circonstances exceptionnelles
Sans objet.
Informations Internet
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).
Informations réservées aux professionnels de santé
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
Comme pour tous les vaccins injectables, il est recommandé de disposer d'un traitement médical approprié et de surveiller le sujet en cas de réaction anaphylactique suite à ladministration du vaccin.
FLUARIX doit être administré par voie intramusculaire ou par voie sous-cutanée profonde.
FLUARIX ne doit en aucun cas être administré par voie intravasculaire.
FLUARIX peut être administré en même temps que dautres vaccins. Les injections doivent être pratiquées sur des membres différents.
Le vaccin doit être amené à température ambiante avant utilisation.
Agiter avant emploi. Inspecter visuellement avant ladministration.
Lorsquune dose de 0,5 ml est indiquée, la totalité du contenu de la seringue doit être injecté.
Instructions pour ladministration de 0,25 ml de vaccin chez les enfants âgés de 6 à 35 mois.
|
Lorsqu'une dose de 0,25 ml est indiquée, la seringue préremplie doit être maintenue en position verticale et la moitié du volume doit être éliminée jusqu'à ce que le bouchon-piston atteigne la ligne marquée sur la seringue.
Pour les seringues non marquées par une ligne, le schéma 1 expliquera lutilisation de la dose de 0,25 ml. Alignez la seringue sur le schéma de telle manière que son bord supérieur corresponde à la flèche du haut. Poussez le piston jusquà atteindre la flèche du bas. Le volume restant de 0,25 ml doit être injecté.
|
Schéma 1
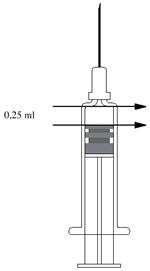
|
Instructions pour ladministration du vaccin présenté en seringue préremplie sans aiguille sertie
Pour fixer l'aiguille à la seringue, reportez-vous au schéma 2.

1. En tenant le corps de la seringue dune main (en évitant de tenir le piston), dévisser lembout protecteur de la seringue en le tournant dans le sens inverse des aiguilles dune montre.
2. Pour fixer laiguille sur la seringue, visser laiguille dans le sens des aiguilles dune montre sur la seringue jusquà sentir un blocage (voir schéma 2).
3. Enlever le protège aiguille, ce qui à loccasion peut être un peu difficile.
4. Administrer le vaccin.
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur
Autres
Sans objet.

