
ANSM - Mis à jour le : 13/01/2017
LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution
Latanoprost
Veuillez lire attentivement cette notice avant dutiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin, le médecin traitant votre enfant ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit ou pour votre enfant. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant dutiliser LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ?
3. Comment utiliser LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ?
6. Contenu de lemballage et autres informations.
Classe pharmacothérapeutique : ANTIGLAUCOMATEUX et MYOTIQUES, ANALOGUES DE PROSTAGLANDINES.
LATANOPROST PFIZER appartient à une famille de médicaments appelés analogues des prostaglandines. Il agit en augmentant le drainage du liquide intraoculaire vers le sang.
LATANOPROST PFIZER est indiqué chez les adultes atteints de glaucome à angle ouvert ou dhypertension intraoculaire. Ces deux pathologies sont liées à une pression élevée à lintérieur de lil (de vos yeux) risquant ainsi dendommager votre vue.
LATANOPROST PFIZER est aussi utilisé chez les enfants et les bébés atteints dhypertension intraoculaire ou de glaucome.
LATANOPROST PFIZER peut être utilisé chez ladulte (y compris le sujet âgé) et chez lenfant, de la naissance jusquà lâge de 18 ans. LATANOPROST PFIZER na pas été étudié chez les enfants nés avant terme (âge gestationnel inférieur à 36 semaines).
Nutilisez jamais LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution :
· si vous êtes allergique (hypersensible) au latanoprost ou à lun des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissement et précautions
Adressez-vous à votre médecin, au médecin traitant votre enfant ou à votre pharmacien avant de prendre LATANOPROST PFIZER ou avant de le donner à votre enfant, si certaines des situations ci-dessous correspondent à votre cas ou au cas de votre enfant :
· si vous ou votre enfant devez être opéré de lil ou lavez déjà été (y compris sil sagit dune opération de la cataracte).
· si vous ou votre enfant avez dautres problèmes oculaires (douleur au niveau de lil, irritation ou inflammation, vision trouble).
· si vous ou votre enfant souffrez dune sécheresse oculaire.
· si vous ou votre enfant présentez un asthme sévère ou mal contrôlé.
· si vous ou votre enfant portez des lentilles de contact. Vous pouvez utiliser LATANOPROST PFIZER, à condition de suivre les instructions mentionnées section 3 « COMMENT UTILISER LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ? ».
· si vous avez souffert ou souffrez actuellement dune infection virale de lil due au virus herpès simplex (HSV).
Enfants
Sans objet.
Autres médicaments et LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution
Si vous ou votre enfant prenez ou avez pris récemment un autre médicament, si vous prenez un autre collyre de la famille des prostaglandines ou même un médicament obtenu sans ordonnance, parlez-en à votre médecin, au médecin traitant votre enfant ou à votre pharmacien.
LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution avec des aliments et boissons
Sans objet.
Vous ne devez pas utiliser LATANOPROST PFIZER si vous êtes enceinte ou si vous allaitez.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre ce médicament.
Sportifs
Sans objet.
Conduite de véhicules et utilisation de machines
LATANOPROST PFIZER a une influence mineure ou modérée sur l'aptitude à conduire des véhicules et à utiliser des machines.
Comme pour les autres collyres, si vous avez des troubles transitoires de la vue après linstillation du produit, vous ne devez pas conduire de véhicule ou utiliser de machine jusquà ce que votre vision normale soit rétablie.
LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution contient un conservateur appelé chlorure de benzalkonium (0,2 mg/ml), qui peut être absorbé par les lentilles de contact souples et peut les teinter. Par conséquent, il faut éviter tout contact avec les lentilles de contact souples.
Si vous ou votre enfant portez des lentilles de contact, retirez-les avant instillation et remettez-les 15 minutes après linstillation.
Il a été rapporté que le chlorure de benzalkonium entraînait des irritations oculaires, des sécheresses oculaires et pouvait altérer la couche cornéenne. LATANOPROST PFIZER doit être utilisé avec précaution chez les patients présentant une sécheresse oculaire et les patients ayant une cornée abimée. Par ailleurs, ces patients doivent être surveillés en cas dutilisation prolongée.
Voir les instructions destinées aux porteurs de lentilles de contact en section 3.
3. COMMENT UTILISER LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ?
Veillez à toujours utiliser LATANOPROST PFIZER en suivant exactement les indications de votre médecin ou du médecin traitant votre enfant. Vérifiez auprès de votre médecin, du médecin traitant votre enfant ou de votre pharmacien en cas de doute.
La posologie indiquée chez ladulte (y compris chez le sujet âgé) et lenfant est dune goutte dans lil (les yeux) à traiter, une fois par jour, de préférence le soir.
Nutilisez pas LATANOPROST PFIZER plus dune fois par jour, votre traitement pourrait être moins efficace si vous lutilisez plus souvent.
Utilisez LATANOPROST PFIZER tel que vous la indiqué votre médecin ou le médecin traitant votre enfant jusquà ce quils vous demandent darrêter.
Porteurs de lentilles de contact
Si vous ou votre enfant portez des lentilles de contact, retirez-les avant dutiliser LATANOPROST PFIZER et remettez-les 15 minutes après linstillation.
Présentation avec bouchon à vis et capuchon protecteur en PE jetable
Suivez les étapes décrites ci-dessous destinées à faciliter lutilisation de LATANOPROST PFIZER :
1. Lavez-vous les mains, asseyez-vous ou installez-vous confortablement.
2. Otez le capuchon extérieur (que vous pouvez jeter).

3. Dévissez le capuchon interne et conservez-le.
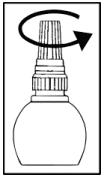
4. Avec vos doigts abaissez doucement la paupière inférieure de lil atteint.
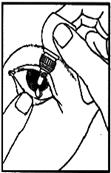
5. Placez le haut du flacon de lil atteint, sans le toucher.
6. Pressez légèrement le flacon afin de ne déposer quune seule goutte dans lil, puis relâchez la paupière inférieure.
7. Appuyez légèrement avec votre doigt sur le coin interne de lil atteint (proche du nez) pendant une minute pour favoriser le passage de LATANOPROST PFIZER dans lil.
8. Recommencez cette opération pour traiter votre deuxième il si votre médecin vous a indiqué de le faire.
9. Replacez le capuchon interne sur le flacon.
Présentation avec bouchon à vis et anneau de sécurité
Suivez les étapes décrites ci-dessous destinées à faciliter lutilisation de LATANOPROST PFIZER :
1. Lavez-vous les mains, asseyez-vous ou installez-vous confortablement.
2. Dévissez le capuchon et conservez-le.
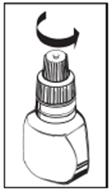
3. Avec vos doigts abaissez doucement la paupière inférieure de lil atteint.
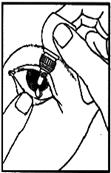
4. Approchez lembout du flacon de lil atteint, sans toucher lil.
5. Pressez légèrement le flacon afin de ne déposer quune seule goutte dans lil, puis relâchez la paupière inférieure.
6. Appuyez légèrement avec votre doigt sur le coin interne de lil atteint (proche du nez) pendant une minute pour favoriser le passage de LATANOPROST PFIZER dans lil.
7. Répétez cette procédure dans lautre il si cela vous a été prescrit par votre médecin.
8. Replacez le capuchon sur le flacon.
Si vous devez utiliser LATANOPROST PFIZER avec un autre collyre, attendez au moins cinq minutes entre linstillation de LATANOPROST PFIZER et celle dun autre collyre.
Si vous avez utilisé plus de LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution que vous nauriez dû :
En cas dinstillation excessive, une sensation dirritation peut apparaître et vos yeux peuvent larmoyer et devenir rouges, ceci devrait passer. Si vous êtes inquiet, parlez-en à votre médecin, au médecin traitant votre enfant ou à votre pharmacien.
En cas dingestion accidentelle de LATANOPROST PFIZER, contactez immédiatement votre médecin ou le médecin traitant votre enfant.
Si vous oubliez dutiliser LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution :
Attendez le moment de ladministration suivante, pour instiller votre collyre.
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
En cas de doute, parlez-en à votre médecin ou à votre pharmacien.
Si vous arrêtez dutiliser LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution :
Si vous désirez arrêter votre traitement, parlez-en à votre médecin ou au médecin traitant votre enfant.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus dinformations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Sont listés ci-dessous les effets indésirables connus avec lutilisation de LATANOPROST PFIZER :
Très fréquent (pouvant affecter plus de 1 patient sur 10) :
· Une modification de la couleur des yeux, par augmentation de la quantité de pigments bruns dans liris. Le changement de la couleur des yeux a surtout été observé chez des patients ayant liris de plusieurs couleurs (cest-à-dire vert-marron, jaune-marron, bleu-marron, ou encore gris-marron) plus que chez les patients ayant liris dune seule couleur (bleu, gris, vert ou brun). Cette modification de la couleur des yeux se fait très progressivement et survient en général dans les 8 premiers mois du traitement. Cette modification de couleur peut être définitive et peut être plus visible si vous nêtes traité que pour un seul il. Il ny a apparemment pas de problème associé à ce changement de couleur de lil. Le changement de la couleur de lil ne se poursuit pas après larrêt du traitement.
· Une rougeur au niveau de lil.
· Une irritation oculaire (sensation de brûlure, grain de sable, démangeaison, picotement ou sensation de corps étranger). Si lirritation est telle quelle fait larmoyer votre il de manière excessive, ou quelle vous amène à considérer larrêt de ce médicament, parlez-en à votre médecin, pharmacien ou infirmier/ère rapidement (dans la semaine). Vous aurez alors peut être besoin que votre traitement soit revu afin de sassurer quil reste adapté à votre état.
· Des modifications progressives des cils et du duvet autour de lil traité ont été majoritairement observées dans la population japonaise. Ces changements se traduisent par une couleur plus foncée, un épaississement, un allongement et une quantité plus importante de cils et de duvet.
Fréquent (pouvant affecter moins de 1 patient sur 10) :
· Une irritation ou une érosion de la surface oculaire.
· Une inflammation de la paupière (blépharite).
· Une douleur de lil,
· Une gêne visuelle à la lumière (photophobie).
Peu fréquent (pouvant affecter moins de 1 patient sur 100) :
· Un dème de la paupière.
· Une sécheresse oculaire.
· Une inflammation ou irritation de la surface oculaire (kératite).
· Une vision trouble.
· Une conjonctivite.
· Une éruption cutanée.
Rare (pouvant affecter moins de 1 patient sur 1000) :
· Une inflammation de liris, la partie colorée de lil (iritis/uvéite).
· Un gonflement de la rétine (dème maculaire).
· Un gonflement et des ulcérations de la surface oculaire.
· Un gonflement du pourtour de lil (dème périorbitaire).
· Des cils mal orientés ou une rangée supplémentaire de cils.
· Une réaction cutanée localisée aux paupières, une coloration plus foncée des paupières.
· De lasthme, ou une aggravation de lasthme et une gêne respiratoire (dyspnée).
Très rare (pouvant affecter moins de 1 patient sur 10000) :
· Des douleurs dans la poitrine ou une aggravation dune angine de poitrine préexistante, des yeux dapparence creuse (creusement du sillon palpéral).
Les effets suivants ont également été rapportés : kyste dans la partie colorée de lil (kyste irien), maux de tête, étourdissements, sensations désagréables de battements cardiaques (palpitations), douleur musculaire, douleur articulaire et développement dune infection virale de lil due au virus de lherpès simplex (HSV).
Les effets indésirables observés plus souvent chez lenfant que chez ladulte sont un rhume et de la fièvre.
Dans de très rares cas, certains patients présentant des lésions sévères au niveau de la couche claire située sur le devant de lil (la cornée) ont développé des taches troubles sur celle-ci du fait de laccumulation de calcium pendant le traitement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.ansm.sante.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
Nutilisez pas ce médicament après la date de péremption indiquée sur la boîte et le flacon compte-gouttes. La date de péremption fait référence au dernier jour de ce mois.
A conserver au réfrigérateur (entre 2°C et 8°C).
Conserver le flacon compte-gouttes dans lemballage extérieur, à labri de la lumière.
Après la 1ère ouverture, le flacon doit être conservé à une température ne dépassant pas 25°C et utilisé dans un délai de 4 semaines.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS
Ce que contient LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution
· La substance active est :
Latanoprost .................................................................................................... 50 microgrammes
Pour 1ml
2,5 ml de collyre en solution (contenu dans un flacon compte-gouttes) contient 125 microgrammes de latanoprost.
Une goutte contient environ 1,5 microgrammes de latanoprost.
· Les autres composants sont :
Chlorure de benzalkonium, chlorure de sodium, phosphate monosodique monohydraté (E339a) et phosphate disodique anhydre (E339b), eau pour préparations injectables.
LATANOPROST PFIZER 50 microgrammes/ml, collyre en solution est conditionné en boîtes de 1, 3 ou 6 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
Chaque boîte contient un flacon compte-gouttes. Chaque flacon compte-gouttes contient 2,5 ml de solution.
Titulaire de lautorisation de mise sur le marché
23-25, AVENUE DU DOCTEUR LANNELONGUE
75014 PARIS
Exploitant de lautorisation de mise sur le marché
PFIZER PFE FRANCE
23-25, AVENUE DU DOCTEUR LANNELONGUE
75014 PARIS
PFIZER MANUFACTURING BELGIUM NV
RIJKSWEG 12
2870 PUURS
BELGIQUE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous le seul nom suivant :
Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).