ANSM - Mis à jour le : 19/06/2017
Ventoline® 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose
Sulfate de salbutamol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser VENTOLINE 2,5 mg/2,5 ml solution pour inhalation par nébuliseur en récipient ?
3. Comment utiliser VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose?
6. Contenu de lemballage et autres informations.
Classe pharmacothérapeutique : BRONCHODILATATEUR BETA-2 MIMETIQUE A ACTION RAPIDE ET DE COURTE DUREE PAR VOIE INHALEE - code ATC : R03AC02
Ce médicament contient un bêta-2 mimétique : le salbutamol. Cest un bronchodilatateur (il augmente le calibre des bronches) à action rapide (en quelques minutes) et de courte durée qui sadministre par voie inhalée (en linspirant) à laide dun appareil pour nébulisation (un nébuliseur permettant de transformer certains liquides en un nuage de particules).
Lusage de ce médicament par ce mode dadministration doit être réservé au traitement des crises dasthme graves et des poussées aiguës au cours de la bronchite chronique obstructive (maladie chronique, invalidante qui se caractérise par une diminution progressive du souffle liée à une inflammation des bronches), lorsque ces situations nécessitent linhalation de fortes doses de salbutamol.
En fonction de la sévérité de votre asthme, votre médecin peut prescrire Ventoline seul ou en complément dun traitement de fond continu par un ou plusieurs autres médicaments, comme les corticoïdes par voie inhalée.
Si vous prenez déjà un autre médicament pour traiter votre asthme, votre médecin pourra en augmenter la posologie. Contacter votre médecin en cas dapparition de symptômes dasthme importants.
Nutilisez jamais VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose :
· Si vous êtes allergique au salbutamol (la substance active) ou à lun des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· En cas de risque davortement (par exemple un risque de fausse couche).
Ne renouvelez pas la prise de ce médicament si une augmentation de la gêne respiratoire survient à la suite de linhalation de ce produit, et contactez votre médecin.
En cas de doute, demandez lavis de votre médecin ou de votre pharmacien.
Avertissements et précautions
Faites attention avec ce médicament :
· Ce produit actif en inhalation, doit atteindre lextrémité des petites bronches. En cas dencombrement des voies respiratoires (par des mucosités abondantes) ou dinfection, son efficacité peut être diminuée. Consultez rapidement votre médecin afin quil mette en place un traitement plus adapté.
· Avant le début du traitement, prévenez votre médecin si vous souffrez des maladies suivantes afin quil détermine les modalités de prescription et de surveillance les plus adaptées à votre cas :
o maladie de la glande thyroïde,
o maladie cardio-vasculaire, notamment certains troubles du rythme cardiaque, angine de poitrine (douleurs violentes localisées au niveau de la poitrine et pouvant sétendre dans le bras gauche), ou hypertension artérielle (augmentation de la pression du sang dans les artères),
o diabète.
Adressez-vous à votre médecin ou pharmacien avant dutiliser VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose.
Enfants
Sans objet.
Autres médicaments et VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose
Informez votre médecin ou pharmacien si vous prenez, avez pris récemment ou pourriez prendre tout autre médicament, y compris un médicament obtenu sans ordonnance.
VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose avec des aliments et boissons
Sans objet.
Si vous respectez les conditions normales dutilisation, vous pouvez utiliser ce médicament pendant votre grossesse.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Sportifs
Attention, ce médicament contient un principe actif pouvant rendre positifs les tests pratiqués lors de contrôles antidopage.
Conduite de véhicules et utilisation de machines
Sans objet.
VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose contient {excipient}
Sans objet.
Posologie et fréquence dadministration
Respectez toujours la posologie indiquée par votre médecin. En cas de doute, consultez votre médecin ou votre pharmacien.
La posologie initiale de salbutamol recommandée par inhalation est de 2,5 mg, soit 1 unidose de 2,5 ml par nébulisation. Cette posologie peut être augmentée jusquà 5 mg, soit 2 unidoses de 2,5 ml par nébulisation.
Chez ladulte, des posologies plus élevées, allant jusquà 40 mg par jour, peuvent être données sous surveillance médicale stricte à lhôpital pour le traitement dune obstruction sévère des voies aériennes.
Chez lenfant et le nourrisson :
50 à 150 microgrammes de salbutamol par kilogramme de poids corporel (soit 0,05 à 0,15 ml/kg de la solution à 2,5 mg/2,5 ml), sans dépasser généralement 5 mg de salbutamol par nébulisation (soit 2 unidoses de 2,5 mg/2,5 ml).
Pour les nourrissons âgés de moins de 18 mois, on ne dépassera pas 2,5 mg (soit 1 unidose de 2,5 ml par nébulisation pour le dosage 2,5 mg/2,5 ml).
Sous surveillance médicale, la nébulisation peut être renouvelée toutes les 20 à 30 minutes en fonction du résultat clinique et de la tolérance du traitement.
Mode dadministration
Ce médicament sinhale grâce à un appareil pour nébulisation appelé également nébuliseur (voie respiratoire exclusivement).
Ne linjectez pas. Ne lavalez pas.
Pour lutilisation et lentretien de lappareil de nébulisation, conformez-vous aux instructions délivrées par le fabricant de lappareil utilisé.
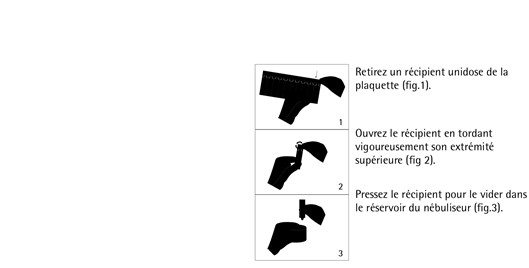
Mode demploi :
La solution est prête à lemploi, cependant si une dilution est nécessaire, elle doit être réalisée dans du sérum physiologique stérile.

Assemblez le nébuliseur pour ladministration selon les instructions du fabricant.
Évitez le contact des yeux avec laérosol généré par le nébuliseur.
Avec les appareils pneumatiques (dispositif utilisant notamment un compresseur dair), le débit dair ou doxygène destiné à pulser la solution sera adapté en fonction de létat du patient et des recommandations du fabricant de lappareil de nébulisation.
La nébulisation ne doit en général pas excéder 10 à 20 minutes.
La technique dutilisation par le patient doit être vérifiée régulièrement.
Après nébulisation, la solution inutilisée restant dans la cuve de lappareil doit être jetée. Le nettoyage et lentretien du matériel se feront selon les recommandations du fabricant.
Les récipients unidoses ne contiennent aucun conservateur, ils doivent être utilisés immédiatement après louverture.
Pour chaque nébulisation un nouveau récipient doit être utilisé. Le contenu des récipients unidoses partiellement ouverts ou endommagés ne doit pas être administré.
Si vous avez pris plus de VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose que vous nauriez dû
Si vous avez pris accidentellement une dose supérieure à la dose recommandée, vous pouvez présenter des effets indésirables tels que tachycardie (accélération du rythme cardiaque), maux de tête, tremblements ou agitation (voir la rubrique 4 : « Quels sont les effets indésirables éventuels ? »).
Consultez immédiatement votre médecin et emportez avec vous cette notice ou votre médicament afin que votre médecin sache ce que vous avez pris.
Si vous oubliez de prendre VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez de prendre VENTOLINE 2,5 mg/2,5 ml, solution pour inhalation par nébuliseur en récipient unidose
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Prévenez votre médecin si vous ressentez pendant le traitement une douleur thoracique (due à des problèmes cardiaques tels quune angine de poitrine), mais ninterrompez pas votre traitement sans avis médical.
En cas d'aggravation de votre gêne respiratoire (respiration sifflante) juste après la prise de ce médicament, cessez immédiatement de l'utiliser, et contactez votre médecin dès que possible.
Si disponible, utilisez, dès que possible un autre médicament daction rapide pour traiter votre asthme.
Peuvent être observés :
· Fréquemment :
o tremblements des extrémités (pieds et mains),
o augmentations du rythme cardiaque,
o maux de tête.
· Peu fréquemment :
o palpitations,
o irritations de la bouche ou de la gorge,
o crampes musculaires.
· Rarement :
o comme avec dautres produits inhalés, une toux ou une augmentation de la gêne respiratoire pourrait survenir à la suite de linhalation du produit. Dans ce cas, arrêtez le traitement et contactez votre médecin afin quil envisage un autre traitement.
· Très rarement :
o bouffées de chaleur, rougeurs sur la peau,
o nervosité, agitation,
o diminution du taux de potassium dans le sang,
o anomalies du rythme cardiaque
o augmentation du taux dacide lactique dans le sang*
o réactions allergiques telles que sensation doppression de la poitrine, démangeaisons, sifflement respiratoire, gonflement des paupières, du visage et/ou des lèvres et éruption cutanée, baisse de la tension artérielle pouvant aller jusquau malaise.
Des augmentations de la quantité de sucre dans le sang ont également été rapportées : cet effet régresse à larrêt du traitement.
* Cet effet survient le plus souvent chez les personnes ayant une maladie rénale sévère. Les
symptômes comprennent:
respiration rapide, essoufflement, même si vous ressentez une amélioration dans vos sifflements.
sensation de froid
douleurs à l'estomac, nausées et vomissements.
Contacter immédiatement votre médecin en cas dapparition de ces symptômes et arrêter de prendre Ventoline.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.ansm.sante.fr
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
Tenir ce médicament hors de la vue et de la portée des enfants.
Nutilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
Conservez le récipient unidose dans la boîte, à labri de la lumière, à une température ne dépassant pas +30°C.
Jetez le récipient unidose après utilisation.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS
· La substance active est le sulfate de salbutamol
Un récipient unidose en contient 3,00 mg (correspondant à 2,50 mg de salbutamol).
· Les autres composants sont :
chlorure de sodium, acide sulfurique dilué, eau pour préparations injectables.
Ce médicament se présente sous forme de solution pour inhalation par nébuliseur en récipient unidose.
Une boîte peut contenir 10, 20, 30 ou 60 récipients unidose.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de lautorisation de mise sur le marché
100, ROUTE DE VERSAILLES
78163 MARLY-LE-ROI CEDEX
Exploitant de lautorisation de mise sur le marché
100, ROUTE DE VERSAILLES
78163 MARLY-LE-ROI CEDEX
INDUSTRIESTRASSE 32-36
23843 BAD OLDESLOE
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).