ANSM - Mis à jour le : 06/06/2017
BIMATOPRST TEVA 0,1 mg/mL, collyre en solution
Bimatoprost
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que Bimatoprost Teva 0,1 mg/mL, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser Bimatoprost Teva 0,1 mg/mL, collyre en solution ?
3. Comment utiliser Bimatoprost Teva 0,1 mg/mL, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver Bimatoprost Teva 0,1 mg/mL, collyre en solution ?
6. Contenu de lemballage et autres informations.
1. QUEST-CE QUE Bimatoprost Teva 0,1 mg/mL, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : S01EE03
Le collyre Bimatoprost Teva est utilisé chez ladulte pour réduire une tension élevée dans lil. Ce médicament peut être utilisé seul ou en association avec dautres gouttes appelées « bêta-bloquants », qui réduisent également la tension dans lil.
Comment fonctionne Bimatoprost Teva :
Lil contient un liquide aqueux et transparent qui nourrit lintérieur de lil. Ce liquide est constamment évacué de lil et du nouveau liquide est produit pour le remplacer. Si le liquide ne peut pas être évacué suffisamment vite, la pression à lintérieur de lil augmente. Ce médicament agit en augmentant la quantité de liquide évacué. Cela diminue la tension à lintérieur de lil. Si cette tension excessive nest pas réduite, elle peut entraîner une maladie appelée glaucome et conduire finalement à la détérioration de votre vue.
Nutilisez jamais Bimatoprost Teva 0,1 mg/mL, collyre en solution :
· si vous êtes allergique au bimatoprost ou à lun des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· si vous avez par le passé dû arrêter dutiliser un collyre en raison dun effet secondaire provoqué par le conservateur appelé chlorure de benzalkonium.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant dutiliser Bimatoprost Teva si vous :
· avez des problèmes respiratoires ;
· avez des troubles au niveau du foie ou des reins ;
· avez subi une chirurgie de la cataracte dans le passé ;
· souffrez de sécheresse des yeux ;
· avez ou avez eu des problèmes de cornée (partie avant transparente de lil) ;
· portez des lentilles de contact (voir rubrique « Bimatoprost Teva 0,1 mg/mL, collyre en solution contient du chlorure de benzalkonium » ci-dessous) ;
· avez ou avez eu une tension artérielle basse ou un rythme cardiaque lent ;
· avez eu une infection virale ou une inflammation de lil.
Bimatoprost Teva peut provoquer un assombrissement et un allongement de vos cils, et assombrir également la peau qui entoure vos paupières. La couleur de votre iris peut aussi sassombrir au fil du temps. Ces modifications peuvent être permanentes. Le changement peut être encore plus visible si vous ne traitez quun seul il.
Enfants et adolescents
Bimatoprost Teva na pas fait lobjet détudes sur les enfants de moins de 18 ans et ne devrait donc pas être utilisé par des patients de moins de 18 ans.
Autres médicaments et Bimatoprost Teva 0,1 mg/mL, collyre en solution
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Laction de Bimatoprost Teva peut affecter ou être affectée par laction dautres médicaments que vous prenez, y compris par dautres collyres prescrits en cas de glaucome (par exemple, un analogue des prostaglandines). Parlez-en avec votre médecin car il pourrait avoir besoin de contrôler la pression dans vos yeux au cours du traitement.
Bimatoprost Teva 0,1 mg/mL, collyre en solution avec des aliments et boissons
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Bimatoprost Teva peut passer dans le lait maternel, et lallaitement est donc déconseillé pendant que vous prenez Bimatoprost Teva.
Conduite de véhicules et utilisation de machines
Votre vue peut devenir trouble pendant un court moment juste après lutilisation de Bimatoprost Teva. Il est déconseillé de conduire un véhicule ou manipuler un outil ou une machine jusquà ce que vous ayez retrouvé une vue normale.
Bimatoprost Teva 0,1 mg/mL, collyre en solution contient du chlorure de benzalkonium
Éviter le contact avec les lentilles de contact souples. Retirer les lentilles de contact avant application et attendre au moins 15 minutes avant de les remettre. En raison de la présence de chlorure de benzalkonium, ce médicament peut provoquer une irritation des yeux et peut décolorer les lentilles de contact souple.
3. COMMENT UTILISER Bimatoprost Teva 0,1 mg/mL, collyre en solution ?
Bimatoprost Teva est destiné à être instillé seulement dans lil. La dose recommandée est dune goutte de Bimatoprost Teva dans lil à traiter, une fois par jour, chaque soir.
Si vous utilisez Bimatoprost Teva avec un autre médicament ophtalmique, attendez au moins cinq minutes entre lutilisation de Bimatoprost Teva et lutilisation de lautre médicament ophtalmique.
NE PAS utiliser plus dune fois par jour, car lefficacité du traitement pourrait diminuer.
Mode demploi :
Nutilisez PAS le flacon si la bague dinviolabilité située sur le col du flacon a été cassée avant sa première utilisation.

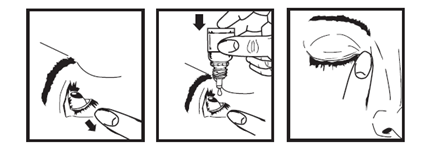
1. Lavez-vous les mains. Inclinez la tête légèrement en arrière et regardez en haut.
2. Tirez doucement la paupière inférieure jusquà ce quil y ait une petite poche.
3. Retournez le flacon à lenvers et appuyez dessus pour en faire tomber une goutte dans chaque il à traiter.
4. Lâchez la paupière inférieure et fermez votre il.
5. Tout en maintenant votre il fermé, appuyez avec le doigt contre le coin interne de l'il traité (du côté du nez), pendant 1 minute.
Essuyer tout excès sécoulant le long de la joue.
Si une goutte tombe à côté de votre il, recommencez.
Pour éviter les infections et les lésions de lil, NE touchez PAS votre il ou quoi que ce soit avec lembout du flacon. Remettez le bouchon et refermez le flacon aussitôt après lavoir utilisé.
Si vous avez utilisé plus de Bimatoprost Teva 0,1 mg/mL, collyre en solution que vous nauriez dû :
Si vous avez utilisé plus de Bimatoprost Teva que vous nauriez dû, il est peu probable que ceci entraîne des effets néfastes. Instillez la goutte suivante à lheure habituelle. Si vous êtes inquiet, parlez-en à votre médecin ou à votre pharmacien.
Si vous oubliez dutiliser Bimatoprost Teva 0,1 mg/mL, collyre en solution :
Si vous arrêtez dutiliser Bimatoprost Teva 0,1 mg/mL, collyre en solution :
Bimatoprost Teva doit être utilisé chaque jour pour agir correctement. Si vous arrêtez dutiliser Bimatoprost Teva, la tension dans votre il risque daugmenter. Vous devez informer votre médecin avant dinterrompre ce traitement.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice.
Très fréquent : pouvant affecter plus de 1 personne sur 10
Effets oculaires
· Légère rougeur (jusquà 29 % des personnes).
Fréquent : pouvant affecter jusquà 1 personne sur 10
Effets oculaires
· Petites érosions ponctuées superficielles de lil, avec ou sans inflammation.
· Irritations.
· Démangeaisons des yeux.
· Cils plus longs.
· Irritation quand une goutte est administrée dans lil.
· Douleur oculaire.
Effets dermatologiques
· Rougeur et démangeaisons des paupières.
· Coloration sombre de la peau autour de lil.
· Pilosité autour de lil.
Peu fréquent : pouvant affecter jusquà 1 personne sur 100
Effets oculaires
· Coloration plus sombre de liris.
· Fatigue oculaire.
· Gonflement de la surface de lil.
· Troubles de la vision.
· Perte des cils.
Effets dermatologiques
· Sécheresse de la peau.
· Croûtes au bord de la paupière.
· Gonflement de la paupière.
· Démangeaisons.
Effets généraux
· Maux de tête.
· Sensation de malaise.
Fréquence indéterminée : ne peut être estimée sur la base des données disponibles
Effets oculaires
· dème maculaire (gonflement de la rétine au fond de lil pouvant entrainer une dégradation de la vision).
· Coloration plus foncée de la paupière.
· Yeux enfoncés dans les orbites.
· Sécheresse de lil.
Effets généraux
· Asthme.
· Aggravation de lasthme.
· Aggravation de laffection pulmonaire appelée « bronchopneumopathie chronique obstructive (BPCO) ».
· Essoufflement.
· Symptômes de réaction allergique (gonflement, rougeur de lil et éruptions cutanées de la peau).
Outre les effets secondaires de Bimatoprost Teva 0,1 mg/mL, les effets secondaires suivants ont été constatés lors de lutilisation dun autre médicament contenant une concentration plus élevée de bimatoprost (0,3 mg/mL) :
· Vertiges.
· Brûlure dans lil.
· Réaction allergique dans lil.
· Inflammation des paupières.
· Difficulté à voir nettement.
· Détérioration de la vision.
· Gonflement de la couche transparente qui recouvre lil.
· Impression davoir quelque chose dans lil.
· Sensibilité à la lumière.
· Larmoiement.
· Yeux collants.
· Assombrissement des cils.
· Saignement de la rétine.
· Inflammation dans lil.
· dème maculaire cystoïde (gonflement de la rétine à lintérieur de lil conduisant à une dégradation de la vision).
· Contractions de la paupière.
· Rétraction de la paupière de la surface de lil.
· Rougeur de la peau autour de lil.
· Augmentation de la tension artérielle.
· Faiblesse.
· Augmentation des résultats des tests sanguins qui évaluent le fonctionnement du foie.
Autres effets indésirables rapportés avec les collyres contenant du phosphate
Dans de très rares cas, certains patients présentant des lésions graves de la couche claire située à lavant de lil (la cornée) ont développé des taches opaques sur la cornée en raison dune accumulation de calcium pendant le traitement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER Bimatoprost Teva 0,1 mg/mL, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
Nutilisez pas ce médicament après la date de péremption indiquée sur létiquette du flacon et sur lemballage extérieur après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 30°C.
Vous devrez jeter le flacon au plus tard quatre semaines après lavoir ouvert pour la première fois, même sil contient encore quelques gouttes. Ceci évitera les infections. Pour vous aider à vous en souvenir, notez la date douverture dans la case prévue sur la boîte.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS
Ce que contient Bimatoprost Teva 0,1 mg/mL, collyre en solution
· La substance active est : le bimatoprost.
Un millilitre de solution contient 0,1 mg de bimatoprost.
· Les autres composants sont : chlorure de benzalkonium (conservateur), chlorure de sodium, phosphate disodique anhydre (E339), acide citrique anhydre (E330) et eau pour préparations injectables. De faibles quantités dacide chlorhydrique ou dhydroxyde de sodium peuvent être ajoutées pour maintenir un niveau dacidité normal (niveaux de pH).
Quest-ce que Bimatoprost Teva 0,1 mg/mL, collyre en solution et contenu de lemballage extérieur
Bimatoprost Teva est un collyre en solution limpide, incolore à légèrement jaune, qui est commercialisé dans une boîte contenant 1 ou 3 flacons en matière plastique munis chacun dun bouchon à vis. Chaque flacon est rempli à moitié environ et contient 3 millilitres de solution. Cette quantité est suffisante pour 4 semaines dutilisation.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de lautorisation de mise sur le marché
100-110, ESPLANADE DU GENERAL DE GAULLE
92931 PARIS LA DEFENSE CEDEX
Exploitant de lautorisation de mise sur le marché
100-110, ESPLANADE DU GENERAL DE GAULLE
92931 PARIS LA DEFENSE CEDEX
TEVA PHARMACEUTICAL WORKS PRIVATE LIMITED COMPANY
Táncsics Mihály út 82.
H-2100 Gödöllő
HONGRIE
ou
Teva Nederland B.V.
Swensweg 5,
2031 GA Haarlem
PAYS-BAS
ou
Teva Pharma B.V.
Swensweg 5,
2031 GA Haarlem
PAYS-BAS
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants :
Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).