1
2
ANSM - Mis à jour le : 27/11/2023
BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
Brinzolamide/tartrate de brimonidine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension ?
3. Comment utiliser BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension ?
6. Contenu de lemballage et autres informations
BRINZOLAMIDE/BRIMONIDINE ZENTIVA est utilisé pour réduire la pression dans les yeux chez les patients adultes (âgés de 18 ans et plus) ayant des pathologies oculaires appelées glaucome ou hypertonie oculaire et pour qui une pression élevée dans les yeux ne peut pas être contrôlée efficacement par un seul médicament.
Nutilisez jamais BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
· si vous êtes allergique au brinzolamide, au tartrate de brimonidine ou à l'un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6)
· si vous êtes allergique aux médicaments appelés sulfonamides [incluant par exemple des médicaments utilisés pour traiter le diabète et les infections ainsi que des diurétiques (médicaments favorisant lélimination de leau)]
· si vous prenez un inhibiteur de la monoamine oxydase (IMAO) (incluant par exemple des médicaments pour traiter la dépression ou la maladie de Parkinson) ou certains antidépresseurs. Vous devez prévenir votre médecin si vous prenez des antidépresseurs
· si vous avez des problèmes rénaux sévères
· si vous avez trop dacidité dans le sang (une maladie appelée acidose hyperchlorémique)
· chez les bébés et les nourrissons de moins de 2 ans.
Avertissements et précautions
Adressez-vous à votre médecin, optométriste (opticien) ou pharmacien avant dutiliser BRINZOLAMIDE/BRIMONIDINE ZENTIVA si vous avez actuellement ou si vous avez eu dans le passé :
· des problèmes de foie
· une forme d'hypertension dans les yeux appelée glaucome à angle étroit
· les yeux secs ou des problèmes de cornée
· une maladie coronarienne (dont les symptômes peuvent inclure une douleur ou une oppression thoracique, un essoufflement ou une suffocation), une insuffisance cardiaque, une pression artérielle basse ou élevée
· une dépression
· des troubles de la circulation sanguine ou une mauvaise circulation (comme la maladie de Raynaud, le syndrome de Raynaud ou une insuffisance cérébrale)
· si vous avez déjà développé une éruption cutanée sévère ou une desquamation de la peau, des cloques et/ou des lésions buccales suite à lutilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA ou dautres médicaments apparentés.
Faites attention lors de lutilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension :
Des réactions cutanées graves, y compris un syndrome de Stevens-Johnson et une nécrolyse épidermique toxique, ont été rapportées en association avec le traitement par le brinzolamide. Arrêtez lutilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA et consultez immédiatement un médecin si vous remarquez l'un des symptômes liés à ces réactions cutanées graves décrites dans la rubrique 4.
Si vous portez des lentilles de contact souples, nutilisez pas le collyre quand vous portez vos lentilles. Voir la rubrique « Port de lentilles de contact - BRINZOLAMIDE/BRIMONIDINE ZENTIVA contient du chlorure de benzalkonium » ci-dessous.
Enfants et adolescents
BRINZOLAMIDE/BRIMONIDINE ZENTIVA nest pas destiné à une utilisation chez les enfants et les adolescents âgés de moins de 18 ans car il na pas été étudié dans cette classe dâge. Il est particulièrement important que ce médicament ne soit pas utilisé chez les enfants de moins de 2 ans (voir rubrique « Nutilisez jamais BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension » ci-dessus) car sa sécurité nest pas démontrée.
Autres médicaments et BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
Informez votre médecin, optométriste (opticien) ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
BRINZOLAMIDE/BRIMONIDINE ZENTIVA peut affecter ou être affecté par les autres médicaments que vous prenez, y compris d'autres collyres pour traiter le glaucome.
Informez votre médecin si vous prenez ou avez l'intention de prendre l'un des médicaments suivants :
· médicaments pour réduire la pression artérielle
· médicaments pour le cur, notamment la digoxine (utilisée pour le traitement de pathologies cardiaques)
· autres médicaments pour traiter le glaucome qui sont également prescrits pour le mal de laltitude (acétazolamide, méthazolamide et dorzolamide)
· médicaments pouvant affecter le métabolisme, tels que la chlorpromazine, le méthylphénidate et la réserpine
· médicaments antiviraux, antirétroviraux [utilisés pour traiter le virus de limmunodéficience humaine (VIH)] ou antibiotiques
· médicaments anti-levures ou antifongiques
· inhibiteurs de la monoamine oxydase (IMAO) ou antidépresseurs, notamment l'amitriptyline, la nortriptyline, la clomipramine, la miansérine, la venlafaxine et la duloxétine
· anesthésiques
· sédatifs, opiacés ou barbituriques
Vous devez également signaler à votre médecin si la dose dun de vos médicaments actuels est modifiée.
BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension avec de l'alcool
Si vous consommez régulièrement de l'alcool, demandez conseil à votre médecin, optométriste (opticien) ou pharmacien avant de prendre ce médicament. BRINZOLAMIDE/BRIMONIDINE ZENTIVA peut être affecté par l'alcool.
Si vous êtes enceinte, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin, optométriste (opticien) ou pharmacien avant de prendre ce médicament. Il est conseillé aux femmes en âge de procréer d'utiliser un moyen de contraception efficace pendant le traitement par BRINZOLAMIDE/BRIMONIDINE ZENTIVA. L'utilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA n'est pas recommandée pendant la grossesse. N'utilisez pas BRINZOLAMIDE/BRIMONIDINE ZENTIVA sauf s'il vous a été clairement prescrit par votre médecin.
Si vous allaitez, BRINZOLAMIDE/BRIMONIDINE ZENTIVA peut passer dans votre lait. L'utilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA n'est pas recommandée pendant l'allaitement.
Conduite de véhicules et utilisation de machines
Vous pouvez trouver que votre vision est trouble ou anormale juste après avoir utilisé BRINZOLAMIDE/BRIMONIDINE ZENTIVA. BRINZOLAMIDE/BRIMONIDINE ZENTIVA peut également provoquer une sensation vertigineuse, une somnolence ou de la fatigue chez certains patients.
Ne conduisez pas de véhicules et nutilisez pas de machines tant que les symptômes n'ont pas disparu.
Port de lentilles de contact - BRINZOLAMIDE/BRIMONIDINE ZENTIVA contient du chlorure de benzalkonium
Ce médicament contient 0,15 mg de chlorure de benzalkonium dans 5 mL de produit, équivalant à 0,03 mg/mL.
Le chlorure de benzalkonium peut être absorbé par les lentilles de contact souples et modifier leur couleur. Retirer les lentilles de contact avant application et attendre au moins 15 minutes avant de les remettre. Le chlorure de benzalkonium peut également provoquer une irritation des yeux, surtout si vous souffrez du syndrome de lil sec ou dun trouble de la cornée (couche transparente à lavant de lil). En cas de sensation anormale, de picotements ou de douleur dans les yeux après avoir utilisé ce médicament, contactez votre médecin.
3. COMMENT UTILISER BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension ?
N'utilisez BRINZOLAMIDE/BRIMONIDINE ZENTIVA que dans les yeux. Ne pas avaler ou injecter.
La dose recommandée est une goutte dans l'il ou les yeux atteints(s) deux fois par jour. Utilisez-le chaque jour à la même heure.
Comment lutiliser
· Lavez-vous les mains avant de commencer.
|
|
|
|
1 |
2 |
· Agitez bien avant usage.
· Dévissez le bouchon du flacon. Après retrait du bouchon, si la bague de sécurité du flacon est trop lâche, retirez-la avant dutiliser le produit.
· Ne touchez pas l'embout du flacon avec vos doigts lors de l'ouverture ou de la fermeture du flacon. Vous risqueriez de contaminer le collyre.
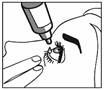
· Tenez le flacon tête en bas, entre le pouce et vos autres doigts. Penchez la tête en arrière.
· Avec un doigt propre, tirez doucement votre paupière inférieure vers le bas pour créer un sillon entre la paupière et votre il. La goutte sera déposée à cet endroit (figure 1).
· Rapprochez lembout du flacon de lil. Si besoin, utilisez un miroir.
· Ne touchez pas votre il, votre paupière, les surfaces voisines ou dautres surfaces avec le compte-gouttes. Vous risqueriez de contaminer le collyre.
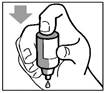
· Appuyez légèrement sur la base du flacon pour libérer une goutte de BRINZOLAMIDE/BRIMONIDINE ZENTIVA.
· Ne comprimez pas le flacon ; il est conçu pour quune légère pression sur la base suffise (figure 2).
Pour réduire la quantité de médicament pouvant pénétrer dans le reste du corps après application de la goutte de collyre, fermez lil et appuyez doucement sur le coin de l'il proche du nez avec un doigt pendant au moins 2 minutes.
Si vous devez traiter les deux yeux, recommencez ces étapes pour l'autre il. Il n'est pas nécessaire de fermer et dagiter le flacon avant dappliquer la goutte dans l'autre il. Refermez bien le flacon immédiatement après usage.
Si vous devez utiliser un autre collyre en plus de BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension, attendez au moins cinq minutes entre l'application de BRINZOLAMIDE/BRIMONIDINE ZENTIVA et celle de l'autre collyre.
Si une goutte tombe à côté de votre il, recommencez.
Si vous avez utilisé plus de BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension que vous nauriez dû
Rincez votre il avec de leau tiède. Ne mettez pas dautre goutte jusquà ce que le moment soit venu de mettre la goutte suivante.
Des adultes ayant accidentellement avalé des médicaments contenant de la brimonidine ont présenté une diminution du rythme cardiaque, une baisse de la tension artérielle pouvant être suivie d'une augmentation de la tension artérielle, une insuffisance cardiaque, des difficultés à respirer et des effets sur le système nerveux. Si cela devait arriver, contactez immédiatement votre médecin.
Des effets indésirables graves ont été signalés chez des enfants ayant accidentellement avalé des médicaments contenant de la brimonidine. Ces enfants ont présenté les signes suivants : somnolence, torpeur, température corporelle basse, pâleur et difficultés à respirer. Si cela devait arriver, contactez immédiatement votre médecin.
En cas d'ingestion accidentelle de BRINZOLAMIDE/BRIMONIDINE ZENTIVA, contactez immédiatement votre médecin.
Si vous oubliez dutiliser BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
Continuez votre traitement en prenant la dose suivante, comme prévu. Nutilisez pas de dose double pour compenser la dose que vous avez oublié dutiliser. Nutilisez pas plus dune goutte dans lil (les yeux) atteint(s), deux fois par jour.
Si vous arrêtez dutiliser BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
Narrêtez pas de prendre BRINZOLAMIDE/BRIMONIDINE ZENTIVA sans en parler dabord à votre médecin. Si vous arrêtez de prendre BRINZOLAMIDE/BRIMONIDINE ZENTIVA sans en parler à votre médecin, la pression de votre il ne sera pas contrôlée, ce qui pourrait provoquer une perte de la vue.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin, à votre optométriste (opticien) ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Si vous présentez l'un des effets indésirables suivants, arrêtez le traitement et consultez immédiatement votre médecin, car ils peuvent être un signe de réaction au médicament. La fréquence dune réaction allergique à ce médicament nest pas connue (la fréquence ne peut être estimée à partir des données disponibles).
· Réactions cutanées graves, notamment rash ou rougeur et démangeaisons corporelles ou oculaires
· Problèmes pour respirer
· Douleurs à la poitrine, irrégularité du battement cardiaque
Contactez immédiatement votre médecin si vous présentez une fatigue extrême ou une sensation vertigineuse.
Les effets indésirables suivants ont été observés avec BRINZOLAMIDE/BRIMONIDINE ZENTIVA et d'autres médicaments contenant uniquement du brinzolamide ou de la brimonidine.
Arrêtez lutilisation de BRINZOLAMIDE/BRIMONIDINE ZENTIVA et adressez-vous immédiatement à votre médecin si vous observez lun des symptômes suivants :
· plaques rougeâtres non surélevées, en forme de cible ou circulaires sur le tronc, souvent avec des cloques centrales, une desquamation de la peau, aphtes de la bouche, de la gorge, du nez, des organes génitaux et des yeux. Ces éruptions cutanées graves peuvent être précédées de fièvre et de symptômes pseudo-grippaux (syndrome de Stevens-Johnson, nécrolyse épidermique toxique).
Fréquents (pouvant affecter jusquà 1 personne sur 10)
· Effets oculaires : conjonctivite allergique (allergie oculaire), inflammation à la surface de lil, douleur oculaire, gêne oculaire, vision trouble ou anormale, rougeur oculaire.
· Effets indésirables généraux : somnolence, sensation vertigineuse, mauvais goût dans la bouche, bouche sèche.
Peu fréquents (pouvant affecter jusquà 1 personne sur 100)
· Effets oculaires : lésion de la surface oculaire avec perte de cellules, inflammation de la paupière, dépôts à la surface de l'il, sensibilité à la lumière, gonflement de l'il (affectant la cornée ou la paupière), sécheresse oculaire, écoulement oculaire, yeux larmoyants, rougeur de la paupière, sensation anormale ou réduite dans l'il, fatigue oculaire, baisse de la vision, vision double, particules de médicament dans les yeux.
· Effets indésirables généraux : baisse de la pression artérielle, douleur à la poitrine, battements du cur irréguliers, rythme cardiaque lent ou rapide, palpitations, difficulté pour dormir (insomnie), cauchemars, dépression, faiblesse généralisée, maux de tête, sensation vertigineuse, nervosité, irritabilité, sensation générale de malaise, perte de mémoire, souffle court, asthme, saignements du nez, symptômes de rhume, sécheresse du nez ou de la gorge, maux de gorge, irritation de la gorge, toux, écoulement nasal, nez bouché, éternuements, infection des sinus, congestion de la poitrine, bourdonnement d'oreille, indigestion, gaz intestinaux ou maux d'estomac, nausées, diarrhée, vomissements, sensation anormale dans la bouche, symptômes allergiques aggravés sur la peau, rash, sensation cutanée anormale, perte de cheveux, démangeaisons généralisées, augmentation du taux de chlore dans le sang ou baisse du nombre de globules rouges lors de la prise de sang, douleur, mal au dos, douleurs ou spasmes musculaires, douleur au rein telle que douleur dans le bas du dos, baisse de la libido, problèmes sexuels masculins.
Très rares (pouvant affecter jusquà 1 personne sur 10 000)
· Effets oculaires : diminution de la taille de la pupille
· Effets indésirables généraux : évanouissement, augmentation de la pression artérielle
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
· Effets oculaires : diminution de la croissance des cils
· Effets indésirables généraux : tremblements, sensation diminuée, perte du goût, valeurs de la fonction hépatique anormales lors de la prise de sang, gonflement du visage, douleur articulaire, envie fréquente d'uriner, douleur à la poitrine, gonflement des extrémités, plaques rougeâtres non surélevées, en forme de cible ou circulaires sur le tronc, souvent avec des cloques centrales, une desquamation de la peau, aphtes de la bouche, de la gorge, du nez, des organes génitaux et des yeux et pouvant être précédées de fièvre et de symptômes pseudo-grippaux. Ces éruptions cutanées graves peuvent engager le pronostic vital (syndrome de Stevens-Johnson, nécrolyse épidermique toxique).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre optométriste (opticien) ou à votre pharmacien. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension ?
Tenir ce médicament hors de la vue et de la portée des enfants.
Nutilisez pas ce médicament après la date de péremption indiquée sur le flacon et sur la boîte après « EXP ». La date de péremption fait référence au dernier jour de ce mois.
Ce médicament ne nécessite pas de précautions particulières de conservation.
Jetez le flacon 4 semaines après lavoir ouvert afin d'éviter les infections et utilisez un nouveau flacon. Inscrivez la date douverture du flacon dans lespace prévu à cet effet sur la boîte.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS
Ce que contient BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg par mL, collyre en suspension
· Les substances actives sont : le brinzolamide et le tartrate de brimonidine. Un mL de suspension contient 10 mg de brinzolamide et 2 mg de tartrate de brimonidine, équivalant à 1,3 mg de brimonidine.
· Les autres composants sont : chlorure de benzalkonium (solution à 50 %) (voir rubrique 2 « Port de lentilles de contact - BRINZOLAMIDE/BRIMONIDINE ZENTIVA contient du chlorure de benzalkonium »), propylèneglycol (E1520), carbomère 974P, acide borique (E284), chlorure de sodium, tyloxapol, acide chlorhydrique et/ou hydroxyde de sodium et eau pour préparations injectables.
Des petites quantités dacide chlorhydrique et/ou dhydroxyde de sodium sont ajoutées pour conserver des niveaux dacidité (niveaux de pH) normaux.
Flacon de 10 mL en PEBD blanc, muni dun embout compte-gouttes en PEBD blanc et dun capuchon en PEHD/PEBD blanc avec une bague dinviolabilité, contenant 5 mL de suspension homogène blanche à blanchâtre.
Les présentations suivantes sont disponibles : boîtes contenant 1 ou 3 flacons de 5 mL.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de lautorisation de mise sur le marché
35 RUE DU VAL DE MARNE
75013 PARIS
Exploitant de lautorisation de mise sur le marché
ZENTIVA FRANCE
35 RUE DU VAL DE MARNE
75013 PARIS
DERVENAKION 6, PALLINI
15351 ATTIKIS
GRECE
OU
BALKANPHARMA-RAZGRAD AD
68 APRILSKO VASTANIE BLVD.
RAZGRAD, 7200
BULGARIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
{mois AAAA}.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).