
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 13/10/2015
TISSEEL, solutions pour colle
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Composant 1 : solution de protéines pour colle
Fibrinogène humain (en tant que protéine coagulable).......................................... 91 mg[1] /ml
Aprotinine (synthétique)............................................................................... 3 000 UIK[2] /ml
Excipient(s) à effet notoire :
Polysorbate 80......................................................................................... 0,6 1,9 mg/ml
Composant 2 : solution de thrombine
Thrombine humaine.......................................................................................... 500 UI[3] /ml
Chlorure de calcium......................................................................................... 40 µmol/ml
1, 2 ou 5 ml de solution de protéines pour colle congelée (avec de laprotinine synthétique) et 1, 2 ou 5 ml de solution de thrombine congelée (avec du chlorure de calcium) se combinent pour produire 2, 4 ou 10 ml de solution de colle de fibrine prête à l'emploi.
|
Après mélange |
1 ml |
2 ml |
4 ml |
10 ml |
|
Composant 1 : solution de protéines pour colle Fibrinogène humain (en tant que protéine coagulable)
Aprotinine synthétique |
45,5 mg
1 500 UIK |
91 mg
3 000 UIK |
182 mg
6 000 UIK |
455 mg
15 000 UIK |
|
Composant 2 : solution de thrombine Thrombine humaine Chlorure de calcium |
250 UI 20 μmol |
500 UI 40 μmol |
1 000 UI 80 μmol |
2 500 UI 200 μmol |
TISSEEL contient du facteur XIII humain co-purifié avec du fibrinogène humain dans des limites de 0,6 à 5 UI/ml.
Pour la liste complète des excipients, voir rubrique 6.1.
Congelées
Lorsqu'elles sont congelées : solutions congelées incolores à jaune pâle, opalescentes ;
Après décongélation : liquides incolores à jaune pâle.
4.1. Indications thérapeutiques
· Pour lamélioration de lhémostase ;
· Comme colle tissulaire pour améliorer la cicatrisation ou pour renforcer les sutures en chirurgie vasculaire et dans les anastomoses gastro-intestinales ;
· Pour le collage des tissus, afin d'améliorer l'adhérence de tissus distincts (par exemple lambeaux tissulaires, greffes, greffes de peau mince [greffes en filet]).
Lefficacité a été démontrée chez les patients entièrement héparinisés.
4.2. Posologie et mode d'administration
Lutilisation de TISSEEL est réservée aux chirurgiens expérimentés qui ont reçu une formation à l'utilisation de TISSEEL.
Le volume de TISSEEL à appliquer et la fréquence dapplication doivent toujours être adaptées aux besoins cliniques sous-jacents du patient.
La dose à appliquer dépend de différents facteurs dont notamment le type dintervention chirurgicale, létendue de la surface à traiter et le mode dapplication, ainsi que le nombre dapplications.
Lapplication du produit doit être adaptée à chaque individu par le médecin traitant. Lors des essais cliniques, les doses individuelles étaient généralement comprises entre 4 et 20 ml. Pour certaines procédures (par exemple un traumatisme hépatique ou le collage de grandes surfaces brûlées), des quantités plus importantes peuvent être nécessaires.
Le volume initial de produit à appliquer sur un site anatomique donné ou une surface cible doit être suffisant pour couvrir entièrement la zone dapplication prévu. Lapplication peut être répétée si nécessaire. Cependant, éviter de réappliquer TISSEEL sur une couche préexistante de TISSEEL polymérisé car TISSEEL ne va pas adhérer à une couche déjà polymérisée.
A titre indicatif, pour le collage de surfaces, 1 boîte de TISSEEL 2 ml (à savoir 1 ml de solution de protéines pour colle plus 1 ml de solution de thrombine) suffira pour coller une surface dau moins 10 cm².
Lorsque TISSEEL est appliqué par pulvérisation, la même quantité permet de recouvrir des surfaces nettement plus importantes, en fonction de lindication spécifique et du patient.
Pour éviter la formation dune quantité excessive de tissu de granulation et assurer une absorption progressive de la colle de fibrine solidifiée, il est recommandé d'appliquer une couche aussi fine que possible de TISSEEL.
Population pédiatrique
La sécurité et lefficacité de TISSEEL nont pas été établies chez les patients pédiatriques.
Mode dadministration
Pour application épilésionnelle.
Pour une utilisation en toute sécurité de TISSEEL par pulvérisation, les recommandations suivantes doivent être respectées :
· En chirurgie ouverte, il convient d'utiliser un dispositif de contrôle de la pression assurant une pression maximum de 2,0 bars (28,5 psi).
· Lors d'interventions peu invasives et laparoscopiques, il convient d'utiliser un dispositif de contrôle de la pression assurant une pression maximum de 1,5 bar (22 psi) et fonctionnant exclusivement à l'aide de gaz carbonique.
· Avant d'appliquer TISSEEL, la surface de la plaie doit être séchée à l'aide des techniques classiques (par ex. application intermittente de compresses, de tampons, utilisation de dispositifs d'aspiration).
· TISSEEL ne doit être strictement reconstitué et administré conformément aux instructions et uniquement avec les dispositifs recommandés pour ce produit (voir rubrique 6.6).
· Pour l'application par pulvérisation, voir les rubriques 4.4 et 6.6 pour les recommandations spécifiques concernant la pression à appliquer et la distance à respecter par rapport au tissu selon le type de procédure chirurgicale et la longueur de lembout dapplicateur.
· Dans les procédures chirurgicales nécessitant l'utilisation de petits volumes de colle de fibrine, il est conseillé d'expulser et d'éliminer les premières gouttes de produit.
TISSEEL nest pas indiqué pour remplacer les sutures cutanées destinées à fermer une plaie chirurgicale.
TISSEEL ne doit jamais être appliqué en intravasculaire. Une application intravasculaire peut entraîner des événements thromboemboliques mettant en jeu le pronostic vital.
TISSEEL ne doit pas être appliqué en cas dhypersensibilité aux substances actives ou à lun des excipients.
4.4. Mises en garde spéciales et précautions d'emploi
Pour application épilésionnelle uniquement. Ne pas appliquer par voie intravasculaire.
Des complications thromboemboliques mettant en jeu le pronostic vital peuvent se produire si le produit est involontairement appliqué en intravasculaire.
La prudence est de rigueur lors de l'application de colle de fibrine au moyen de gaz comprimé.
Toute application au moyen de gaz sous pression peut exposer à un risque potentiel dembolie gazeuse, de rupture tissulaire ou demprisonnement de gaz avec compression susceptible de mettre en jeu le pronostic vital.
TISSEEL doit être appliqué en fine couche. Une couche de produit trop épaisse risque de perturber lefficacité du produit et le processus de cicatrisation de la lésion.
Des cas dembolie gazeuse mettant en jeu le pronostic vital ou fatals sont survenus lors de lutilisation de dispositifs par pulvérisation employant un régulateur de pression pour appliquer la colle de fibrine. Cet événement semble être lié au fait que le dispositif dapplication par pulvérisation ait été utilisé à des pressions supérieures à celles recommandées et/ou à trop forte proximité de la surface des tissus. Le risque semble plus élevé lorsque les colles de fibrine sont vaporisées au moyen d'air, par comparaison avec le CO2, et ne peut donc être exclu avec TISSEEL lorsqu'il est pulvérisé en chirurgie ouverte.
Lors de l'application de TISSEEL à l'aide d'un dispositif dapplication par pulvérisation, veiller à maintenir la pression dans lintervalle recommandé par le fabricant du dispositif dapplication (se reporter au tableau de la rubrique 6.6 pour les pressions et les distances).
Lapplication par pulvérisation de TISSEEL ne doit être effectuée que sil est possible dévaluer précisément la distance de pulvérisation, conformément aux recommandations du fabricant. Ne pas pulvériser à des distances inférieures à celles recommandées.
Lors de la pulvérisation de TISSEEL, il convient de surveiller attentivement toute modification de la pression artérielle, de la fréquence cardiaque, de la saturation en oxygène et du taux de CO2 de fin dexpiration en raison du risque dembolie gazeuse (voir également rubrique 4.2).
TISSEEL ne doit pas être utilisé avec le système EASY SPRAY / SPRAY SET dans les espaces clos de l'organisme.
Avant dadministrer TISSEEL, il faut veiller à ce que les parties du corps en dehors de la surface dapplication souhaitée soient suffisamment protégées (couvertes) pour éviter une adhésion des tissus au niveau de sites non désirés.
Si les colles de fibrine sont appliquées dans des espaces confinés, par exemple le cerveau ou la moelle épinière, il faut tenir compte du risque de complications par compression.
Pour assurer un mélange adéquat du composant de protéines pour colle et du composant de thrombine, les premières gouttes du produit de l'aiguille d'application doivent être expulsées et éliminées immédiatement avant l'utilisation.
Comme pour tout produit dorigine protéique, des réactions allergiques d'hypersensibilité sont possibles.
L'application intravasculaire est susceptible daugmenter la probabilité et la gravité des réactions d'hypersensibilité aiguës chez les patients sensibles.
Des réactions d'hypersensibilité et des réactions anaphylactiques (également fatales, incluant le choc anaphylactique) ont été signalées avec TISSEEL. Les signes de réaction dhypersensibilité comprennent éruptions cutanées, urticaire généralisée, oppression thoracique, respiration sifflante et hypotension. Si ces symptômes apparaissent, ladministration doit être interrompue immédiatement, et les mesures standards actuellement en vigueur pour le traitement du choc doivent être appliquées. Le produit restant doit être retiré du site d'application.
TISSEEL contient une protéine synthétique (aprotinine). Même en cas dapplication strictement locale, il existe un risque de réaction anaphylactique liée à la présence daprotinine. Ce risque apparaît plus élevé sil y a eu une exposition antérieure, même bien tolérée. Toute application daprotinine ou de produit à base daprotinine doit donc être inscrite dans le dossier du patient.
Laprotinine synthétique ayant une structure identique à l'aprotinine dorigine bovine, l'utilisation de TISSEEL chez les patients allergiques aux protéines bovines doit être attentivement évaluée.
Deux études rétrospectives non randomisées portant sur la chirurgie de pontage coronarien ont montré que le risque de mortalité était accru de manière statistiquement significative chez les patients qui avaient reçu de la colle de fibrine. Bien que ces études n'aient pas pu montrer une relation de causalité, on ne peut pas exclure que l'augmentation du risque soit associée à l'utilisation de TISSEEL chez ces patients. Par conséquent, il convient d'être plus attentif pour éviter une administration intravasculaire accidentelle de ce produit.
Il faut éviter d'injecter dans la muqueuse nasale car des complications thromboemboliques peuvent survenir dans la région de l'artère ophtalmique.
L'injection tissulaire de TISSEEL risque dendommager les tissus environnants.
Le polysorbate 80 peut provoquer des irritations cutanées localement limitées telle qu'une dermite de contact.
Les mesures habituelles de prévention du risque de transmission dagents infectieux par les médicaments préparés à partir de sang ou de plasma humain comprennent la sélection clinique des donneurs, la recherche des marqueurs spécifiques dinfection sur chaque don et sur les mélanges de plasma ainsi que la mise en uvre dans le procédé de fabrication détapes efficaces pour linactivation/élimination virale. Cependant, lorsque des médicaments préparés à partir de sang ou de plasma humain sont administrés, le risque de transmission dagents infectieux ne peut pas être totalement exclu. Ceci sapplique également aux virus inconnus ou émergents ou autres types dagents infectieux.
Les mesures prises sont considérées comme efficaces vis-à-vis des virus enveloppés tels que le VIH, le VHB et le VHC, et vis-à-vis du virus non enveloppé, le VHA.
Les mesures prises peuvent être dune efficacité limitée vis-à-vis des virus non enveloppés, tels que le parvovirus B19. Linfection par le parvovirus B19 peut être sévère chez le ftus et chez les personnes atteintes de certains types danémies ou d'un déficit immunitaire).
Les préparations contenant de la cellulose oxydée ne doivent pas être utilisées avec TISSEEL (voir rubrique 6.2 Incompatibilités).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
La sécurité demploi des colles/hémostatiques à base de fibrine pour une utilisation au cours de la grossesse ou de lallaitement chez lêtre humain na pas été établie dans le cadre dessais cliniques contrôlés. Les études expérimentales chez lanimal sont insuffisantes pour évaluer la sécurité du produit en ce qui concerne la reproduction, le développement de lembryon ou du ftus, le déroulement de la grossesse et le développement péri- et post-natal.
Le produit ne doit donc pas être administré aux femmes enceintes ou qui allaitent à moins dune nécessité absolue.
Voir rubrique 4.4 pour des informations relatives à l'infection au parvovirus B19.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
L'apparition de réactions allergiques ou d'hypersensibilité (telles quangioedème, brûlures et démangeaisons au site d'application, bradycardie, bronchospasmes, frissons, difficultés respiratoires, érythème transitoire (« flushing »), urticaire généralisée, céphalées, éruptions cutanées, hypotension, léthargie, nausées, prurit, agitation, tachycardie, oppression thoracique, fourmillements, vomissements, respiration sifflante) peut survenir dans de rares cas chez des patients traités avec des hémostatiques/colles à base de fibrine.
Dans certains cas isolés, ces réactions ont évolué vers une anaphylaxie sévère. Ces réactions peuvent être observées surtout si la préparation est appliquée de façon répétée ou administrée à des patients dont l'hypersensibilité à laprotinine (voir rubrique 4.4) ou à dautres composants du produit est connue.
Même si un traitement répété avec TISSEEL a été bien toléré, une administration ultérieure de TISSEEL ou une administration systémique daprotinine peut entraîner des réactions anaphylactiques sévères.
La présence d'anticorps contre les hémostatiques/colles à base de fibrine peut être constatée en de rares occasions.
Une injection intravasculaire accidentelle est susceptible d'entraîner un incident thromboembolique et une CIVD, ainsi que dinduire un risque de réaction anaphylactique (voir la rubrique 4.4).
Pour la sécurité vis-à-vis dagents transmissibles, voir la rubrique 4.4.
Les effets indésirables présentés dans cette rubrique ont été rapportés lors des études cliniques évaluant la sécurité et lefficacité de TISSEEL ou après la mise sur le marché de colles de fibrine commercialisées par Baxter. Dans ces études cliniques, TISSEEL a été administré pour un complément d'hémostase dans la chirurgie cardiaque, vasculaire et d'arthroplastie totale de la hanche et lors d'opérations du foie et de la rate. Dautres essais cliniques comprenaient le collage de vaisseaux lymphatiques chez des patients subissant une dissection des ganglions lymphatiques axillaires, le collage de l'anastomose colique et la fermeture de la dure-mère dans la fosse postérieure. Dans ces études, la colle de fibrine Baxter a été administrée chez 1 146 patients.
Très fréquent (≥ 1/10)
Fréquent (≥ 1/100 à < 1/10)
Peu fréquent (≥ 1/1 000 à < 1/100)
Rare (≥ 1/10 000 à < 1/1 000)
Très rare (< 1/10 000)
Fréquence indéterminée (ne peut être estimée à partir des données disponibles)
|
Classe de systèmes d'organes |
Terme préférentiel MedDRA |
Fréquence |
|
Infections et infestations |
Infection de plaie post-opératoire |
Fréquent |
|
Affections hématologiques et du système lymphatique |
Augmentation des produits de dégradation de la fibrine |
Peu fréquent |
|
Affections du système immunitaire |
Réactions d'hypersensibilité * |
Peu fréquent |
|
Réactions anaphylactiques * |
Peu fréquent |
|
|
Choc anaphylactique * |
Peu fréquent |
|
|
Paresthésie |
Peu fréquent |
|
|
Bronchospasme |
Peu fréquent |
|
|
Respiration sifflante |
Peu fréquent |
|
|
Prurit |
Peu fréquent |
|
|
Erythème |
Peu fréquent |
|
|
Affections du système nerveux |
Trouble sensoriel |
Fréquent |
|
Affections cardiaques |
Bradycardie |
Peu fréquent |
|
Tachycardie |
Peu fréquent |
|
|
Affections vasculaires |
Thrombose de la veine axillaire ** |
Fréquent |
|
Hypotension |
Rare |
|
|
Hématome (SAI) |
Peu fréquent |
|
|
Embolie artérielle |
Peu fréquent |
|
|
Embolie artérielle cérébrale |
Peu fréquent |
|
|
Infarctus cérébral ** |
Peu fréquent |
|
|
Affections respiratoires, thoraciques et médiastinales |
Dyspnée |
Peu fréquent |
|
Affections gastro-intestinales |
Nausées |
Peu fréquent |
|
Obstruction intestinale |
Peu fréquent |
|
|
Affections de la peau et du tissu sous-cutané |
Rash |
Fréquent |
|
Urticaire |
Peu fréquent |
|
|
Retard de cicatrisation |
Peu fréquent |
|
|
Affections musculo-squelettiques et systémiques |
Extrémités douloureuses |
Fréquent |
|
Troubles généraux et anomalies au site dadministration |
Douleur liée à la procédure |
Peu fréquent |
|
Douleur |
Fréquent |
|
|
Température augmentée |
Fréquent |
|
|
Bouffée congestive |
Peu fréquent |
|
|
dème |
Peu fréquent |
|
|
Lésions, intoxications et complications liées aux procédures |
Sérome |
Très fréquent |
|
Angidème |
Peu fréquent |
* Les réactions anaphylactiques et le choc anaphylactique ont inclus des issues fatales.
** Comme résultat d'une application intravasculaire au niveau du sinus pétreux supérieur.
Réactions liées à la classe
Les autres effets indésirables associés à la classe des colles de fibrine/substances hémostatiques comprennent : embolie gazeuse lors de l'utilisation de dispositifs employant de l'air ou du gaz comprimé ; ce phénomène semble être lié à lutilisation du dispositif par pulvérisation à des pressions supérieures à celles recommandées et/ou à une proximité immédiate de la surface des tissus. Les manifestations d'hypersensibilité comprennent l'irritation au point d'application, la gêne thoracique, les frissons, les maux de tête, la léthargie, les impatiences et les vomissements.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.ansm.sante.fr.
Aucun cas de surdosage na été rapporté.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Le système dadhésion de la fibrine déclenche la phase finale de la coagulation sanguine physiologique. La conversion du fibrinogène en fibrine se produit par fractionnement du fibrinogène en monomères de fibrine et en fibrinopeptides. Les monomères de fibrine sagrègent et forment un caillot fibrineux. Le facteur XIIIa, qui est activé à partir du facteur XIII par l'action concomitante de la thrombine et des ions calcium, stabilise la fibrine en réseau.
Au cours de la cicatrisation de la lésion, la plasmine induit une augmentation de lactivité fibrinolytique et de la décomposition de la fibrine en ses produits de dégradation. La dégradation protéolytique de la fibrine est inhibée par les anti-fibrinolytiques. Laprotinine est présente dans TISSEEL en tant quanti-fibrinolytique afin déviter la dégradation prématurée du caillot.
Concernant les données d'efficacité, des études in vivo ont été menées sur quatre modèles animaux reproduisant autant que possible la situation des patients. TISSEEL a fait preuve defficacité concernant l'hémostase primaire et secondaire ainsi que la cicatrisation de la plaie.
Une étude clinique prospective, en parallèle, randomisée, en double aveugle, multicentrique a évalué TISSEEL par rapport à une présentation précédente du produit avec simple inactivation virale chez 317 patients subissant une chirurgie cardiaque avec pontage cardiopulmonaire et sternotomie médiane. Si l'hémostase ne pouvait être obtenue avec les méthodes chirurgicales classiques, les patients étaient traités avec TISSEEL ou un produit contrôle. Le but était d'obtenir l'hémostase dans les 5 minutes après l'administration et de la maintenir jusqu'à la fermeture chirurgicale de la plaie.
Le résultat, basé sur un intervalle de confiance unilatéral à 97,5 %, montre que TISSEEL (double inactivation virale) n'était pas inférieur à la formulation précédente (simple inactivation virale) chez les patients traités avec succès.
|
Hémostase dans les 5 minutes et maintenue jusqu'à la fermeture chirurgicale |
||
|
|
TISSEEL (double inactivation virale) |
Colle de fibrine (simple inactivation virale) |
|
Echantillon complet d'analyse |
127/144 (88,2 %) |
129/144 (89,6 %) |
|
Analyse per protocole |
108/123 (87,8 %) |
122/135 (90,4 %) |
5.2. Propriétés pharmacocinétiques
TISSEEL est uniquement destiné à une application épilésionnelle. Ladministration intravasculaire est contre-indiquée. En conséquence, aucune étude pharmacocinétique par voie intravasculaire na été réalisée chez lhomme.
Aucune étude pharmacocinétique na été menée chez différentes espèces d'animaux de laboratoire.
Les colles/ hémostatiques à base de fibrine sont métabolisés de la même manière que la fibrine endogène par fibrinolyse et phagocytose.
5.3. Données de sécurité préclinique
Des études de toxicité en dose unique chez les rats et les lapins nont montré aucune toxicité aiguë de TISSEEL. En outre, aucun signe d'activité mutagène na été observé lors des tests in vitro appropriés. La solution de protéines pour colle a également été bien tolérée, dans les cultures in vitro de fibroblastes humains, démontrant une excellente compatibilité cellulaire et une absence de cytotoxicité. En se basant sur un examen détaillé de la littérature, toute influence délétère ou toxique due à des réactifs S/D résiduels sur TISSEEL peut être exclue.
Composant 1 : solution de protéines pour colle
albumine humaine, L-histidine, nicotinamide, citrate de sodium dihydraté, polysorbate 80 (Tween 80), eau pour préparations injectables.
Composant 2 : solution de thrombine
albumine humaine, chlorure de sodium, eau pour préparations injectables.
Ce médicament ne doit pas être mélangé avec dautres médicaments à lexception de ceux mentionnés en rubrique 6.6.
2 ans.
6.4. Précautions particulières de conservation
A conserver et transporter congelé (£ -20 °C). La chaîne du froid doit être assurée sans interruption jusqu'à l'application.
Conserver dans lemballage dorigine à labri de la lumière.
Le produit non ouvert, décongelé à une température maximum de 25 °C, peut être conservé pendant 72 heures maximum à une température ne dépassant pas 25 °C. Si la solution n'est pas utilisée dans les 72 heures suivant la décongélation, TISSEEL doit être jeté.
Ne jamais recongeler ou réfrigérer la solution après décongélation.
6.5. Nature et contenu de l'emballage extérieur
Les solutions de protéines pour colle et de thrombine sont fournies dans une seringue à usage unique prête à l'emploi en polypropylène à double compartiment, munie d'un capuchon, en sachet.
Le produit est fourni dans l'un des conditionnements suivants :
· Seringue AST (« Advanced Syringe Technology »), seringue à double compartiment en polypropylène à usage unique munie d'un capuchon protecteur.
· Système à double seringue (SDS), deux seringues en polypropylène, clippées dans le double porte-seringue DUPLOJECT (clip à deux seringues), chacune munie d'un capuchon protecteur.
Contenu du conditionnement :
· Contenu du conditionnement avec la seringue AST :
o 1 seringue à double compartiment prête à l'emploi remplie de 1 ml, 2 ml ou 5 ml de solution de protéines pour colle congelée (avec aprotinine synthétique) dans un compartiment et 1 ml, 2 ml ou 5 ml de solution de thrombine dans l'autre. Chaque compartiment est fermé par un capuchon en caoutchouc siliconé. Le produit est emballé dans deux sachets stériles en aluminoplastique.
o 1 set de dispositifs d'application (= DUO set) constitué de 2 pièces de raccordement et de 4 canules d'application (non pointues) et dun double piston.
OU
· Contenu du conditionnement avec le système à double seringue :
o 1 système à double seringue constitué de deux seringues à usage unique avec piston clippées dans le double porte-seringue DUPLOJECT. La seringue à échelle graduée bleue est remplie de 1 ml, 2 ml ou 5 ml de solution de protéines pour colle congelée (avec aprotinine synthétique) et la seringue à échelle graduée noire est remplie de 1 ml, 2 ml ou 5 ml de solution de thrombine. Chaque seringue est fournie avec un piston en polypropylène à anneau d'étanchéité et est fermée par un capuchon protecteur. Les seringues sont clippées dans le double porte-seringue afin d'avoir une tige de piston commune. Le produit est emballé dans deux sachets en plastique stériles.
o 1 set de dispositifs d'application (= DUPLOJECT COMBI) constitué de 2 pièces de raccordement et de 4 canules d'application (non pointues).
Conditionnements :
TISSEEL est disponible dans les conditionnements suivants : 1 x 2 ml (1 ml + 1 ml), 1 x 4 ml (2 ml
+ 2 ml) et 1 x 10 ml (5 ml + 5 ml).
Toutes les présentations peuvent ne pas être commercialisées.
Dautres accessoires pour lapplication du produit sont disponibles auprès de BAXTER.
6.6. Précautions particulières délimination et de manipulation
Avant ladministration de TISSEEL, veiller à couvrir toutes les parties du corps situées hors de la zone à traiter afin d'empêcher l'adhérence des tissus sur des sites non souhaités.
Pour empêcher ladhésion de TISSEEL aux gants et aux instruments, humidifier ces derniers à laide dune solution de chlorure de sodium avant tout contact.
La recommandation pour le collage de surfaces est la suivante : une présentation de TISSEEL 2 ml (cest-à-dire 1 ml de solution de protéines pour colle plus 1 ml de solution de thrombine) suffira pour coller une surface dau moins 10 cm².
La dose nécessaire dépend de la dimension de la surface à couvrir.
Eviter d'appliquer les deux composants de TISSEEL séparément l'un après l'autre.
TISSEEL ne doit pas être soumis à des températures supérieures à 37 °C et ne peut pas être réchauffé au micro-onde.
Précautions particulières de manipulation et préparation
La solution de protéines pour colle et la solution de thrombine sont conditionnées dans une seringue prête à l'emploi. Le contenu a été stérilisé et emballé dans des conditions dasepsie. Le sachet interne et son contenu sont stériles tant que lintégrité du sachet externe na pas été compromise.
La seringue prête à l'emploi peut être décongelée à l'aide de l'une des méthodes suivantes :
Il est recommandé de décongeler et de réchauffer les deux composants de la colle au bain-marie stérile à une température comprise entre 33 et 37 °C. La température du bain-marie ne doit pas dépasser 37 °C. (Pour contrôler la plage de température spécifiée, la température de leau doit être contrôlée à laide dun thermomètre et leau doit être changée si nécessaire. En cas dutilisation dun bain-marie stérile pour la décongélation et le réchauffement, la seringue pré-remplie doit être retirée de ses sachets). Ne retirer le capuchon protecteur de la seringue qu'une fois la décongélation terminée et fixer immédiatement la canule d'application. N'utiliser TISSEEL qu'après décongélation totale.
1) Décongélation rapide (bain-marie stérile)
Placer le sachet interne sur le champ stérile, retirer la seringue prête à l'emploi du sachet interne et la placer directement dans le bain-marie stérile. Vérifier que le contenu de la seringue prête à l'emploi est entièrement immergé dans leau.
Tableau 1 : durées de décongélation et de réchauffement au bain-marie stérile à une température de 33 à 37 °C maximum.
|
Conditionnement |
Durées de décongélation et de réchauffement Bain-marie stérile entre 33 et 37 °C Produit sans sachet |
|
|
AST |
Système à double seringue |
|
|
2 ml |
5 minutes |
8 minutes |
|
4 ml |
5 minutes |
9 minutes |
|
10 ml |
12 minutes |
13 minutes |
2) Décongélation dans un bain-marie non stérile
Le produit peut également être décongelé hors du champ stérile à laide dun bain-marie non stérile.
Laisser la seringue prête à l'emploi dans les deux sachets et placer lensemble dans un bain-marie hors du champ stérile pendant la durée appropriée. Vérifier que les sachets restent immergés dans l'eau pendant toute la durée de la décongélation. Après la décongélation, retirer les sachets du bain-marie, sécher le sachet externe et placer le sachet interne contenant la seringue prête à l'emploi sur le champ stérile.
Tableau 2 : durées de décongélation et de réchauffement hors du champ stérile avec un bain-marie non stérile à une température de 33 à 37 °C maximum.
|
Conditionnement |
Durées de décongélation et de réchauffement Bain-marie non stérile entre 33 et 37 °C Produit dans les sachets |
|
|
AST |
Système à double seringue |
|
|
2 ml |
30 minutes |
31 minutes |
|
4 ml |
40 minutes |
46 minutes |
|
10 ml |
80 minutes |
64 minutes |
3) Décongélation dans un incubateur
Une troisième méthode consiste à décongeler et réchauffer les composants de la colle dans un incubateur entre 33 et 37 °C maximum.
Les durées de décongélation et de réchauffement dans un incubateur sont indiquées au tableau 3. Les données concernent le produit dans les sachets.
Tableau 3 : durées de décongélation et de réchauffement dans un incubateur à une température de 33 à 37 °C maximum.
|
Conditionnement |
Durées de décongélation et de réchauffement Incubateur entre 33 et 37 °C Produit dans les sachets |
|
|
AST |
Système à double seringue |
|
|
2 ml |
40 minutes |
62 minutes |
|
4 ml |
85 minutes |
77 minutes |
|
10 ml |
105 minutes |
114 minutes |
4) Décongélation à température ambiante (ne dépassant pas 25°C)
Le produit peut être décongelé à température ambiante. Les durées indiquées dans le tableau 4 sont les durées minimales pour une décongélation à température ambiante. Après décongélation, le produit doit être conservé à température ambiante et utilisé dans les 72 heures.
Lors dune décongélation à température ambiante, le produit doit ensuite être réchauffé à 33 37 °C maximum juste avant utilisation. Les durées de réchauffement correspondantes sont également indiquées dans le tableau 4.
Tableau 4 : durées de décongélation et de réchauffement à température ambiante (= TA) suivies dun réchauffement supplémentaire, avant utilisation, dans un incubateur à une température de 33 à 37 °C maximum.
|
Conditionnement |
Durées de décongélation et de réchauffement à température ambiante (25 °C maximum) suivies d'un réchauffement supplémentaire en incubateur entre 33 et 37 °C maximum Produit dans les sachets |
|||
|
AST |
Système à double seringue |
|||
|
Décongélation à température ambiante (25 °C maximum) |
Réchauffement en incubateur (33-37 °C) |
Décongélation à température ambiante (25 °C maximum) |
Réchauffement en incubateur (33-37 °C) |
|
|
2 ml |
60 minutes |
+ 15 minutes |
82 minutes |
+ 28 minutes |
|
4 ml |
110 minutes |
+ 25 minutes |
117 minutes |
+ 30 minutes |
|
10 ml |
160 minutes |
+ 35 minutes |
167 minutes |
+ 44 minutes |
Remarque :
· Ne pas décongeler le produit en le tenant dans les mains.
· Ne pas réchauffer TISSEEL au micro-onde.
· Ne jamais recongeler ni réfrigérer le produit après décongélation.
Stabilité après décongélation
Après une décongélation rapide (cest-à-dire à des températures comprises entre 33 et 37 °C), TISSEEL peut être conservé entre 33 et 37 °C pendant 12 heures maximum.
Le produit en sachet non ouvert, décongelé à température ambiante, peut être conservé pendant 72 heures maximum à température ambiante contrôlée (ne dépassant pas 25 °C). Si TISSEEL n'est pas utilisé dans les 72 heures suivant la décongélation, il doit être jeté.
Manipulation après décongélation/avant application
Pour assurer un mélange optimal des deux solutions et une parfaite solidification de la colle de fibrine, les deux composants doivent être réchauffés à une température de 33 à 37 °C immédiatement avant utilisation.
La solution de protéines de colle et la solution de thrombine doivent être limpides ou légèrement opalescentes. Ne pas utiliser de solutions troubles ou présentant des dépôts. Avant administration, les produits décongelés doivent être inspectés visuellement pour mettre en évidence la présence de particules, un changement de coloration, ou tout changement de laspect. Dans lun ou lautre de ces cas, jeter les solutions.
La solution de protéines pour colle, une fois décongelée, doit être un liquide légèrement visqueux. Si la solution a la consistance dun gel solidifié, elle doit être considérée comme dénaturée (par exemple, en raison dune interruption de la chaîne du froid ou par un surchauffage pendant le réchauffement). Dans ce cas, TISSEEL ne doit pas être utilisé.
Ne pas retirer la seringue des sachets avant utilisation. Ne pas retirer les capuchons de protection des seringues avant utilisation. Ne pas utiliser TISSEEL avant la fin de la décongélation et du réchauffement (consistance liquide).
Pour plus dinformations relatives à la préparation, veuillez-vous adresser à linfirmière ou au médecin responsable.
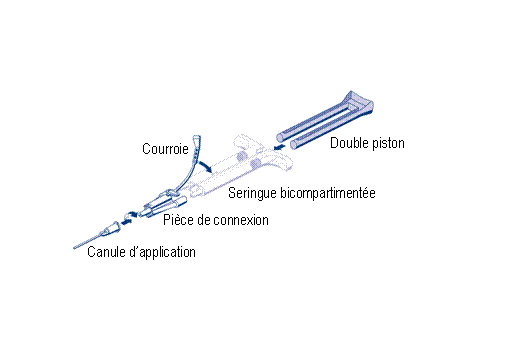
Administration avec la seringue AST :
Pour lapplication, la seringue bicompartimentée prête à l'emploi contenant la solution de protéines pour colle et la solution de thrombine doit être connectée à une pièce de raccordement et à une canule dapplication, fournis dans les accessoires. Le piston commun de la seringue bicompartimentée prête à l'emploi garantit ladministration de volumes égaux via la pièce de raccordement, les solutions étant mélangées dans la canule dapplication avant administration.
Instructions d'utilisation pour AST :


· Connecter les embouts de la seringue bicompartimentée à la pièce de raccordement en sassurant quils sont fermement fixés. Fixer la pièce de raccordement en attachant la languette de sécurité à la seringue bicompartimentée. Si la languette de sécurité se déchire, utiliser la pièce de raccordement de rechange. En labsence de pièce de rechange, une utilisation de la seringue est toujours possible, mais il convient de vérifier létanchéité du raccordement afin déviter tout risque de fuite.
· Fixer une canule dapplication à la pièce de raccordement.
· Ne pas expulser lair présent dans la pièce de raccordement ou la canule dapplication avant de commencer lapplication proprement dite, sinon louverture de la canule risque de sobstruer.
· Appliquer le mélange de solution de protéines pour colle et de solution de thrombine sur la surface dapplication ou sur la surface des parties à coller.
OU
Administration avec le système à double seringue :
Pour lapplication, les deux seringues à usage unique contenant la solution de protéines pour colle et la solution de thrombine doivent être connectées à une pièce de raccordement et à une canule dapplication, fournis dans le set de dispositifs (DUPLOJECT COMBI). Le piston commun du double porte-seringue DUPLOJECT garantit ladministration de volumes égaux via la pièce de raccordement, les solutions étant mélangées dans la canule dapplication avant administration.
Instructions d'utilisation du système à double seringue
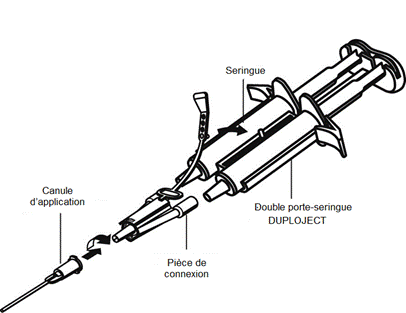
· Connecter les embouts du système à double seringue à la pièce de raccordement en sassurant quils sont fermement fixés. Fixer la pièce de raccordement en attachant la languette de sécurité au double porte-seringue DUPLOJECT. Si la languette de sécurité se déchire, utiliser la pièce de raccordement de rechange. En labsence de pièce de rechange, une utilisation de la seringue est toujours possible, mais il convient de vérifier létanchéité du raccordement afin déviter tout risque de fuite.
· Fixer une canule dapplication à la pièce de raccordement.
· Ne pas expulser lair présent dans la pièce de raccordement ou la canule dapplication avant de commencer lapplication proprement dite, sinon louverture de la canule risque de sobstruer.
· Appliquer le mélange de solution de protéines pour colle et de solution de thrombine sur la surface dapplication ou sur la surface des parties à coller.
Remarque :
· Si lapplication des composants de la colle de fibrine est interrompue, il est possible que la canule soit immédiatement obstruée. Dans ce cas, remplacer la canule dapplication par une nouvelle canule juste avant la reprise de lapplication. Si les ouvertures de la pièce de raccordement sont obstruées, utiliser la pièce de raccordement de rechange fournie avec lemballage.
· Après le mélange des composants, la colle de fibrine commence à agir en quelques secondes en raison de la concentration élevée en thrombine (500 UI/ml).
· La colle de fibrine peut également être appliquée avec d'autres accessoires parfaitement adaptés fournis par BAXTER, par exemple pour lutilisation endoscopique, la chirurgie peu invasive ou lapplication sur de grandes surfaces ou des zones difficiles daccès. Lors de lutilisation de ces dispositifs dapplication, respecter scrupuleusement les instructions dutilisation des dispositifs.
· Après l'application de TISSEEL, laisser au moins 2 minutes pour obtenir une polymérisation suffisante.
· Dans certaines applications, des matériaux biocompatibles, comme la compresse de collagène, sont utilisés comme substance porteuse ou pour la consolidation.
Pulvérisation
Lors de l'application de TISSEEL à l'aide d'un dispositif de pulvérisation, veiller à utiliser une pression et une distance avec le tissu conformes aux limites recommandées par le fabricant comme suit :
|
Recommandations concernant la pression, la distance et les dispositifs pour l'application par pulvérisation de TISSEEL |
|||||
|
Chirurgie |
Spray set à utiliser |
Embouts applicateurs à utiliser |
Dispositif de contrôle de la pression à utiliser |
Distance recommandée avec le tissu ciblé |
Pression de pulvérisation recommandée |
|
Plaie ouverte |
Tisseel / Artiss Spray Set |
Sans objet |
EasySpray |
10-15 cm |
1,5-2,0 bars (21,5-28,5 psi) |
|
Tisseel / Artiss Spray Set boîte de 10 |
Sans objet |
EasySpray |
|||
|
|
|||||
|
Procédures laparoscopiques / peu invasives |
Sans objet |
Applicateur Duplospray MIS 20 cm |
Régulateur Duplospray MIS |
2-5 cm |
1,21,5 bar (18-22 psi) |
|
Régulateur Duplospray MIS NIST B11 |
|||||
|
Applicateur Duplospray MIS 30 cm |
Régulateur Duplospray MIS |
||||
|
Régulateur Duplospray MIS NIST B11 |
|||||
|
Applicateur Duplospray MIS 40 cm |
Régulateur Duplospray MIS |
||||
|
Régulateur Duplospray MIS NIST B11 |
|||||
|
Embout remplaçable |
Régulateur Duplospray MIS |
||||
|
Régulateur Duplospray MIS NIST B11 |
|||||
Lors de la pulvérisation de TISSEEL, tout changement de pression artérielle, de fréquence cardiaque,
de saturation en oxygène et de taux de CO2 de fin d'expiration en raison du risque d'embolie gazeuse doit être surveillé (voir également rubriques 4.2 et 4.4).
Pour l'application de TISSEEL dans les espaces thoraciques et abdominaux fermés, le système d'applicateur et de régulateur DUPLOSPRAY MIS est recommandé. Consulter le mode d'emploi du dispositif DUPLOSPRAY MIS.
Elimination
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
IMMEUBLE BERLIOZ
4 BIS RUE DE LA REDOUTE
78280 GUYANCOURT
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 34009 550 008 6 0 : Seringue (polypropylène) à double compartiment de 1 x 2 ml (1 ml + 1 ml) muni de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication et dun double piston.
· 34009 550 008 7 7 : Seringue (polypropylène) à double compartiment de 1 x 4 ml (2 ml + 2 ml) muni de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication et dun double piston.
· 34009 550 008 8 4 : Seringue (polypropylène) à double compartiment de 1 x 10 ml (5 ml + 5 ml) muni de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication et dun double piston.
· 34009 550 008 9 1 : Système à double seringues (polypropylène) de 1 x 2 ml (1 ml + 1 ml) avec piston, clippées dans un double porte-seringue et munies de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication.
· 34009 550 009 1 4 : Système à double seringues (polypropylène) de 1 x 4 ml (2 ml + 2 ml) avec piston, clippées dans un double porte-seringue et munies de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication.
· 34009 550 009 2 1 : Système à double seringues (polypropylène) de 1 x 10 ml (5 ml + 5 ml) avec piston, clippées dans un double porte-seringue et munies de capuchons, avec un set de dispositifs dapplication constitué de 2 pièces de raccordement et de 4 canules dapplication.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[A compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[A compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I. Réservé à lusage hospitalier. Lutilisation de TISSEEL est réservée aux chirurgiens expérimentés.