RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 10/01/2018
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Miconazole................................................................................................................................. 2 g
1,25 mL de gel contient 31,25 mg de miconazole.
2,5 mL de gel contient 62,5 mg de miconazole.
Excipient à effet notoire : éthanol (alcool).
Titre alcoolique volumique : 1,1 % (v/v)
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Nourrissons âgés de 4 à 24 mois : 1,25 mL appliqués 4 fois par jour après les repas.
Enfants âgés de 2 ans et plus : 2,5 mL appliqués 4 fois par jour après les repas.
Adultes : 5 mL (correspondant à deux cavités de 2,5 mL), appliqués 4 fois par jour après les repas.
La durée habituelle du traitement est de 7 à 15 jours.
Le traitement doit être continué pendant au moins une semaine après que les symptômes aient disparu.
Pour les candidoses orales, les prothèses dentaires doivent être retirées la nuit et brossées avec le gel.
Mode dadministration
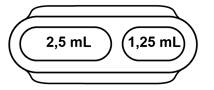
Le dispositif de mesure comprend deux cavités distinctes de 1,25 mL et 2,5 mL.

Chaque dose doit être divisée en petites portions et le gel appliqué sur la (les) zone(s) affectée(s) avec un doigt propre. Le gel ne doit pas être appliqué au fond de la gorge en raison du risque de suffocation.
Le gel ne doit pas être avalé immédiatement, mais gardé dans la bouche aussi longtemps que possible (voir rubrique 4.4).
DAKTARIN 2 %, gel buccal ne doit pas être utilisé dans les cas suivants :
· Hypersensibilité à la substance active, à dautres dérivés imidazolés ou à l'un des excipients mentionnés dans la rubrique 6.1.
· Chez le nourrisson âgé de moins de 4 mois ou chez des patients pour qui le réflexe de déglutition nest pas encore suffisamment développé (voir rubrique 4.4).
· Insuffisance hépatique, compte-tenu du métabolisme hépatique.
· Utilisation en association avec :
o les anti-vitamines K (warfarine, acénocoumarol, fluindione),
o les sulfamides hypoglycémiants.
(voir rubrique 4.5)
4.4. Mises en garde spéciales et précautions d'emploi
Compte-tenu dun faible passage systémique du miconazole lors de ladministration de DAKTARIN 2%, gel buccal, la survenue de réactions cutanées graves (par exemple, nécrolyse épidermique toxique et syndrome de Stevens Johnson) décrits avec certains dérivés azolés par voie systémique ne peut être exclue (voir rubrique 4.8). Il est recommandé que les patients soient informés sur les signes des réactions cutanées graves, et que lutilisation de DAKTARIN 2%, gel buccal soit arrêtée dès lors que de tels signes cutanés apparaissent ou sont suspectés.
DAKTARIN 2 %, gel buccal doit être administré à distance des repas ou au moins 10 minutes après.
Dans la mesure du possible, il doit être conservé dans la bouche 2 ou 3 minutes avant d'être avalé.
Dans lindication perlèche, appliquer le gel sur les lésions à traiter avec le bout des doigts, par massage doux jusquà pénétration complète.
Risque de suffocation chez les nourrissons et les jeunes enfants
- Lors de ladministration du gel de miconazole, il est important de sassurer que le réflexe de déglutition est bien acquis, en particulier chez les nourrissons âgés de 4 à 6 mois.
- La limite dâge minimum pour ladministration du produit doit être augmentée à 5-6 mois pour les nourrissons nés prématurés ou les nourrissons présentant un retard de développement neuromusculaire.
- DAKTARIN 2 %, gel buccal doit être administré avec précaution chez les nourrissons et les jeunes enfants (âgés de 4 à 24 mois). Il faut agir avec prudence pour sassurer que le gel nobstrue pas la gorge. Le gel ne doit donc pas être appliqué au fond de la gorge.
- Chaque dose doit être divisée en petites portions et appliquée dans la bouche avec un doigt propre. Observer le patient pour détecter une éventuelle suffocation.
- Le gel ne doit pas être appliqué sur le mamelon dune femme allaitant en raison du risque détouffement du nourrisson.
Excipient à effet notoire
DAKTARIN 2 %, gel buccal contient de faibles quantités déthanol (alcool), inférieures à 100 mg par dose (22 mg d'alcool dans 2,5 mL de gel).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Associations contre-indiquées (voir rubrique 4.3)
+ Anti-vitamines K (warfarine, acénocoumarol, fluindione)
Hémorragies imprévisibles, éventuellement graves. Des saignements, dont certains avec une issue fatale, ont été rapportés lors de lutilisation concomitante de miconazole en gel buccal et de warfarine.
+ Sulfamides hypoglycémiants
Augmentation de l'effet hypoglycémiant avec survenue possible de manifestations hypoglycémiques, voire de coma.
Associations faisant l'objet de précautions demploi
+ Phénytoïne (et, par extrapolation, fosphénytoïne)
Augmentation des concentrations plasmatiques de phénytoïne pouvant atteindre des valeurs toxiques. Mécanisme invoqué : inhibition du métabolisme hépatique de la phénytoïne.
Surveillance clinique étroite, dosage des concentrations plasmatiques de phénytoïne et adaptation éventuelle de sa posologie pendant le traitement par le miconazole et après son arrêt.
4.6. Fertilité, grossesse et allaitement
Grossesse
Les études effectuées chez l'animal n'ont pas mis en évidence d'effet tératogène mais une foetotoxicité sur plusieurs espèces. En clinique, aucun effet malformatif ou foetotoxique n'est apparu à ce jour. Toutefois, le nombre de grossesses documentées exposées au miconazole est insuffisant pour exclure tout risque. En conséquence, l'utilisation du miconazole ne doit être envisagée au cours de la grossesse que si nécessaire.
Il n'existe pas de données sur l'excrétion du miconazole dans le lait maternel. En conséquence, la prudence s'impose en cas de prescription chez la femme en cours d'allaitement. Le gel ne doit pas être appliqué sur le mamelon dune femme allaitante en raison du risque de suffocation du nourrisson (voir rubrique 4.4).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Le tableau suivant présente tous les effets indésirables identifiés, y compris ceux qui ont été rapportés au cours de l'expérience post-commercialisation.
Les effets indésirables sont classés en fonction de leur fréquence selon la convention suivante : très fréquent (³ 1/10), fréquent (³ 1/100 à < 1/10), peu fréquent (³ 1/1 000 à < 1/100), rare (³ 1/10 000 à < 1/1 000), très rare (< 1/10 000), indéterminée (fréquence ne pouvant être estimée à partir des données cliniques disponibles).
|
Classe de systèmes organes |
Effets indésirables |
|
Fréquence indéterminée |
|
|
Affections du système immunitaire
|
Réaction anaphylactique, hypersensibilité |
|
Affections du système nerveux
|
Dysgueusie |
|
Affections respiratoires, thoraciques et médiastinales |
Suffocation |
|
Affections gastro-intestinales |
Sécheresse buccale, Nausées, Gêne buccale, Vomissement, Diarrhée, Stomatite, Décoloration de la langue, Régurgitation (effet observé dans la population pédiatrique) |
|
Affections de la peau et du tissu sous-cutané
|
Angioedème, Rash, Pustulose exanthémateuse aiguë généralisée* |
|
Troubles généraux et anomalies au site dadministration |
Goût du produit anormal |
|
Investigations |
Transaminases augmentées
|
*Compte-tenu dun faible passage systémique du miconazole lors de ladministration de DAKTARIN 2 %, gel buccal, la survenue deffets indésirables non dose-dépendants décrits avec certains dérivés azolés tels que des réactions cutanées graves autres que celle mentionnée dans le tableau ci-dessus (syndrome de Stevens-Johnson, nécrolyse épidermique toxique) ne peut être exclue.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr.
En cas de surdosage accidentel, des vomissements et une diarrhée peuvent apparaître.
Traitement
Il n'existe pas d'antidote spécifique. Un traitement symptomatique sera mis en place.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Antifongique à large spectre et antibactérien Gram+, le miconazole est actif en particulier sur les Candida et autres levures, principaux responsables des mycoses buccales.
Le miconazole inhibe la biosynthèse de lergostérol dans les champignons et modifie la composition dautres composants lipidiques constituant la membrane, ce qui entraîne une nécrose des cellules fongiques.
5.2. Propriétés pharmacocinétiques
Après application sous forme de gel buccal, le miconazole reste présent dans la cavité buccale pendant plusieurs heures ainsi que l'attestent les concentrations salivaires qui varient de 5 à 0,4 µg/mL de 30 minutes à 3 heures suivant une application de 125 mg de miconazole (6,25 g de gel buccal). Le miconazole est progressivement et modérément résorbé le long du tractus digestif. Il présente une biodisponibilité analogue, à dose équivalente, à celle de la forme orale (comprimé dosé à 125 mg).
Bien qu'administré de façon locale sous forme de gel buccal, le miconazole est absorbé systémiquement.
Distribution
Le miconazole absorbé se lie aux protéines plasmatiques (88,2%), dabord sur la sérum-albumine et sur les globules rouges (10,6%).
Biotransformation et élimination
La portion de miconazole absorbée est largement métabolisée ; moins de 1% de la dose administrée est excrété dans les urines sous forme inchangée. Lélimination seffectue principalement par les fèces, après biotransformation hépatique. La demi-vie terminale du miconazole plasmatique est de 20 à 25h chez la plupart des patients. La concentration plasmatique de miconazole est modérément réduite (approximativement 50%) pendant lhémodialyse.
5.3. Données de sécurité préclinique
3 ans.
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Tube aluminium de 40 g ou 80 g avec dispositif de mesure en polypropylène de 2,5 mL. Un tube de 40 g contient léquivalent de 12 doses de 2,5 mL. Un tube de 80 g contient approximativement léquivalent de 25 doses de 2,5 mL.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières délimination et de manipulation
Pour les instructions dutilisation, se référer à la rubrique 3 « Comment prendre DAKTARIN 2 %, gel buccal » de la notice.
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
1, RUE CAMILLE DESMOULINS
TSA 91003
92787 ISSY-LES-MOULINEAUX CEDEX 9
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 34009 326 806 8 9 : 40 g en tube (aluminium)
· 34009 348 308 0 8 : 80 g en tube (aluminium)
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
Date de première autorisation : 04 mai 1984
Date de dernier renouvellement : 04 mai 2009
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.