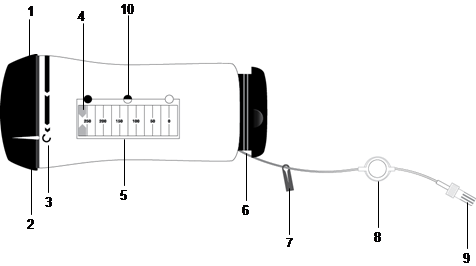
1. Capuchon du système dadministration
6. Tuyau
2. Flèche indicatrice
7. Élément de fixation
3. Position MARCHE
8. Filtre
4. Flèche de surveillance
9. Bouchon du tuyau
5. Fenêtre de la jauge
10. Indicateurs circulaires
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 05/07/2018
ROPIVACAINE READYFUSOR 2 mg/ml, solution pour perfusion en système dadministration
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
1 ml de solution pour perfusion contient du chlorhydrate de ropivacaïne monohydraté, correspondant à 2 mg de chlorhydrate de ropivacaïne.
1 dispositif dadministration (pompe à perfusion ROPIVACAINE READYFUSOR) contient 250 ml de solution pour perfusion de chlorhydrate de ropivacaïne monohydraté, correspondant à 500 mg de chlorhydrate de ropivacaïne.
Excipient(s) à effet notoire : chaque ml contient 0,16 mmol (3,7 mg) de sodium. Chaque unité contient 40 mmol (920 mg) de sodium.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution pour perfusion en système dadministration
Solution limpide, incolore en flacon à soufflets, contenu dans un dispositif dadministration (pompe à perfusion ROPIVACAINE READYFUSOR, voir rubrique 6.6).
4.1. Indications thérapeutiques
ROPIVACAINE READYFUSOR est utilisé :
· Pour maintenir un bloc nerveux périphérique continu par une perfusion continue.
· Pour linfiltration continue de la plaie.
4.2. Posologie et mode d'administration
Posologie
Adultes
Le dispositif dadministration, la pompe à perfusion ROPIVACAINE READYFUSOR délivre le produit avec un débit denviron 5 ml/h, correspondant à 10 mg/h, pendant une durée maximale de 48 h.
Le débit de perfusion fixe de 5 ml (10 mg) par heure apporte une analgésie suffisante avec seulement un léger bloc moteur non progressif dans la plupart des cas de douleur post-opératoire modérée à sévère.
En fonction du statut clinique du patient, il convient denvisager la prescription dautres analgésiques par voie orale (pour une analgésie contrôlée par le patient), ou linjection de bolus supplémentaires dun anesthésique local. Dans ce cas, il faut également tenir compte de la fiche dinformation de lautre médicament.
Population pédiatrique
ROPIVACAINE READYFUSOR nest pas indiqué chez lenfant et ladolescent.
Mode dadministration
Pour utilisation périneurale et infiltration.
Pour maintenir un bloc nerveux périphérique continu par perfusion périneurale continue, la technique ci-après peut être recommandée :
· Tout dabord, à moins quil nait été induit avant lopération, le bloc est réalisé avec la ropivacaïne 7,5 mg/ml.
· Lanalgésie est ensuite maintenue avec ROPIVACAINE READYFUSOR.
Pour linfiltration continue de la plaie, un cathéter multi-perforé doit être placé dans la plaie pendant lintervention chirurgicale (voir les rubriques 6.5 et 6.6).
Une surveillance étroite de leffet analgésique doit être mise en place afin dinterrompre le traitement de la douleur dès que la douleur le permet.
Précautions à prendre avant la manipulation ou ladministration du médicament
Pour les instructions concernant la préparation du médicament avant administration, voir la rubrique 6.6.
· Anesthésie régionale intraveineuse.
· Anesthésie paracervicale obstétricale.
· Utilisation intravasculaire.
· Utilisation intrathécale
· Utilisation intra-cérébrale.
· Utilisation intra-articulaire.
4.4. Mises en garde spéciales et précautions d'emploi
Les données ci-après concernent toutes les voies dadministration de la solution de ropivacaïne 2 mg/ml afin de couvrir lensemble du spectre des données de sécurité.
Cardiovasculaire
Les patients traités par des anti-arythmiques de classe III (par exemple lamiodarone) doivent être étroitement surveillés. Un monitoring ECG devra être envisagé car les effets cardiaques peuvent être additifs.
On a signalé de rares cas darrêt cardiaque au cours de lutilisation de ROPIVACAINE READYFUSOR pour un bloc nerveux périphérique, surtout après injection intravasculaire accidentelle involontaire à des patients âgés ou à des patients cardiaques. Dans certains cas, la réanimation fut difficile. En cas darrêt cardiaque, des tentatives répétées de réanimation peuvent savérer nécessaires pour augmenter les chances dévolution favorable.
Blocs au niveau de la tête et du cou
Certaines procédures d'anesthésie locale telles que des injections au niveau de la tête et du cou peuvent s'accompagner d'une plus grande fréquence d'effets indésirables sévères et cela, quel que soit lanesthésique local employé.
Blocs nerveux périphériques majeurs
Des blocs nerveux périphériques majeurs peuvent impliquer ladministration dun grand volume danesthésique local dans des zones fortement vascularisées, souvent proches des grands vaisseaux sanguins où le risque dinjection intravasculaire et/ou dabsorption systémique rapide est accru, ce qui peut entraîner des concentrations plasmatiques élevées.
Hypersensibilité
Il faut tenir compte du risque dhypersensibilité croisée avec dautres anesthésiques locaux de type amide.
Patients en mauvais état général
Les patients qui présentent un état général médiocre du fait de leur âge ou d'autres facteurs de risque tels qu'un bloc auriculoventriculaire partiel ou complet, une affection hépatique évoluée ou une insuffisance rénale sévère nécessitent une attention particulière, bien qu'une anesthésie locorégionale soit fréquemment indiquée chez ces patients.
Insuffisants hépatiques et rénaux
La ropivacaïne étant métabolisée par le foie, elle doit être utilisée avec prudence en cas d'insuffisance hépatique sévère, et les ré-injections limitées en raison d'une élimination retardée. Chez l'insuffisant rénal, aucune adaptation posologique n'est en principe nécessaire en administration unique ou en traitement de courte durée. Une acidose et une hypoprotidémie plasmatique, souvent associées à l'insuffisance rénale, peuvent augmenter le risque de toxicité systémique.
Porphyrie aiguë
ROPIVACAINE READYFUSOR peut être porphyrinogène et ne peut être prescrit aux patients ayant une porphyrie aiguë que lorsqu'il n'y a pas d'alternative plus sûre. Des précautions appropriées doivent être prises pour les patients vulnérables conformément aux manuels standards, et/ou en consultation avec des experts de cette maladie.
Chondrolyse
Il a été rapporté après commercialisation des cas de chondrolyse chez des patients recevant une perfusion post-opératoire intra-articulaire continue d'anesthésiques locaux, y compris la ropivacaïne. La majorité des cas de chondrolyse rapportés ont concerné larticulation de l'épaule. La perfusion intra-articulaire continue nest pas une indication approuvée pour ROPIVACAINE READYFUSOR. La perfusion intra-articulaire continue avec ROPIVACAINE READYFUSOR doit être évitée, étant donné que lefficacité et la sécurité demploi nont pas été établies.
Administration prolongée
Ladministration prolongée de ropivacaïne doit être évitée chez les patients qui prennent simultanément des inhibiteurs puissants du cytochrome CYP1A2 comme la fluvoxamine et lénoxacine (voir la rubrique 4.5).
Quand on veut obtenir des blocs prolongés par perfusion continue, il faut tenir compte du risque datteindre des taux plasmatiques toxiques ou de provoquer une lésion locale du tissu nerveux. Des doses cumulatives allant jusquà 675 mg de ropivacaïne par 24 h pour lanalgésie chirurgicale et post-opératoire ont été bien tolérées chez les adultes. Il en est de même pour des perfusions péridurales continues post-opératoires administrées à raison de 28 mg/h pendant 72 h. Chez un nombre limité de patients, des doses supérieures allant jusquà 800 mg/jour ont été administrées avec des effets indésirables relativement faibles.
Dans des études cliniques, une perfusion péridurale de ropivacaïne 2 mg/ml seule ou mélangée à 1-4 microgrammes/ml de fentanyl a été administrée pour le traitement de la douleur post-opératoire pendant un maximum de 72 heures. Lassociation de ropivacaïne et de fentanyl a amélioré le soulagement de la douleur mais a induit des effets indésirables des opiacés. Lassociation de ropivacaïne et de fentanyl n'a été étudiée que pour la ropivacaïne 2 mg/ml.
Population pédiatrique
ROPIVACAINE READYFUSOR nest pas indiqué chez les enfants et les adolescents.
Excipients à effet notoire
Ce médicament contient 3,7 mg de sodium par ml. En tenir compte chez les patients suivant un régime contrôlé en sodium.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Le cytochrome P450 (CYP) 1A2 joue un rôle dans la formation du 3-hydroxy ropivacaïne, métabolite majeur. In vivo, la clairance plasmatique de la ropivacaïne diminue jusquà 77 % au cours dune co-administration de fluvoxamine, un inhibiteur sélectif et puissant du CYP1A2. Par conséquent, des inhibiteurs puissants du CYP1A2 tels que la fluvoxamine et lénoxacine administrés conjointement pendant ladministration prolongée de ROPIVACAINE READYFUSOR peuvent créer une interaction avec ROPIVACAINE READYFUSOR. Ladministration prolongée de ropivacaïne chez les patients qui prennent en même temps des inhibiteurs puissants du CYP1A2 doit être évitée (voir aussi la rubrique 4.4).
In vivo, la clairance plasmatique de la ropivacaïne est réduite de 15 % en cas de co-administration de kétoconazole, un inhibiteur puissant et sélectif du CYP3A4. Cependant, linhibition de cette isoenzyme est probablement peu significative au point de vue clinique.
In vitro, la ropivacaïne est un inhibiteur compétitif du CYP2D6 mais elle ne semble pas inhiber cette isoenzyme aux concentrations plasmatiques cliniquement atteintes.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il ny a pas de données adéquates sur lutilisation de la ropivacaïne pendant la grossesse humaine. Les résultats des études expérimentales avec les animaux nont révélé aucun effet nocif direct ou indirect, relatif à la grossesse, au développement embryonnaire/ftal, à laccouchement ou au développement post-natal (voir rubrique 5.3).
Par mesure de précaution, il est préférable déviter lutilisation de ROPIVACAINE READYFUSOR pendant la grossesse.
Nous ne disposons actuellement pas de données relatives à lexcrétion de la ropivacaïne dans le lait humain.
Il convient dinterrompre lallaitement de façon temporaire pendant la durée du traitement avec ROPIVACAINE READYFUSOR. Le lait sera tiré et détruit pendant cette période.
Fertilité
Nous ne disposons daucune donnée.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables de ROPIVACAINE READYFUSOR sont comparables à ceux des autres anesthésiques locaux de type amide à longue durée d'action. Les effets indésirables doivent être distingués des effets physiologiques induits par le bloc nerveux proprement dit.
Les fréquences utilisées dans le tableau de la rubrique 4.8 sont : très fréquents (≥ 1/10), fréquents (≥ 1/100 à < 1/10), peu fréquents (≥ 1/1 000 à < 1/100), rares (≥ 1/10 000 à < 1/1 000), très rares (< 1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
|
Classes de systèmes dorganes |
Fréquence |
Effet indésirable |
|
Affections du système immunitaire |
Rares |
Réactions allergiques (réactions anaphylactiques, dème angioneurotique et urticaire) |
|
Affections psychiatriques |
Peu fréquents |
Anxiété |
|
Affections du système nerveux |
Fréquents |
Paresthésie, sensation vertigineuse, céphalées |
|
Peu fréquents |
Symptômes de toxicité au niveau du système nerveux central (convulsions, convulsions de type grand mal, crises dépilepsie, étourdissements, paresthésie péribuccale, engourdissement de la langue, hyperacousie, acouphènes, troubles de la vision, dysarthrie, contractions musculaires, tremblements*, hypoesthésie |
|
|
Fréquence indéterminée |
Dyskinésie |
|
|
Affections cardiaques |
Fréquents |
Bradycardie, tachycardie |
|
Rares |
Arrêt cardiaque, troubles du rythme cardiaque |
|
|
Affections vasculaires |
Très fréquents |
Hypotension |
|
Fréquents |
Hypertension |
|
|
Peu fréquents |
Syncope |
|
|
Affections respiratoires, thoraciques et médiastinales |
Peu fréquents |
Dyspnée |
|
Affections gastro-intestinales |
Très fréquents |
Nausées |
|
Fréquents |
Vomissements |
|
|
Affections musculo-squelettiques et systémiques |
Fréquents |
Dorsalgie |
|
Affections du rein et des voies urinaires |
Fréquents |
Rétention urinaire |
|
Troubles généraux et anomalies au site dadministration |
Fréquents |
Elévation de la température, frissons |
|
Peu fréquents |
Hypothermie |
* Ces symptômes surviennent surtout suite à une injection intravasculaire accidentelle, à un surdosage ou à une absorption rapide, voir rubrique 4.9.
Effets indésirables liés à la classe pharmacothérapeutique
Complications neurologiques
Une neuropathie et un dysfonctionnement de la moelle épinière (p. ex. : syndrome de lartère spinale antérieure, arachnoïdite, equina cauda), qui peuvent dans de rares cas entraîner des séquelles irréversibles, ont été associés avec une anesthésie régionale, indépendamment de lanesthésique local utilisé.
Toxicité systémique aiguë
Les réactions toxiques systémiques impliquent principalement le système nerveux central (SNC) et le système cardiovasculaire. Des réactions de ce type sont provoquées par les concentrations sanguines élevées en un anesthésique local ; celles-ci peuvent être le résultat dune injection intravasculaire (accidentelle), dun surdosage ou dune absorption exceptionnellement rapide à partir de zones fortement vascularisées (voir aussi rubrique 4.4). Les réactions au niveau du SNC sont similaires pour tous les anesthésiques locaux de type amide, tandis que les réactions cardiovasculaires dépendent davantage, tant quantitativement que qualitativement, du médicament.
Toxicité du système nerveux central
La toxicité au niveau du système nerveux central constitue une réponse par paliers, caractérisée par des symptômes et des signes de sévérité croissante : d'abord des troubles de la vue ou de l'ouïe, un engourdissement péribuccal, des vertiges, des étourdissements, une sensation de picotements et une paresthésie. De la dysarthrie, de la rigidité musculaire et de la crispation musculaire sont plus sévères et peuvent précéder lapparition de convulsions généralisées. Ces symptômes ne doivent pas être confondus avec un comportement neurotique. Une perte de conscience et des convulsions de type grand mal peuvent suivre et durer de quelques secondes à quelques minutes. De lhypoxie et de lhypercapnie peuvent apparaître rapidement pendant les convulsions en raison dune activité musculaire accrue accompagnée dinterférence avec la respiration. Dans les cas sévères, de lapnée peut apparaître. Lacidose respiratoire et métabolique augmente et accroît les effets toxiques des anesthésiques locaux.
La guérison est consécutive à redistribution de lanesthésique local à partir du système nerveux central, son métabolisme et son excrétion. La guérison peut être rapide à moins que de grandes quantités du médicament naient été injectées.
Toxicité du système cardiovasculaire
La toxicité cardiovasculaire est lindice dune situation plus grave. Lhypotension, la bradycardie, larythmie et même un arrêt cardiaque peuvent survenir comme résultat de fortes concentrations systémiques en anesthésiques locaux. Chez des volontaires, la perfusion intraveineuse de ropivacaïne a fait apparaître des signes de dépression de la conductivité et de la contractibilité.
Des signes de toxicité au niveau du système nerveux central précèdent généralement les effets cardiovasculaires toxiques à moins que le patient ne soit sous anesthésie générale ou n'ait été soumis à une lourde sédation par benzodiazépines ou barbituriques.
Traitement de la toxicité systémique aiguë
Voir rubrique 4.9.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr.
Symptômes
Des injections intravasculaires accidentelles danesthésiques locaux peuvent provoquer des réactions toxiques systémiques immédiates (en quelques secondes à quelques minutes). En cas de surdosage, le pic de concentration plasmatique peut ne pas être atteint avant 1 à 2 h en fonction du site dinjection: les signes de toxicité peuvent alors être retardés (voir rubrique 4.8).
Traitement
Si des signes de toxicité systémique aiguë apparaissent, il convient darrêter immédiatement linjection de lanesthésique local. Les symptômes de toxicité au niveau du SNC (convulsions, dépression du SNC) doivent être traités rapidement par des mesures de soutien appropriées des voies respiratoires et par ladministration danticonvulsivants.
En cas darrêt circulatoire, on commencera immédiatement une réanimation cardio-pulmonaire. Une oxygénation et une ventilation optimales, une circulation assistée et un traitement de lacidose sont dune importance vitale.
Si une dépression cardiovasculaire apparaît (hypotension, bradycardie), un traitement approprié par des liquides intraveineux, des amines vasopressives et/ou des agents inotropes doit être envisagé.
En cas darrêt cardiaque, des essais répétés de réanimation peuvent être nécessaires pour une évolution favorable.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : anesthésique local de type amide, code ATC : N01BB09
La ropivacaïne est un anesthésique local de type amide à longue durée daction. La ropivacaïne possède à la fois des propriétés anesthésiques et analgésiques. De fortes doses produisent une anesthésie de type chirurgical tandis que de faibles doses génèrent un bloc sensitif accompagné dun bloc moteur restreint et non progressif.
Le mécanisme d'action consiste en une réduction réversible de la perméabilité membranaire de la fibre nerveuse vis-à-vis des ions sodium. Cela entraîne une diminution de la vitesse de dépolarisation et une augmentation du seuil d'excitabilité, ce qui se traduit par un blocage local des influx nerveux.
La ropivacaïne se distingue surtout par sa longue durée daction. Lapparition et la durée dune anesthésie locale efficiente dépendent du site dadministration et de la dose, mais ne sont pas influencées par la présence dun vasoconstricteur (p. ex. : ladrénaline (épinéphrine)).
Des volontaires sains exposés à des perfusions intraveineuses ont bien supporté la ropivacaïne à faibles doses et ont présenté les symptômes attendus au niveau du SNC avec la dose maximale tolérée. L'expérience clinique dont on dispose pour ce médicament indique une bonne marge de sécurité lors d'utilisations adéquates aux doses recommandées.
5.2. Propriétés pharmacocinétiques
La ropivacaïne possède un centre chiral et est disponible sous forme de S-(-)-énantiomère pur. Elle est très liposoluble. Tous les métabolites ont un effet anesthésique local, mais il est nettement moins puissant et d'une durée nettement plus courte que celui de la ropivacaïne.
Les concentrations plasmatiques de ropivacaïne dépendent de la dose, de la voie dadministration et du niveau de vascularisation au point dinjection. La ropivacaïne jouit dune pharmacocinétique linéaire avec une Cmax proportionnelle à la dose.
La ropivacaïne subit une absorption complète et biphasique à partir de lespace péridural avec des taux de demi-vie chez ladulte de lordre de 14 minutes et de 4 h pour les 2 phases. La résorption lente est le facteur limitant de la vitesse d'élimination. C'est la raison pour laquelle la demi-vie délimination apparente est plus longue après injection péridurale qu'après administration intraveineuse. Chez les enfants également, la ropivacaïne présente une absorption biphasique à partir de l'espace péridural caudal.
La ropivacaïne a une clairance totale plasmatique moyenne de lordre de 440 ml/min., une clairance rénale de 1 ml/min., un volume de distribution à létat d'équilibre de 47 litres, et une demi-vie terminale de 1,8 heure après administration intraveineuse. La ropivacaïne présente un rapport d'extraction hépatique intermédiaire d'environ 0,4. Elle est principalement liée dans le plasma à l'alpha-1-glycoprotéine acide, avec une fraction libre de 6 %.
Pendant une perfusion péridurale continue et une perfusion interscalène, on a observé une augmentation de la concentration plasmatique totale due à une augmentation post-opératoire des taux d'alpha-1-glycoprotéine acide (AGP).
Les fluctuations des taux de ropivacaïne non liée, c'est-à-dire pharmacologiquement active, sont moins importantes que pour la concentration plasmatique totale.
Étant donné que la ropivacaïne présente un coefficient dextraction hépatique modéré à faible, sa vitesse délimination devrait dépendre de la concentration plasmatique non liée. Une augmentation en postopératoire de lAGP fera diminuer la fraction non liée par une augmentation de la fixation aux protéines. Il en résultera une diminution de la clairance totale et une augmentation de la concentration plasmatique totale, comme lont montré les études chez lenfant et chez ladulte. La clairance de la ropivacaïne non liée reste inchangée, comme le démontrent les concentrations stables de la fraction non liée au cours dune perfusion postopératoire. Ce sont les taux plasmatiques non liés qui sont responsables des effets pharmacodynamiques systémiques et de la toxicité systémique.
La ropivacaïne traverse facilement le placenta et l'état d'équilibre est rapidement atteint en ce qui concerne le taux de ropivacaïne non liée. Chez le ftus, le taux de liaison aux protéines plasmatiques est moindre que chez la mère : il en résulte des taux plasmatiques totaux plus faibles chez le ftus que chez la mère.
La ropivacaïne est largement métabolisée, principalement par hydroxylation aromatique.
Après administration intraveineuse, 86% de la dose est excrétée dans l'urine, dont seulement environ 1% sous forme non métabolisée. La 3-hydroxy-ropivacaïne, métabolite majeur, est excrétée pour environ 37%, principalement sous une forme conjuguée, dans lurine. On a également observé une élimination urinaire de 1-3% de 4-hydroxy-ropivacaïne, de métabolite N-déalkylé (PPX) et de dérivé 4-hydroxy-déalkylé. Dans le plasma, on a uniquement mis en évidence des concentrations observables du composé 3-hydroxy-ropivacaïne conjugué ou non.
Une altération de la fonction rénale a peu ou pas d'influence sur la pharmacocinétique de la ropivacaïne. La clairance rénale du PPX est corrélée de façon significative à la clairance de la créatinine. Une absence de corrélation entre l'exposition totale, exprimée en ASC, et la clairance de la créatinine indique que la clairance totale du PPX comprend une élimination non rénale, en plus de l'excrétion rénale. Certains patients atteints d'insuffisance rénale peuvent présenter une exposition accrue au PPX résultant d'une faible clairance non rénale. En raison de la réduction de la toxicité dans le SNC du PPX par rapport à la ropivacaïne, les conséquences cliniques sont considérées comme négligeables lors dun traitement à court terme. Les patients présentant une maladie rénale en stade terminal, sous dialyse, nont pas été étudiés.
In vivo, il nexiste aucune évidence de racémisation de la ropivacaïne.
5.3. Données de sécurité préclinique
18 mois
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
La pompe à perfusion ROPIVACAINE READYFUSOR est un cylindre orange avec un capuchon noir à chaque extrémité. Il est conçu pour recevoir un flacon transparent à soufflets en PEHD contenant 250 ml de solution de chlorhydrate de ropivacaïne monohydraté pour perfusion. Un tube sans latex avec raccord Luer y est raccordé en permanence.
Chaque emballage contient une pompe à perfusion ROPIVACAINE READYFUSOR et une poche de transport. Des sets comprenant en outre un cathéter multi-perforé stérile sans latex destiné à être placé dans la plaie (longueur 6,5 ou 15 cm) sont également disponibles.
6.6. Précautions particulières délimination et de manipulation
ROPIVACAINE READYFUSOR est sans conservateur et destiné à un usage unique exclusivement.
La solution doit faire lobjet dun examen visuel avant utilisation. La solution ne peut être utilisée que si elle est limpide, pratiquement exempte de particules et si le récipient nest pas endommagé.
La pompe à perfusion ROPIVACAINE READYFUSOR
La pompe à perfusion ROPIVACAINE READYFUSOR est un système dapplication de médicament non-électrique conçu pour être utilisé sur le lieu dintervention.
Le système dadministration contient un flacon à soufflet contenant 250 ml solution de chlorhydrate de ropivacaïne monohydraté pour perfusion. Un tube avec raccord Luer y est raccordé en permanence. Le tube avec le raccord Luer ainsi que le cathéter multi-perforé stérile (si inclus dans le set) sont sans latex.
Pendant lintervention, un cathéter multi-perforé doit être placé dans la plaie. Le cathéter inclus dans certains sets (voir section 6.5) diffuse uniformément ROPIVACAINE READYFUSOR sur toute la longueur de la plaie dans un rayon de 360°.
Le système dadministration contient une jauge qui permet de déterminer la quantité de liquide restant pendant le schéma de diffusion thérapeutique.
|
|
|
|
1. Capuchon du système dadministration |
6. Tuyau |
|
2. Flèche indicatrice |
7. Élément de fixation |
|
3. Position MARCHE |
8. Filtre |
|
4. Flèche de surveillance |
9. Bouchon du tuyau |
|
5. Fenêtre de la jauge |
10. Indicateurs circulaires |
Instructions pour lutilisation
|
1. Retirez la fermeture inviolable du système dadministration. Si le scellé a été retiré ou endommagé, nutilisez pas ce système dadministration.
|
|
|
2. Amorcez la diffusion du liquide en tournant le capuchon (1) dans le sens des aiguilles dune montre jusquà ce que la flèche indicatrice (2) soit alignée avec la position ON (3).
|
´ |
|
3. Retirez le capuchon du tuyau (9) et vérifiez que le dispositif a été amorcé en regardant le liquide couler dans le tuyau.
|
|
|
4. Connectez le tuyau (6) du système dadministration au port du patient.
|
|
|
5. Placez le système dadministration dans la poche de transport fournie. La poche de transport peut être attachée en bandoulière à lépaule du patient ou serrée autour de la taille comme une ceinture.
|
|
|
6. La diffusion du liquide peut être observée par la fenêtre de la jauge (5) du système dadministration. Le système diffusera environ 5 ml de liquide par heure.
|
|
|
7. Ladministration est terminée lorsque lunité est vide comme lindique la position des flèches vertes de surveillance (4) dans la fenêtre de la jauge.
|
|
|
8. Retirez le système dadministration du patient lorsque ladministration est terminée. |
|
|
9. Après utilisation, veuillez éliminer le système dadministration vide, y compris tout reste de solution. |
|
Mises en garde
· Le système dadministration est exclusivement destiné à un usage unique. Ne réutilisez pas le système dadministration et ne le reconnectez pas.
· Le système dadministration ne doit pas être stérilisé à lautoclave. Le trajet du liquide dans le dispositif a été stérilisé.
· Tout vrillage du tube doit être évité, en effet, dans le cas contraire, le maintien du bloc nerveux périphérique ne peut être garanti et la ré-institution du bloc nécessitera de renouveler ladministration de ropivacaïne 7,5 mg/ml (voir aussi rubrique 4.2).
· Aucun bandage serré ne doit être placé autour du tube.
· Il convient de ne pas utiliser lapplicateur sil est endommagé ou fendu ou si le port du tube semble cassé, fendu ou endommagé de quelque manière que ce soit.
· Il convient de ne pas reconnecter lapplicateur si celui-ci est débranché accidentellement pendant que le médicament est appliqué, car cela pourrait provoquer une infection.
· Le patient ne doit pas prendre de bain ni de douche avec lapplicateur ou tant que le tube est en place sous la peau, car cela pourrait provoquer une infection.
· Le patient ne doit pas toucher le pansement sur la plaie ou le tube sous la peau, car cela pourrait provoquer une infection.
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
Garden Cottage, Hascombe Road
Godalming, Surrey GU8 4AE
Royaume-Uni
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 34009 550 467 1 4 : 250 mL de solution en flacon (PEHD) contenu dans un système d'administration
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste II
Médicament réservé à lusage hospitalier.