RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM - Mis à jour le : 13/08/2024
TESTOSTERONE EVER PHARMA 250 mg/1 mL, solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Enanthate de testostérone.................................................................................................... 250 mg
Correspondant à 180 mg de testostérone
Pour une ampoule de 1 mL.
Excipient à effet notoire : 342,0 mg de benzoate de benzyle par ampoule.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution huileuse limpide de teinte jaunâtre.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Une ampoule de 1 mL de TESTOSTERONE EVER PHARMA (correspondant à 250 mg d'énanthate de testostérone) est injectée toutes les deux à trois semaines.
Pour le traitement d'entretien : 250 mg de TESTOSTERONE EVER PHARMA par voie intramusculaire toutes les trois à six semaines, selon les besoins individuels.
Initiation du traitement
Les taux sériques de testostérone doivent être mesurés avant et pendant linitiation du traitement.
Maintien et individualisation du traitement
Une surveillance attentive des taux de testostérone sérique est nécessaire pendant le maintien du traitement. Il est conseillé de mesurer régulièrement les taux sériques de testostérone. Les mesures doivent être effectuées à la fin d'un intervalle d'injection et les symptômes cliniques doivent être pris en compte. Ces taux sériques doivent se situer dans le tiers inférieur de la fourchette normale. Des taux sériques en dessous de la normale pourraient indiquer quil est nécessaire de raccourcir les intervalles entre les injections. En cas de taux sériques élevés, une augmentation de lintervalle de temps entre les injections peut être envisagée.
Populations particulières
Population pédiatrique
TESTOSTERONE EVER PHARMA n'est pas indiqué chez l'enfant ni ladolescent (voir rubrique 4.4).
Lefficacité et la tolérance de lénanthate de testostérone nont pas été suffisamment établies chez l'enfant et ladolescent.
Patients âgés
Des données limitées ne suggèrent pas la nécessité dadapter les doses chez les patients âgés (voir rubrique 4.4).
Insuffisance hépatique
Aucune étude formelle na été conduite chez des patients présentant une insuffisance hépatique. Lutilisation de TESTOSTERONE EVER PHARMA est contre-indiquée chez les hommes en cas de tumeur hépatique ou dantécédents de tumeur hépatique (voir rubrique 4.3).
Insuffisance rénale
Aucune étude formelle na été conduite chez des patients présentant une insuffisance rénale.
Mode dadministration
Pour injection intramusculaire.
La solution huileuse doit être administrée très lentement (plus de deux minutes) (voir rubriques 4.4 et 4.8). TESTOSTERONE EVER PHARMA est strictement destiné à l'injection intramusculaire. Il faut faire attention d'injecter TESTOSTERONE EVER PHARMA profondément dans le muscle fessier en suivant les précautions habituelles pour l'administration intramusculaire. Des précautions particulières doivent être prises pour éviter l'injection intravassale (voir rubrique 4.4 « Administration»). Le contenu d'une ampoule doit être injecté par voie intramusculaire immédiatement après ouverture. Voir la rubrique 6.6 pour les instructions sur l'ouverture de l'ampoule en toute sécurité.
L'utilisation de TESTOSTERONE EVER PHARMA est contre-indiquée chez les hommes ayant :
· Hypersensibilité à la substance active ou à lun des excipients mentionnés à la rubrique 6.1.
· Cancer androgéno-dépendant de la prostate ou de la glande mammaire chez lhomme.
· Hypercalcémie.
· Tumeur hépatique ou antécédents de tumeur hépatique.
· Adénome prostatique.
L'utilisation de TESTOSTERONE EVER PHARMA chez les femmes est contre-indiquée.
4.4. Mises en garde spéciales et précautions d'emploi
Chez lenfant, la testostérone, en plus de la virilisation, peut entraîner une accélération de la croissance et de la maturation osseuse ainsi quune soudure précoce des cartilages de conjugaison, ceci conduisant à une diminution de la taille définitive. En conséquence, l'utilisation de TESTOSTERONE EVER PHARMA a n'est pas recommandée chez les enfants et les adolescents.
Patients âgés
Lexpérience disponible concernant la sécurité et lefficacité de TESTOSTERONE EVER PHARMA utilisé chez les patients âgés de plus de 65 ans est limitée. Actuellement, il n'existe pas de consensus quant aux valeurs de référence de la testostéronémie en fonction de l'âge. Cependant, la diminution des valeurs physiologiques de la testostéronémie avec l'âge doit être prise en compte.
Examen médical et examens biologiques
Examen médical
Avant d'instaurer un traitement par la testostérone, tous les patients doivent subir impérativement un examen approfondi afin d'écarter tout risque de cancer de la prostate préexistant. Une surveillance attentive et régulière de la prostate et des seins devra être effectuée selon les méthodes usuelles recommandées (toucher rectal et dosage du PSA sérique), au moins une fois par an et deux fois par an chez les sujets âgés et les patients à risque (facteurs cliniques ou familiaux). Les recommandations locales pour la surveillance de la tolérance dans le cadre d'un traitement substitutif de la testostérone doivent être prises en considération.
Examens biologiques
Les taux de testostérone doivent être contrôlés avant le début du traitement, puis à intervalles réguliers pendant le traitement. La posologie doit être adaptée à chaque patient, afin de sassurer que les taux de testostérone sont maintenus à un niveau eugonadique.
Chez les patients recevant un traitement androgénique au long cours, les paramètres biologiques suivants doivent être contrôlés régulièrement : taux dhémoglobine et hématocrite, fonction hépatique et bilan lipidique (voir rubrique 4.8).
En raison de la variabilité des résultats d'analyse entre les différents laboratoires, tous les dosages de testostérone doivent être effectués par le même laboratoire pour un sujet donné.
Tumeurs
Les androgènes peuvent accélérer lévolution dun cancer infra-clinique de la prostate et dune dhyperplasie bénigne de la prostate, en particulier en cas d'utilisation de fortes doses. A ce jour, il nexiste pas de preuve quils augmentent le risque de cancer de la prostate ou dhyperplasie bénigne de la prostate. De même, il nexiste pas de preuve quils peuvent convertir un cancer de la prostate infra-clinique en un cancer de la prostate cliniquement détectable, même si cela ne peut être totalement exclu à ce jour. Par conséquent, il est impératif d'éliminer un cancer de la prostate avant de débuter un traitement avec des préparations à base de testostérone.
TESTOSTERONE EVER PHARMA doit être utilisé avec prudence chez les patients ayant un cancer avec un risque d'hypercalcémie (et d'hypercalciurie associée) lié à des métastases osseuses. Il est recommandé d'assurer un suivi régulier de la calcémie chez ces patients.
Des cas de tumeurs hépatiques bénignes et malignes ont été signalées, chez des utilisateurs de substances hormonales telles que les androgènes. En cas de troubles abdominaux sévères, dhypertrophie hépatique ou des signes d'hémorragie intra-abdominale survenant chez les hommes utilisant TESTOSTERONE EVER PHARMA, une tumeur hépatique doit être considérée dans le diagnostic différentiel et, si nécessaire, le traitement doit être arrêté (voir rubrique 4.3).
Insuffisance cardiaque, hépatique et rénale
Chez les patients atteints dinsuffisance cardiaque, hépatique ou rénale sévère ou de cardiopathie ischémique, le traitement par testostérone peut entraîner des complications sévères caractérisées par un dème avec ou sans insuffisance cardiaque congestive. Dans ce cas, le traitement doit être arrêté immédiatement (voir rubrique 4.3).
Insuffisance hépatique ou rénale
Aucune étude n'a été réalisée pour démontrer l'efficacité et la sécurité de ce médicament chez les patients atteints d'insuffisance rénale ou hépatique. Par conséquent, le traitement substitutif par testostérone doit être utilisé avec prudence chez ces patients.
Insuffisance cardiaque
Il convient dêtre prudent chez les patients ayant des facteurs de risque d'dème, par exemple en cas d'insuffisance cardiaque, hépatique ou rénale sévère ou de cardiopathie ischémique, car le traitement par androgènes peut entraîner une augmentation hydrosodée. En cas de complications sévères caractérisées par un dème, avec ou sans insuffisance cardiaque congestive, le traitement doit être interrompu immédiatement (voir rubrique 4.8).
La testostérone peut entraîner une augmentation de la pression artérielle. Par conséquent, TESTOSTERONE EVER PHARMA doit être utilisé avec précaution chez les hommes présentant une hypertension.
Troubles de la coagulation
En règle générale, les restrictions à lutilisation dinjections intramusculaires chez les patients ayant des troubles acquis ou héréditaires de la coagulation sanguine doivent être observées.
La testostérone et ses dérivés peuvent majorer lactivité des anticoagulants oraux dérivés de la coumarine (voir également la rubrique 4.5).
La testostérone doit être utilisée avec prudence chez les patients souffrant de thrombophilie ou présentant des facteurs de risque de thromboembolie veineuse (TEV) car des cas dévènements thromboemboliques ont été rapportés chez ces patients sous traitement par testostérone lors détudes et de suivis post commercialisation (par exemple : thrombose veineuse profonde, embolie pulmonaire, thrombose oculaire). Chez les patients atteints de thrombophilie, des cas de TEV ont été rapportés même sous traitement anticoagulant. Par conséquent, la poursuite du traitement par la testostérone après un premier événement thrombotique doit être évaluée attentivement. En cas de poursuite du traitement, d'autres mesures doivent être prises afin de réduire au maximum le risque de TEV.
Autres
TESTOSTERONE EVER PHARMA doit être utilisé avec prudence chez les patients souffrant dépilepsie, de migraine, en raison du risque daggravation de leur état.
Une augmentation de la sensibilité à l'insuline peut survenir chez les patients traités par des androgènes qui atteignent des concentrations plasmatiques normales de testostérone après un traitement substitutif. Par conséquent, la dose d'agents hypoglycémiants peut devoir être réduite.
Certains signes cliniques, tels quune irritabilité, une nervosité, une prise de poids, des érections prolongées ou fréquentes peuvent indiquer une exposition excessive aux androgènes et nécessiter un ajustement posologique.
Si dans des cas individuels, des érections fréquentes ou persistantes surviennent, la dose doit être réduite ou le traitement interrompu afin d'éviter des lésions du pénis.
Une apnée du sommeil préexistante peut saggraver sous traitement.
Les athlètes traités par un traitement substitutif de testostérone dans l'hypogonadisme masculin primaire et secondaire doivent être informés que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Les androgènes ne doivent pas être utilisés pour développer la masse musculaire des sujets en bonne santé, ni pour augmenter les capacités physiques.
TESTOSTERONE EVER PHARMA doit être stoppé de façon permanente si les symptômes d'une exposition excessive aux androgènes persistent ou réapparaissent pendant le traitement avec le schéma posologique recommandé.
TESTOSTERONE EVER PHARMA ne doit pas être utilisé chez la femme, car en fonction de la sensibilité individuelle aux androgènes, elle peut développer des signes de virilisation tels quacné, hirsutisme, modification de la voix.
Abus médicamenteux et dépendance
La testostérone a fait lobjet dutilisations abusives, généralement à des doses supérieures à celles recommandées dans lindication approuvée et en association avec dautres stéroïdes androgènes anabolisants. Lutilisation abusive de testostérone et dautres stéroïdes androgènes anabolisants peut provoquer des effets indésirables graves incluant : des événements cardiovasculaires (avec issue fatale dans certains cas), hépatiques et/ou psychiatriques. Lutilisation abusive de testostérone peut entraîner une dépendance et des symptômes de sevrage en cas de réduction significative de la dose ou dinterruption brutale de lutilisation. Lutilisation abusive de testostérone et dautres stéroïdes androgènes anabolisants présente de graves risques pour la santé et doit être déconseillée.
Chez les enfants, la testostérone, en plus de la masculinisation, peut provoquer une croissance et une maturation osseuses accélérées et une fermeture épiphysaire prématurée, réduisant ainsi la taille finale.
Administration
Comme avec toutes les solutions huileuses, TESTOSTERONE EVER PHARMA doit uniquement être injecté par voie intramusculaire et très lentement (plus de deux minutes). Une micro-embolie pulmonaire due aux solutions huileuses peut entraîner des signes et symptômes tels que toux, dyspnée, douleurs thoraciques. Dautres signes et symptômes incluant des réactions vaso-vagales peuvent survenir, tels que, malaise, hyperhidrose, étourdissements, paresthésies ou syncope. Ces réactions peuvent se produire pendant ou immédiatement après l'injection et sont réversibles. Le patient doit donc être surveillés pendant et immédiatement après chaque injection afin de permettre une détection précoce des signes et symptômes possibles de microembolie huileuse pulmonaire. Le traitement est généralement symptomatique, par exemple par oxygénothérapie.
De possibles réactions anaphylactiques après l'injection de TESTOSTERONE EVER PHARMA ont été signalées.
Informations sur les excipients
Ce médicament contient 342,0 mg de benzoate de benzyle dans chaque ampoule de 1 mL.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Médicaments utilisés pour traiter la douleur ou l'inflammation
Les médicaments pour le traitement de l'inflammation ou de la douleur ont une influence sur la production de testostérone.
Anticoagulants oraux
Le statut de coagulation doit être surveillé attentivement lorsque TESTOSTERONE EVER PHARMA est administré avec des dérivés coumariniques, car cette association pourrait entraîner une augmentation du risque hémorragique par effet direct sur la coagulation et/ou les systèmes fibrinolytiques. Une surveillance accrue du temps de prothrombine et un contrôle plus fréquent de l'INR est recommandée.
Adaptation de la posologie de lantivitamine K pendant le traitement par androgène et à son arrêt.
Hypoglycémiants
L'effet hypoglycémiant des antidiabétiques peut être renforcé Par conséquent, une diminution de la posologie des médicaments hypoglycémiants peut être nécessaire.
Autres interactions
L'administration concomitante de testostérone avec de l'ACTH ou des corticostéroïdes peut favoriser la formation d'dèmes ; Ainsi, ces substances actives doivent être administrées avec prudence, en particulier chez les patients atteints de maladies cardiaques ou hépatiques ou chez les patients prédisposés à l'dème.
Interactions avec les tests de laboratoire : Les androgènes peuvent diminuer les taux de globuline liant la thyroxine, ce qui entraîne une diminution des taux sériques totaux de T4 et une augmentation de l'absorption de la résine T3 et T4. Les taux d'hormones thyroïdiennes libres restent cependant inchangés et il n'y a aucune preuve clinique de dysfonctionnement thyroïdien.
4.6. Fertilité, grossesse et allaitement
Grossesse
TESTOSTERONE EVER PHARMA est indiqué chez lhomme uniquement. TESTOSTERONE EVER PHARMA nest pas indiqué chez la femme enceintes (voir rubrique 5.3).
TESTOSTERONE EVER PHARMA est indiqué chez lhomme uniquement. TESTOSTERONE EVER PHARMA nest pas indiqué chez les femmes qui allaitent (voir rubrique 5.3).
Fertilité
Le traitement de substitution par TESTOSTERONE EVER PHARMA peut réduire la spermatogénèse de manière réversible (voir rubriques 4.8 et 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Résumé du profil de sécurité
Les effets indésirables les plus fréquemment observés sous traitement par la testostérone enanthate sont la douleur au site d'injection, la rougeur au site d'injection, la toux et/ou la dyspnée pendant ou immédiatement après l'injection.
Concernant les effets indésirables associés à lutilisation dandrogènes, voir également la rubrique 4.4.
Les effets indésirables sont répertoriés par classes de systèmes d'organes MedDRA. L'évaluation des effets indésirables est fondée sur les groupes de fréquences suivants :
Très fréquent : ≥1/10
Fréquent : ≥1/100 à <1/10
Peu fréquent : ≥1/1 000 à <1/100
Rare : ≥1/10 000 à <1/1 000
Très rare : <1/10 000
Fréquence indéterminée : ne peut être estimée sur la base des données disponibles
Liste tabulée des effets indésirables
|
Classe de systèmes dorganes |
Effet indésirable |
Fréquence |
|
Tumeurs bénignes, malignes et non précisées (incl kystes et polypes) |
Tumeurs du foie bénignes et malignes (voir rubrique 4.4) |
Inconnue |
|
Affections hématologiques et du système lymphatique |
Polyglobulie |
Inconnue |
|
Augmentation de lhématocrite Augmentation de la numération des globules rouges Augmentation du taux dhémoglobine |
Fréquent |
|
|
Affections du système immunitaire |
Hypersensibilité |
Inconnue |
|
Troubles du métabolisme et de la nutrition |
Prise de poids |
Fréquent |
|
Hypercalcémie Rétention hydrique |
Inconnue |
|
|
Affections psychiatriques |
Dépression Anxiété |
Inconnue |
|
Affections du système nerveux |
Maux de tête Paresthésie |
Inconnue |
|
Affections cardiaques |
Trouble du système circulatoire |
Inconnue |
|
Affections gastro-intestinales |
Troubles abdominaux Hémorragie intra-abdominale Nausée |
Inconnue |
|
Affections hépatobiliaires |
Tests de la fonction hépatique anormaux Ictère Élargissement du foie |
Inconnue |
|
Affections de la peau et du tissu sous-cutané |
Acné Alopécie Rash Urticaire Prurit Calvitie masculine |
Inconnue |
|
Affections musculo-squelettiques et systémiques |
Fermeture épiphysaire prématurée* Augmentation de la formation osseuse |
Inconnue |
|
Troubles généraux et anomalies au site dadministration |
Réactions au site dinjection** Asthénie dème |
Inconnue |
|
Investigations |
Augmentation des antigènes prostatiques spécifiques (PSA) |
Inconnue |
|
Affections des organes de reproduction et du sein |
Augmentation de la libido Diminution de la libido Gynécomastie Trouble de la prostate Augmentation de lérection Spermatogenèse anormale Puberté précoce* |
Inconnue |
*Chez les hommes prépubères
**Douleur au site d'injection, érythème au site d'injection, induration au site d'injection, gonflement au site d'injection, inflammation au site d'injection
Description de certains effets indésirables particuliers
Des injections de solutions huileuses telles que TESTOSTERONE EVER PHARMA ont été associées à des réactions systémiques telles que toux, dyspnée, douleur thoracique. Dautres signes et symptômes incluant des réactions vaso-vagales peuvent survenir tels que malaise, hyperhidrose, étourdissements, paresthésies ou syncope (voir rubrique 4.4).
Un traitement à fortes doses ou à long terme avec la testostérone augmente la tendance à la rétention hydrosodée et aux dèmes.
La spermatogénèse est inhibée par le traitement à long terme et à fortes doses par la testostérone enanthate.
Si dans des cas individuels, des érections fréquentes ou persistantes surviennent, la dose doit être réduite ou le traitement interrompu afin d'éviter des lésions du pénis.
Lutilisation de TESTOSTERONE EVER PHARMA pourrait être associée à un risque fréquent daugmentation de lhématocrite, de la numération des globules rouges et du taux dhémoglobine. Cette fréquence a été reliée à lutilisation de médicaments contenant de la testostérone.
Des réactions dhostilité et dagressivité ainsi quune augmentation de la pilosité ont été rapportées sous traitement avec des préparations contenant de la testostérone.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Aucune mesure thérapeutique autre que larrêt du traitement ou une réduction de la dose nest nécessaire après un surdosage.
Les données sur la toxicité aiguë montrent que TESTOSTERONE EVER PHARMA peut être classé comme non toxique après une seule prise. Même dans le cas d'une administration par inadvertance d'un multiple de la dose requise pour le traitement, aucun risque de toxicité aiguë n'est attendu.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ANDROGENES, dérivés du 3-oxoandrostène (4), code ATC : G03BA03.
TESTOSTERONE EVER PHARMA est un ester de l'hormone sexuelle masculine naturelle testostérone et présente tous les effets pharmacologiques de l'hormone naturelle. Il diffère en ce qu'il a un effet de dépôt, en raison du fait que TESTOSTERONE EVER PHARMA n'est que lentement dégradé en testostérone dans le corps.
Mécanisme d'action
Ce médicament est un androgène synthétique et un stéroïde anabolisant et est donc un agoniste du récepteur des androgènes, la cible biologique des androgènes comme la testostérone et la dihydrotestostérone (DHT).
Il a de forts effets androgènes et des effets anabolisants modérés, ce qui le rend utile pour la masculinisation et adapté au traitement de substitution des androgènes.
L'énanthate de testostérone est un ester de testostérone et une prodrogue de longue durée de la testostérone dans le corps. Pour cette raison, il est considéré comme une forme naturelle et bio-identique de testostérone.
Effets pharmacodynamiques
En fonction de l'organe cible, le spectre d'activité de la testostérone est principalement androgène (par exemple, prostate, vésicules séminales, épididyme) ou protéique anabolisant (muscle, os, hématopoïèse, rein, foie).
La testostérone est responsable de l'expression des caractéristiques masculines au cours du développement ftal, de la petite enfance et de la puberté, puis du maintien du phénotype masculin et des fonctions androgènes dépendantes (par exemple, la spermatogenèse, les glandes sexuelles accessoires). Il remplit également des fonctions, par exemple dans la peau, les muscles, le squelette, les reins, le foie, la moelle osseuse et le SNC.
Chez les sujets hypogonadiques, la testostérone produit : un arrêt de croissance osseuse, par soudure des cartilages de conjugaison, généralement précédé d'une poussée de croissance, un développement des organes génitaux externes et internes, une poussée de la pilosité, une mue de la voix, l'apparition de la libido, un effet général d'anabolisme protidique, un développement de la musculature squelettique, une réduction de l'élimination urinaire d'azote, sodium, potassium, chlore, phosphore et eau.
N.B. : La testostérone n'entraîne pas le développement testiculaire : elle diminue la sécrétion hypophysaire de gonadotrophines.
5.2. Propriétés pharmacocinétiques
Après injection intramusculaire de 200 mg d'énanthate de testostérone, les taux sériques maximaux (1233 ± 484 ng/mL) ont été atteints dans les 24 heures suivant l'administration chez les sujets hypogonadiques. Les concentrations étaient supérieures aux niveaux physiologiques normaux pendant environ 9 jours.
Distribution
Dans le sérum des hommes, environ 98% de la testostérone circulante est liée à la SHBG (Sex Hormone Binding Globulin) et à l'albumine. Seule la fraction libre de testostérone est considérée comme biologiquement active.
Biotransformation
La testostérone, obtenue par clivage de la liaison ester de lénanthate de testostérone, est métabolisée et excrétée de la même manière que la testostérone endogène.
Élimination
Environ 90 % d'une dose intramusculaire de testostérone est excrétée dans l'urine sous forme de conjugués glucuroniques et d'acide sulfurique de la testostérone et de ses métabolites ; Environ 6 % sont excrétés dans les matières fécales, principalement sous forme non conjuguée. Après avoir reçu une injection intramusculaire de 200 mg d'énanthate de testostérone, la demi-vie apparente était de 4,2 jours chez les sujets hypogonadiques.
5.3. Données de sécurité préclinique
Des études chez l'animal ont montré que la formulation a un potentiel minimal de sensibilisation ou d'irritation locale après une injection intramusculaire. Les études systémiques à long terme n'ont montré aucune preuve de toxicité testiculaire, bien qu'une inhibition temporaire de la spermatogenèse puisse se produire. Aucune étude de fertilité avec TESTOSTERONE EVER PHARMA n'a été réalisée. TESTOSTERONE EVER PHARMA ne doit pas être administré pendant la grossesse en raison de la possibilité de virilisation du ftus féminin. Cependant les recherches sur les effets embryo-toxiques, en particulier sur les effets tératogènes, nont fourni aucun élément laissant prévoir un trouble ultérieur du développement organique.
Les études in vitro de mutagénicité ont donné des résultats négatifs.
Huile de ricin raffinée, benzoate de benzyle.
30 mois.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
1 mL de solution dans une ampoule en verre brun.
Boîtes en carton de 1, 3, 5 ou 10 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières délimination et de manipulation
Le produit doit être inspecté visuellement pour détecter les particules avant l'administration. Seule une solution claire exempte de particules doit être utilisée.
Le médicament est à usage unique et toute solution non utilisée doit être éliminée conformément à la réglementation en vigueur.
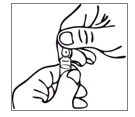
Remarques sur la manipulation de l'ampoule OPC (One-Point-Cut) :
La pointe colorée sous l'ampoule comporte une marque pré-entaillée, permettant ainsi déviter de limer la base de la pointe. Avant ouverture, assurez-vous que toute solution dans la partie supérieure de l'ampoule s'écoule vers la partie inférieure. Utilisez les deux mains pour ouvrir ; Tout en tenant la partie inférieure de l'ampoule dans une main, utilisez l'autre main pour casser la partie supérieure de l'ampoule dans le sens opposé à la pointe colorée.
|
|
7. TITULAIRE DE LAUTORISATION DE MISE SUR LE MARCHE
Oberburgau 3
4866 Unterach am Attersee
Autriche
8. NUMERO(S) DAUTORISATION DE MISE SUR LE MARCHE
· 34009 302 998 9 0 : 1 mL en ampoule (verre brun). Boîte de 1.
· 34009 551 032 8 8 : 1 mL en ampoule (verre brun). Boîte de 3.
· 34009 551 032 9 5 : 1 mL en ampoule (verre brun). Boîte de 5.
· 34009 551 033 0 1 : 1 mL en ampoule (verre brun). Boîte de 10.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE LAUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Prescription initiale réservée aux spécialistes en endocrinologie diabétologie nutrition, en urologie, en gynécologie ou en médecine et biologie de la reproduction andrologie.
Renouvellement non restreint.